前段时间看到一个肺癌案例让我比较吃惊,因为这位患者的情形已经不像传统肺癌那么严重和激烈,而是有一种慢病化趋势了,一位45岁的肺癌患者已经与癌症抗争了6年之久,且目前状态甚至达到了“生活恢复到了发病前的平静……除了有点拉肚子其他都没啥影响、正常上班工作”,和我们以往的认知完全不一样。且这种情形已经不是个例了,让人感慨医学发展的日新月异。
今天来和大家聊聊肺癌这种让人谈之色变的癌症。
01,关于肺癌
为什么会出现这种肺癌慢病化的现象?这要从一种特殊的肺癌聊起。
说到肺癌,可以说是让人谈之色变。肺癌是全世界发病率和死亡率最高的肿瘤。在我国人群死亡全因素里,肺癌是位列导致国人死亡的恶性肿瘤第一名【1】。根据最新统计,2022年,在我国所有的恶性肿瘤新发病例里,肺癌以18.06%的发病率高居我国恶性肿瘤发病第一名,而在死亡率方面,因为肺癌导致的死亡人数更是占了恶性肿瘤死亡的23.9%,同样是位列第一【2】。这两个第一名无疑意味着肺癌这种恶性肿瘤的严峻性。
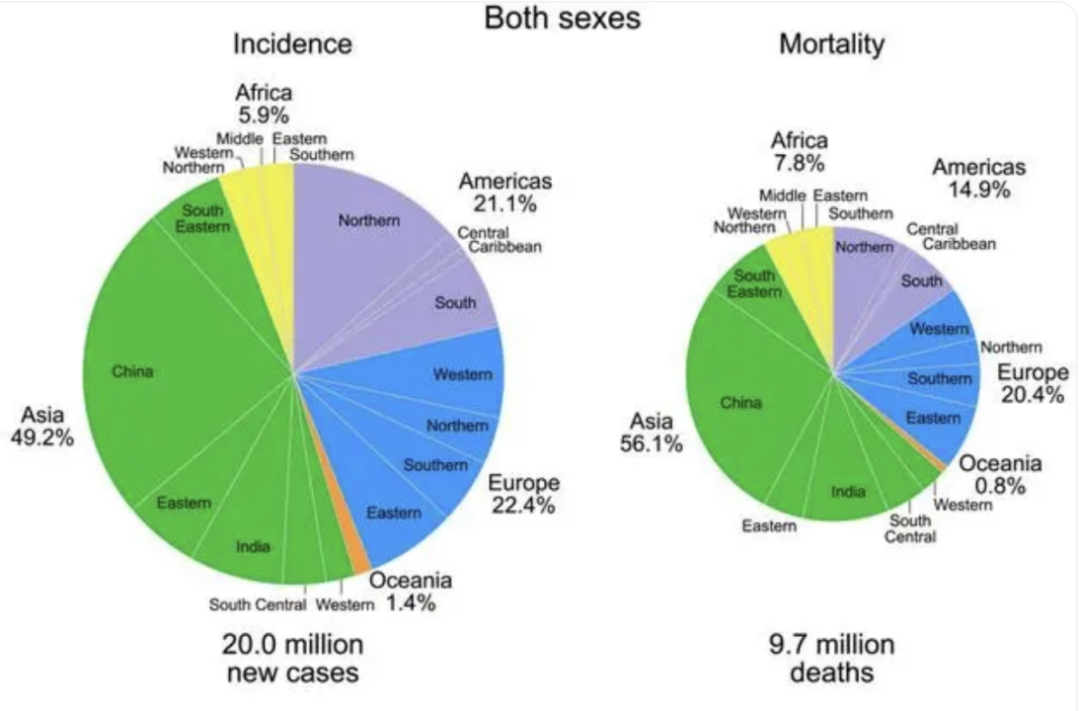
正因为如此,作为第一癌,肺癌的关注程度是非常高的,自然而然,我们也会追问,为什么肺癌发病率和死亡率如此之高?
**02,**肺癌高发,但也不能乱归因
估计很多人面对这个问题,肯定会想到一系列肺癌的致癌因素,比如典型的就是和呼吸有关的吸烟问题,这些年来我们也一直把肺癌和吸烟强关联,从公卫宣传角度,这的确是没毛病,毕竟吸烟的确和肺癌关系密切,而这种外在因素如果控制好,那么可以很好地降低肺癌的发病率。
但是,如果你只以为肺癌和吸烟有关,那可能就不一定对了,因为你一定听过类似的话“xx不吸烟不喝酒,可是依然得了肺癌”,这也是我们在现在宣传中经常遇到的问题,因为不少人就会以此反驳。
**03,**特殊的肺癌-无吸烟史肺癌
事实上,这个说法,某种程度还真的不一定是错的,因为,在肺癌中有一种另类的存在那就是无吸烟史肺癌(lung cancer in never smokers,LCINS),或者叫不吸烟者肺癌,顾名思义就是指不吸烟的人,或者那种极少吸烟的,比如一生中吸烟<100支的人。按理说,他们已经远离了吸烟这个公认的肺癌致癌因素,但是他们依然会得肺癌。
值得一提的是,你不要觉得无吸烟史肺癌是罕见现象,事实上,这个比例并不低,有10-25%的肺癌患者是无吸烟史肺癌,这比例相当高了。而且,近些年来,无吸烟史肺癌发病率甚至有上升的趋势,这种无吸烟史肺癌而且还很严重,往往治疗和预后不大好,这就不得不让我们重视了。
于是研究人员对无吸烟史肺癌进行了深入的研究,结果发现,这类肺癌比较特殊,因为他们在基因上存在特殊的变异,典型的就是间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)变异,这是一个位于2号染色体和5号染色体易位后一段可以编码核仁磷酸蛋白的片段【3】。
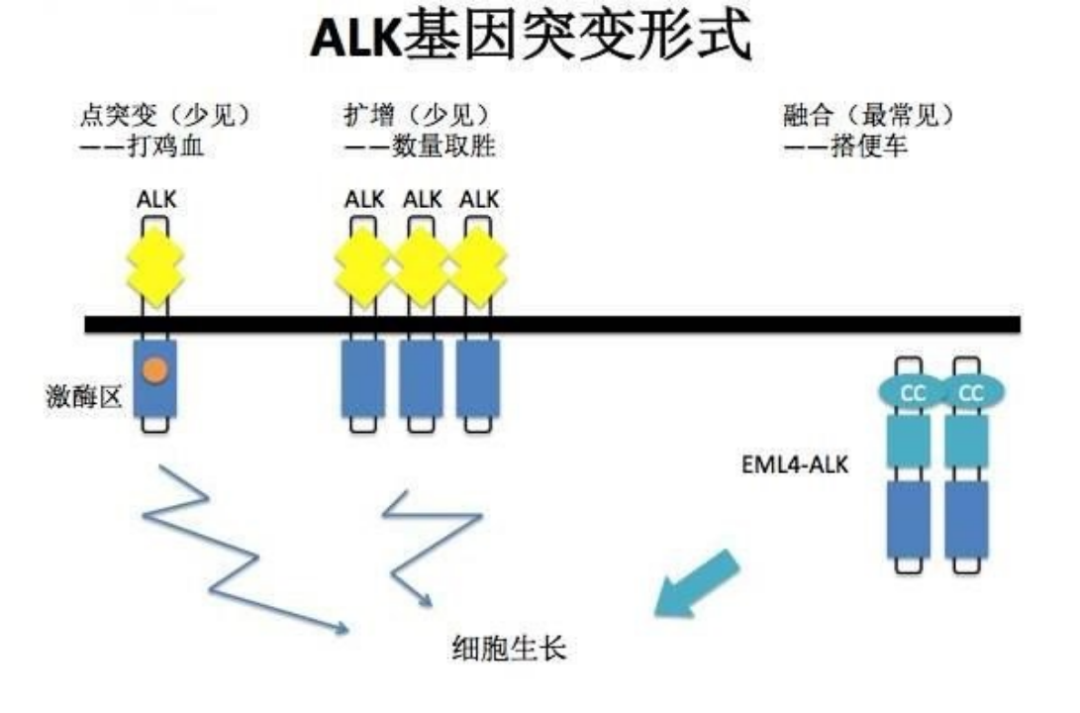
这种基因重排导致的变异会成为非小细胞肺癌(non-small cell lung cance,NSCLC)的重要驱动基因,从而引发部分非小细胞肺癌的发生。研究发现,ALK基因融合阳性患者占非小细胞肺癌患者的3-7%,而非小细胞肺癌也是肺癌的主要类型,约85%的肺癌属于NSCLC。
和其他肺癌不同,ALK基因融合也导致了带有这种变异的非小细胞肺癌具有了特殊性。
首先,ALK融合阳性患者和吸烟的关联度很低,基本上7成的ALK融合阳性肺癌患者是不吸烟的。
其次,ALK融合阳性患者发病较早,很多是在四五十岁就发病了,这和传统肺癌六七十岁发病存在着较大的年龄差异。
第三,从组织学分型上,ALK融合阳性变异以腺癌为主(肺癌分为腺癌、鳞癌和小细胞肺癌),且大部分不和其他驱动基因如EGFR、KRAS变异共存。
04,让ALK肺癌变成“幸运肺癌”-靶向治疗
不过,这种特殊性,也使得研究人员意识到,对于ALK基因融合变异,不应该把其当做传统肺癌,而是应该单独作为一类肺癌类型进行研究。
既然已经知道了ALK融合阳性肺癌的驱动基因,那么,在现代医学科学的条件下,自然可以针对ALK融合阳性进行专门的基因靶向治疗,于是,在短短的几年内首个针对ALK融合阳性肺癌的靶向药物克唑替尼就正式上市了。
其机制简单的说,就是针对ALK。靶向药物是酪氨酸激酶抑制剂(ALK-TKI),可以直接应对ALK融合阳性变异,从而起到对肺癌的治疗。
在ALK靶向药物的作用下,ALK融合阳性肺癌的状况被彻底扭转了,在过去,ALK融合阳性患者是很不幸的,晚期患者5年生存率不到10%,这在所有肺癌里都是比较严峻的。但是有了靶向药物之后,直接逆转了这种情形,ALK融合阳性肺癌患者预后提高到了7年多,而且副反应小、生活质量也得到了提高,反而成为了肺癌患者中率先获得高质量优势生存的群体。
于是ALK变异阳性就有了一个新称呼:钻石突变。甚至有人把ALK变异肺癌称为“幸运肺癌”
05,不断进化中的靶向药物
今天我们看到的是ALK融合阳性肺癌已近率先迈入了肺癌慢病化,但是这种过程可不是一蹴而就的,而是不断的总结经验、更新治疗方案的过程。
最初使用的是一代ALK融合阳性抑制剂如克唑替尼(Crizotinib),它在临床上的确取得了显著的疗效,延长了患者的生存期。但是随着治疗,却发现了一些局限性。
首先是耐药性问题,许多患者在接受治疗后一年出现了耐药性,这就很麻烦了,这意味着药物失效,必须寻找新药物。
其次是对于脑转移的控制有限,而脑转移也是ALK肺癌的重要特征之一,就是容易出现癌症在大脑的发展。
这种情况下,新一代药物的研发就是非常有必要了,而像阿来替尼就是二代ALK抑制剂的一种。
在研发过程中,为了解决一代药物的问题,研究人员做出了很多努力,比如为了控制肺癌的脑转移问题,像阿来替尼之类的二代药物普遍提高了血脑屏障的穿透性,从而让药物在大脑中发挥作用,有效降低脑转移程度。同时,对于耐药性的优化也是一个重要革新,阿来替尼如今的耐药性也一定程度得到了解决。
而同时,第三代药物也在更新中,如劳拉替尼(Lorlatinib)等,一方面努力解决耐药性问题,另一方面也可以覆盖更多的靶点。
但是,并不是说,三代药物一定优于二代和一代药物。这是很多时候人们面对癌症治疗时候的一个较大误区。
06,****靶向药物如何打赢ALK肺癌****
事实上,对于ALK肺癌,如何打赢抗癌战,【排兵布阵】至关重要。
首先,要攻守结合。外行看待病情,容易只关注疗效,这在临床上是不合适的。作为一种严重疾病,虽然ALK肺癌已经慢病化了,但是它依然是癌症啊。很多药物是疗效和毒性兼具的,就像大家熟悉的化疗那种杀敌一千自损八百,绝对不能单一角度去看待。同样,慢病化也意味着长期用药,那么这种情况下,药物的安全性和药物相互作用就至关重要了。
事实上,目前所有的癌症药物都是有副作用的,这无法避免,因此要平衡各种药物的使用,尽可能在维持效果和减少副作用之间做一个平衡。
其次,要瞻前顾后。尽管目前靶向药效果良好,但是我们必须面临一个基本事实:靶向药会耐药,而一但耐药了,那么就基本上只能换药了。
因此在临床上,对于ALK肺癌,是不太建议一上来就直接上最新药物,因为一旦这个药物耐药了,那么就会面临“无药可用”的地步。所以用药还需考虑“后手”是否丰富。比如在中国临床肿瘤学会发布的《非小细胞肺癌诊疗指南2023》中,对于ALK融合阳性非小细胞肺癌的治疗推荐用药如下:
首先在一线治疗,也就是治疗的首选药物和方案方面,最优先等级推荐的是阿来替尼【优先推荐】。而之所以如此,是因为一方面,在多个临床证据中都显示阿来替尼安全性高于所有ALK抑制剂,对于长期用药的慢病来说,这是很关键的一点。
其次,阿来替尼的用药优势还表现在后线选择丰富。如果发生了耐药,那么同样也有一系列药物可以供选择,避免了无药可用的问题。

正因为如此, 才可以作为指南推荐的一线用药。同样,在选择其他药物的时候,一样也是要按照前面我们说的标准,既要权衡疗效和安全性,保障慢病长期用药的安全性,同样也要考虑未来耐药后的其他选择,避免无药可用。
目前在一系列靶向药物的支撑下,ALK融合阳性肺癌已经能够很好的得到了缓解,其生存期也得到了很好的延长,这也是为什么大家称之为“幸运癌”。
虽然如此,但是我们必须看到,还有相当多的肺癌目前治疗效果并不好,这一点从肺癌带来的死亡率上也能看出。
但是随着我们对肺癌乃至整个癌症认知的加深,也许未来我们会有更多的药物来应对癌症,从而争取有一天,癌症不再成为笼罩在所有人头上的阴云。
1、Zhou, Maigeng, Haidong Wang, Xinying Zeng, Peng Yin, Jun Zhu, Wanqing Chen, Xiaohong Li et al. "Mortality, morbidity, and risk factors in China and its provinces, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017." The Lancet 394, no. 10204 (2019): 1145-1158.2、Bray, Freddie, Mathieu Laversanne, Hyuna Sung, Jacques Ferlay, Rebecca L. Siegel, Isabelle Soerjomataram, and Ahmedin Jemal. "Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries." CA: a cancer journal for clinicians 74, no. 3 (2024): 229-263.
3、Schneider, Jaime L., Jessica J. Lin, and Alice T. Shaw. "ALK-positive lung cancer: a moving target." Nature cancer 4, no. 3 (2023): 330-343.
来源: 李雷


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 李雷
李雷 
