作者: 汤波
编辑: Yuki
今天,诺贝尔化学奖正式揭晓,能荣获一次诺贝尔奖,可谓是科学家科研生涯的巅峰时刻。由于种种原因,一些做出重大科学发现的科学家遗憾地与诺贝尔奖擦肩而过,也有一些幸运的科学家却两次获得诺贝尔奖,当然后者属于“凤毛麟角”。
迄今为止,全世界两获诺贝尔奖的科学家只有四位 ,包括获得诺贝尔物理学奖和化学奖各一次的波兰裔法国科学家玛丽·居里,两获诺贝尔物理学奖的美国物理学家约翰·巴丁,获得诺贝尔化学奖和和平奖各一次的美国化学家莱纳斯·鲍林,以及今天我们要介绍的 弗雷德里克·桑格 (Frederick Sanger)。

(弗雷德里克·桑格 | Wikimedia Commons)
1988年,70岁的桑格在《生物化学年鉴》上发表了一篇长达28页的文章,文章题目是《序列,序列,还是序列》,高度概括了自己的科研生涯。桑格的一生,的确与生命大分子序列的解密有着不解之缘, 先是首次测定了蛋白质的序列,后来又发明了RNA和DNA测序的新方法 ,因此成为唯一两获诺贝尔化学奖的科学家。
用“拼图游戏”解读蛋白质
1918年,桑格出生在英国西南部一个小乡村里,父亲是名医生,曾经作为传教士到过中国,母亲出生于富裕的棉商家庭。受父母影响,桑格从小对科学非常感兴趣,高中时就立志要从事科学研究。

(11岁的桑格(中)和哥哥、妹妹生活在 一起 | achievement.org)
18岁那年,桑格进入剑桥大学学习自然科学,在生物化学方面表现出色,但是数学和物理勉为其难。1940年,桑格继续在剑桥大学攻读博士学位,主要研究动物体内的赖氨酸(一种氨基酸)代谢,3年后获得博士学位。
博士毕业后,桑格进入剑桥大学生物化学系 查理斯·齐布纳尔 (Charles Chibnall)教授实验室。齐布纳尔教授已在牛胰岛素的结构方面做了很多研究,他建议桑格去破解牛胰岛素的氨基酸组成。这是极富挑战性的研究,因为当时科学家已知道蛋白质是由20种氨基酸组成的,就像一些颜色不同的海洋球串联在一根绳子上,但是大家并不知道这些氨基酸到底是如何排列的,甚至以为蛋白质并没有固定结构。
齐布纳尔和桑格之所以选择将牛胰岛素作为研究对象,主要是因为牛胰岛素是当时少数几种容易获取的高纯度蛋白质之一,结构也相对简单,只有51个氨基酸,关键它还是治疗糖尿病的标准药物。
这项研究就像是给桑格预留的一样,很快,桑格就找到突破口。大多数小朋友都玩过拼图游戏,一个有漂亮图案的纸板被分割成形状各异的小纸片,小朋友很快就能根据不同小纸片形状来拼接成完整的图形,桑格正是想到了拼图游戏。
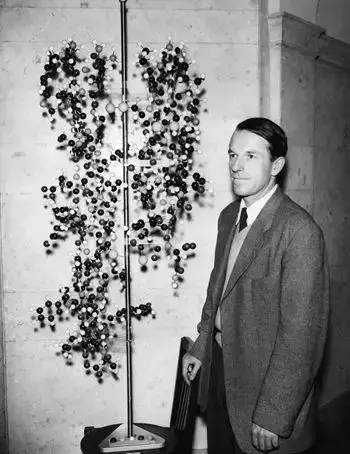
(桑格和胰岛素模型 | achievement.org)
桑格先采用 化整为零 的策略,用蛋白酶将牛胰岛素切成多肽小段,再把一种特殊有机染料结合到多肽段的末端氨基酸上,然后让这个标记有染料的氨基酸脱落下来,让这些脱落的氨基酸在带电极的试纸上“赛跑”,通过与已知的氨基酸进行比较,可以确认它们是哪种氨基酸。
重复这样的试验,就能将每个多肽小段的氨基酸序列测出来,然后拼图游戏开始,将已确认序列的多肽段进行序列比对,确认它们的前后顺序。这样,牛胰岛素的氨基酸序列就全部弄清楚了。
最后,桑格发现胰岛素由两条多肽链组成,一条含有21个氨基酸(A链),另一条含有30个氨基酸(B链),两条多肽链之间通过由两个硫原子组成的链条连接在一起。
这是科学家第一次测定蛋白质的氨基酸组成,也是第一次知道蛋白质有自己特有的结构,开启了人类认识蛋白质这一生命大分子的征程,并为DNA遗传密码的发现奠定了基础。
多年瓶颈,他转向核酸测序
自从1955年破解了牛胰岛素的序列之后,桑格的科研生涯突然陷入了长达10年的瓶颈期。或许是为盛名所累,或许是自己的创新源泉业已枯竭,在这10年里,桑格几乎没有产出什么自己瞧得上眼的科研成果,他把这段时间称为“贫瘠年代”(Lean Years)。

(桑格在1958年的诺贝尔奖庆典上 | bioc.cam.ac.uk)
1962年,原本在英国医学研究理事会工作的桑格,进入新成立的分子生物学实验室。该实验室由诺贝尔化学奖得主马克斯·佩鲁茨(Max Perutz)担任首位主任,弗朗西斯·克里克(Francis Crick)和西德尼·布伦纳(Sydney Brenner)等核酸研究专家也加入其中,桑格负责这个实验室中蛋白质化学实验室的工作,计划继续进行蛋白质结构方面的研究。
由于经常与克里克和布伦纳等分子生物学家接触和交流, 桑格意识到DNA和RNA才是生命科学的未来,开始涉足这一领域 ,不过仍然把关注点放在自己的老本行——测序。当时,科学家刚刚将遗传密码等基础问题弄明白,核酸序列测定仍然是个世界难题。

(桑格在观察一个DNA分子模型 | achievement.org)
桑格很快发现, RNA和DNA的序列并不比蛋白质的好测,因为这些核酸分子特别是RNA极不稳定 ,当时也很难获得高纯度的核酸样品。1965年,美国康奈尔大学的生化学家罗伯特·霍利(Robert Holley)采用类似蛋白质测序“化整为零”的方法,测定了一个只有77个碱基的酵母转运RNA序列。这算得上第一个被测定序列的核酸分子,霍利接着阐明了转运RNA的空间结构,填补了细胞中DNA转录成信使RNA后将氨基酸组装成蛋白质的关键环节,因此与尼伦伯格和霍拉纳一起分享了1968年的诺贝尔奖生理学或医学奖。不过,霍利的测序方法非常麻烦,而且效率低下。
桑格对蛋白质合成过程中核酸的作用也有浓厚兴趣,在霍利测出转运RNA的序列不久,桑格和他的博士后建立了一个基于同位素P(磷)-32放射自显影技术的RNA测序方法,成功测定了大肠杆菌中一个大小为120个碱基的核糖体RNA的序列,效率比以前的方法大幅提高,这一方法也为DNA测序带来了灵感。
成为“经典”的桑格DNA测序法
很快, 桑格又将目光聚焦到更重要的核酸分子DNA上 ,不过DNA测序方法与RNA的截然不同,一方面因为DNA序列都比较长,比如一种简单的噬菌体病毒φX174就有5000多个碱基,如果按照以前的蛋白质和RNA测序方法,工作量实在太大;另一方面缺乏合适的DNA酶,特别是缺乏可切割单个脱氧核苷酸的酶。
显然, DNA测序并不适合用“减法”,那么“加法”行不行呢?
20世纪70年代初,康奈尔大学的华人科学家吴瑞等人建立了一种 位置特异引物延伸测序法 ,即在引物(一段与单链DNA末端互补的寡核苷酸)的引导下,DNA聚合酶能在试管内以单链DNA为模板,将4种游离的脱氧核苷酸(A、T、C和G)组装成互补链,形成双链DNA。如果依次加入这4种脱氧核苷酸,就可测定DNA模板上引物序列之后的每个碱基是什么,从而完成DNA测序。不过这种方法费时费力,效率极低,不适合进行长片段DNA测序。
在此基础上, 经过多年摸索,桑格带领他的博士后发明了 双脱氧终止测序法 。 他们准备了4个试管,每个都加入待测序的模板DNA、DNA聚合酶、寡核苷酸引物单链DNA和4种脱氧核苷酸,但是在每个试管中,这4种脱氧核苷酸中分别有一种会被标记上同位素P-32。当DNA聚合酶催化DNA链延伸反应时,一旦加入同位素标记的脱氧核苷酸,反应就会立即停止,利用凝胶电泳和放射自显影技术,即可轻松检测出链延伸反应在什么脱氧核苷酸上终止的,以此类推,整个模板DNA的序列就能被测出。
1977年,桑格和博士后用这一方法测定了噬菌体病毒φX174的基因组序列,长度为5386个碱基,这是人类第一次测定一个生物体完整的基因组。 1980年,桑格与沃尔特·吉尔伯特(Walter Gilbert)和保罗﹒伯格(Paul Berg)一起分享了诺贝尔化学奖,成为历史上唯一一位两次荣获诺贝尔化学奖的科学家,也是4位两次获得诺贝尔奖的获奖者之一。

(1980年,桑格第二次参加诺贝尔颁奖典礼 | dnalc.cshl.edu)
桑格为人谦和,称自己“ 只是个把实验室搞砸的家伙 ”,“ 在学术上并不辉煌 ”。他曾拒绝英国王室授予的爵士称号,因为他并不想因此与众不同。1983年,65岁的桑格正式退休。2013年11月19日,桑格在剑桥的一家医院于睡梦中与世长辞。
为了纪念桑格,人们将双脱氧终止测序法称为“ 桑格测序法 ”。这一方法很快被广泛用于测定各种功能基因和各种生物基因组的序列,更为人类基因组计划的启动和完成奠定了重要基础。
作者名片

排版:陈小砖
题图来源: achievement.org
参考文献:
Sanger F. Sequences, sequences, and sequences. Annu Rev Biochem. 1988,57:1-28.
Sanger F. The free amino groups of insulin. Biochem J. 1945, 39(5): 507–515.
Holley RW, Apgar J, Everett GA, et al. Structure of a Ribonucleic Acid. Science. 1965, 147 (3664): 1462–1465.
Brownlee GG, Sanger F, Barrell BG. Nucleotide sequence of 5S-ribosomal RNA from Escherichia coli. Nature. 1967, 215 (5102): 735–736.
Wu R. Nucleotide sequence analysis of DNA. Nature New Biology. 1972, 236 (68): 198–200.
Padmanabhan R, Jay E, Wu R. Chemical synthesis of a primer and its use in the sequence analysis of the lysozyme gene of bacteriophage T4. Proceedings of the National Academy of Sciences of the United States of America. 1974,71 (6): 2510–4. Sanger F, Air GM, Barrell BG, et al. Nucleotide sequence of bacteriophage φX174 DNA. Nature. 1977, 265 (5596): 687–695.
Maxam A and Gilbert W. A new method for sequencing DNA. Proceedings of the National Academy of Sciences of the United States of America. 1977, 74 (2): 560–564. Walker John. Frederick Sanger (1918–2013) Double Nobel-prizewinning genomics pioneer. Nature. 2014, 505 (7481): 27.



 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助