近日,一项发表于《异种移植》(Xenotransplantation)期刊的研究,为肾脏异种移植的术后监测提供了新的重要方向。该研究由韩国科学家团队完成,结果表明,通过检测受体血液中的异种来源游离DNA(xd-cfDNA),能够在传统肾功能指标出现异常之前,更早、更灵敏地发现移植肾的损伤迹象,尤其对抗体介导的排斥反应(AMR) 具有突出的预警价值。
研究背景
肾脏异种移植被视为解决器官短缺问题的潜在重要途径。然而,移植后发生的排斥反应是影响移植物长期存活的关键障碍。目前,临床监测主要依赖血清肌酐(Cr)和血尿素氮(BUN)等肾功能指标,但这些指标常在移植肾已经发生显著损伤后才呈现异常。移植肾活检虽可明确诊断,但其有创性限制了频繁实施。因此,开发一种非侵入性、高灵敏度且能早期预警的生物标志物至关重要。在同种异体移植中,供体来源游离DNA(dd-cfDNA)的监测价值已获证实,但该策略在异种移植中的应用效能此前尚不明确。
研究方法
研究团队将经过多重基因编辑(敲除多个介导超急性排斥的糖抗原基因,并敲入多个人源保护基因)的小型猪肾脏,移植给10只食蟹猴,并在术前1周及术后 2、4、6、8 周或终点采集并检测血浆xd-cfDNA。
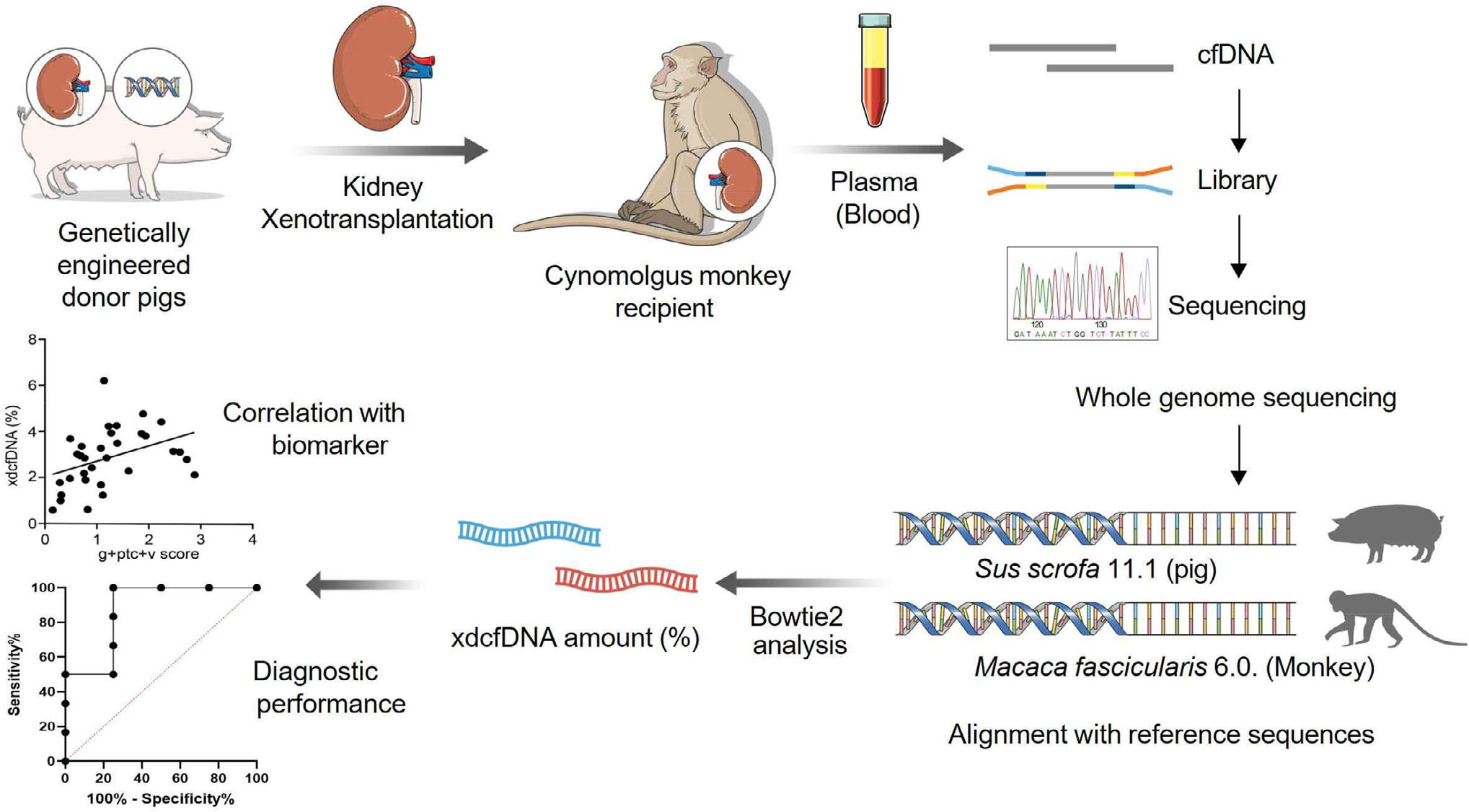
图1.异种移植实验设计流程图
核心发现
01 排斥风险预警窗口提前
血浆xd-cfDNA水平在血清Cr和BUN显著升高前1至2周即开始上升,实现了对排斥风险的更早提示。(图2)
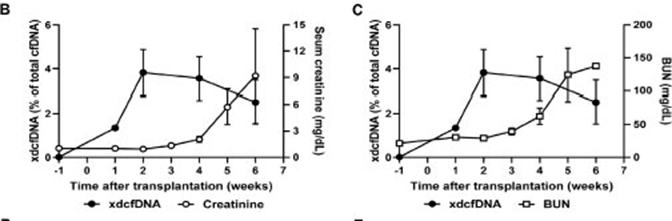
图2.xd-cfDNA与肾功能指标的变化比较
02 卓越的诊断效能
研究确定了血浆xd-cfDNA诊断排斥反应的阈值为2.545%。基于当前研究队列,xd-cfDNA在此阈值下区分“排斥”与“未发生排斥”的敏感度与特异度均达100%(95%CI 64.57%–100% / 43.85%–100%)(图3.)。同时,研究者提出了一个用于早期筛查的、灵敏度更高的预警阈值1.25%。当xd-cfDNA超过预警阈值时,提示需加强监测并辅以其它检查(如供者特异性抗体检测);若其水平持续超过诊断阈值,则建议进行移植肾活检以明确诊断,从而指导免疫抑制方案的及时调整。
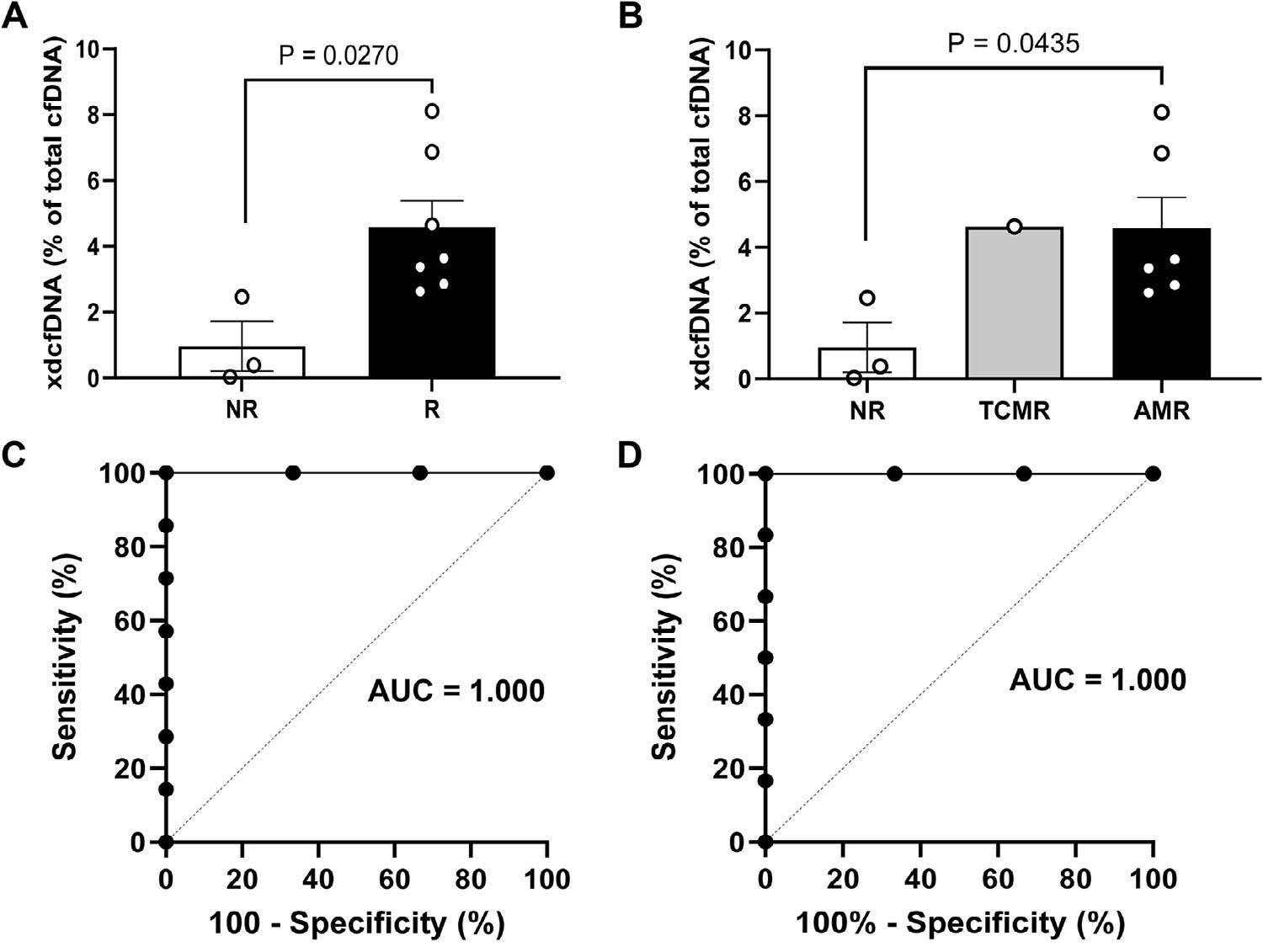
图3.移植后4周时,xd-cfDNA与排斥反应的关联
A. 排斥组与阴性组xd-cfDNA水平比较;B.TCMR组、AMR组与阴性组间xd-cfDNA水平比较;C. xd-cfDNA诊断排斥的ROC曲线;D.xd-cfDNA诊断AMR的ROC曲线。
03 与血管损伤密切关联
xd-cfDNA水平与Banff 2022病理评分体系中的血管病变(如血管内膜炎)以及肾小球毛细血管IgG沉积程度显著相关,表明其能特异性地反映抗体介导的血管内皮损伤。(图4)
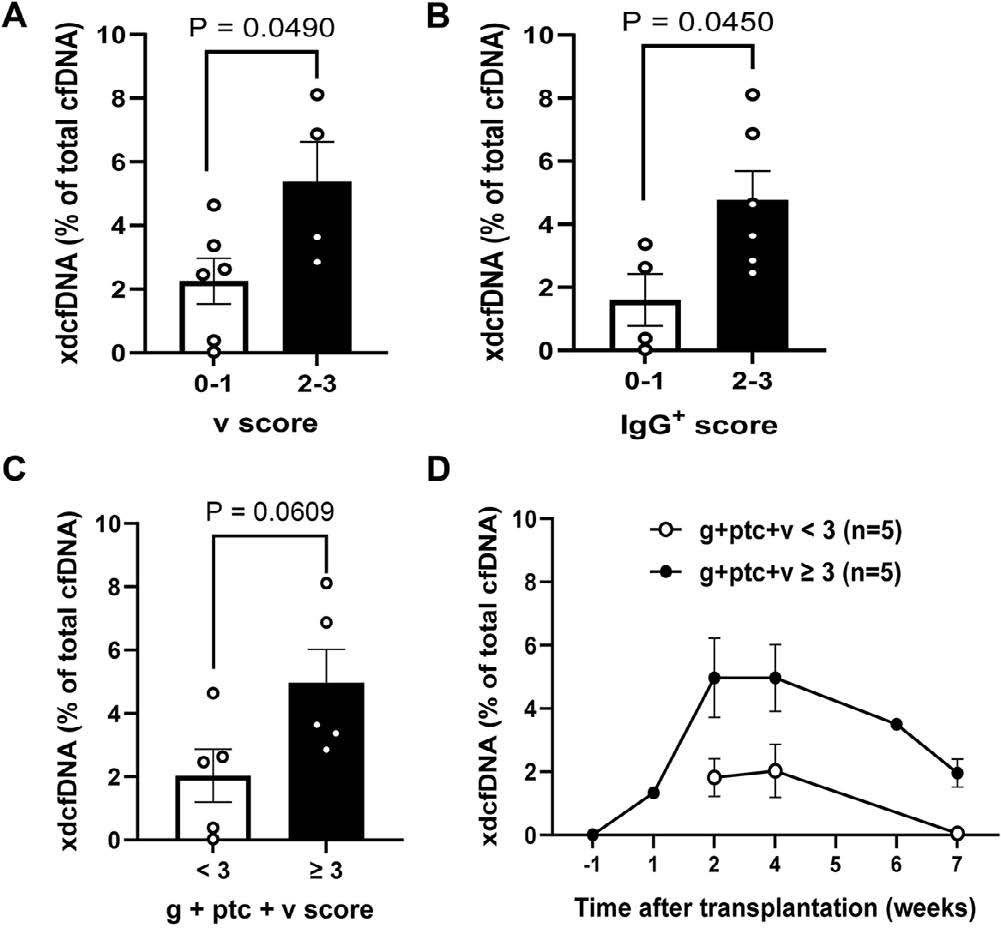
图4.xd-cfDNA水平与活检病理评分的关联
04 提示慢性损伤进程
在出现肾小管萎缩和间质纤维化等慢性损伤病理改变的组别中,xd-cfDNA水平也更高,提示其未来或有助于监测移植肾的慢性化损伤进程。(图5)
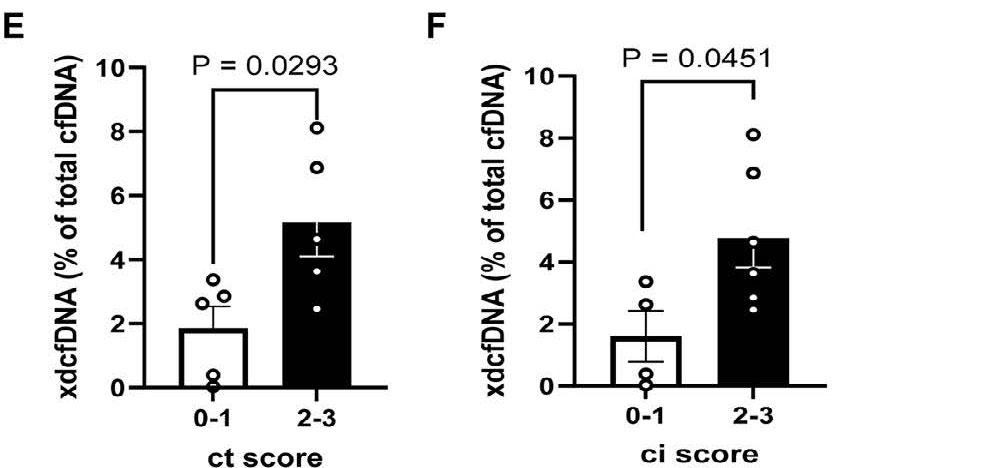
图5.xd-cfDNA在肾小管萎缩亚组与间质纤维化亚组的分别比较
总结
近年来,异种移植临床研究持续推进,但移植物长期存活仍面临挑战,排斥反应可能是影响长期存活的因素之一,如何早期发现排斥反应并调整免疫抑制方案成为异种移植领域研究热点之一。本研究利用猪肾来源的xd-cfDNA检测移植后的排斥反应,提示了xd-cfDNA作为异种移植排斥反应早期诊断生物标志物的巨大潜力。奥根诊断作为国内首个拥有dd-cfDNA自主知识产权并实现广泛临床应用的机构,在异种来源游离DNA(xd-cfDNA)检测方向也已建立具有自主知识产权的检测技术( 一种用于猪异种移植排斥反应监测的分子标志物和试剂盒,CN119552954A,2023年12月28日),能够精准定量异种移植术后的xd-cfDNA,期待能为异种移植临床研究提供有力工具。
参考来源:
Han K-H, et al. Xenograft-derived cell-free DNA as an early biomarker of rejection in genetically engineered pig-to-nonhuman primate kidney xenotransplantation.Xenotransplantation.2025;32:e70100.doi:10.1111/xen.70100
来源: 奥根诊断官网


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 移路相伴
移路相伴 