当我们谈论糖尿病时,往往想到血糖、胰岛素、饮食与运动。但在显微镜下,一个更早、更微妙的世界正在发生变化——肠道细菌与血液代谢物的动态失衡,早在血糖升高之前就已悄然启动。
复旦大学与哥德堡大学的研究团队在 Nature Medicine 发表的一项最新研究,历时近十年、覆盖 2027 名受试者,绘制出一张前所未有的 “菌群—代谢物—血糖控制” 三维动态图谱。研究揭示,糖尿病的代谢异动并非从胰腺开始,而是从微生物和分子层面蔓延开来。
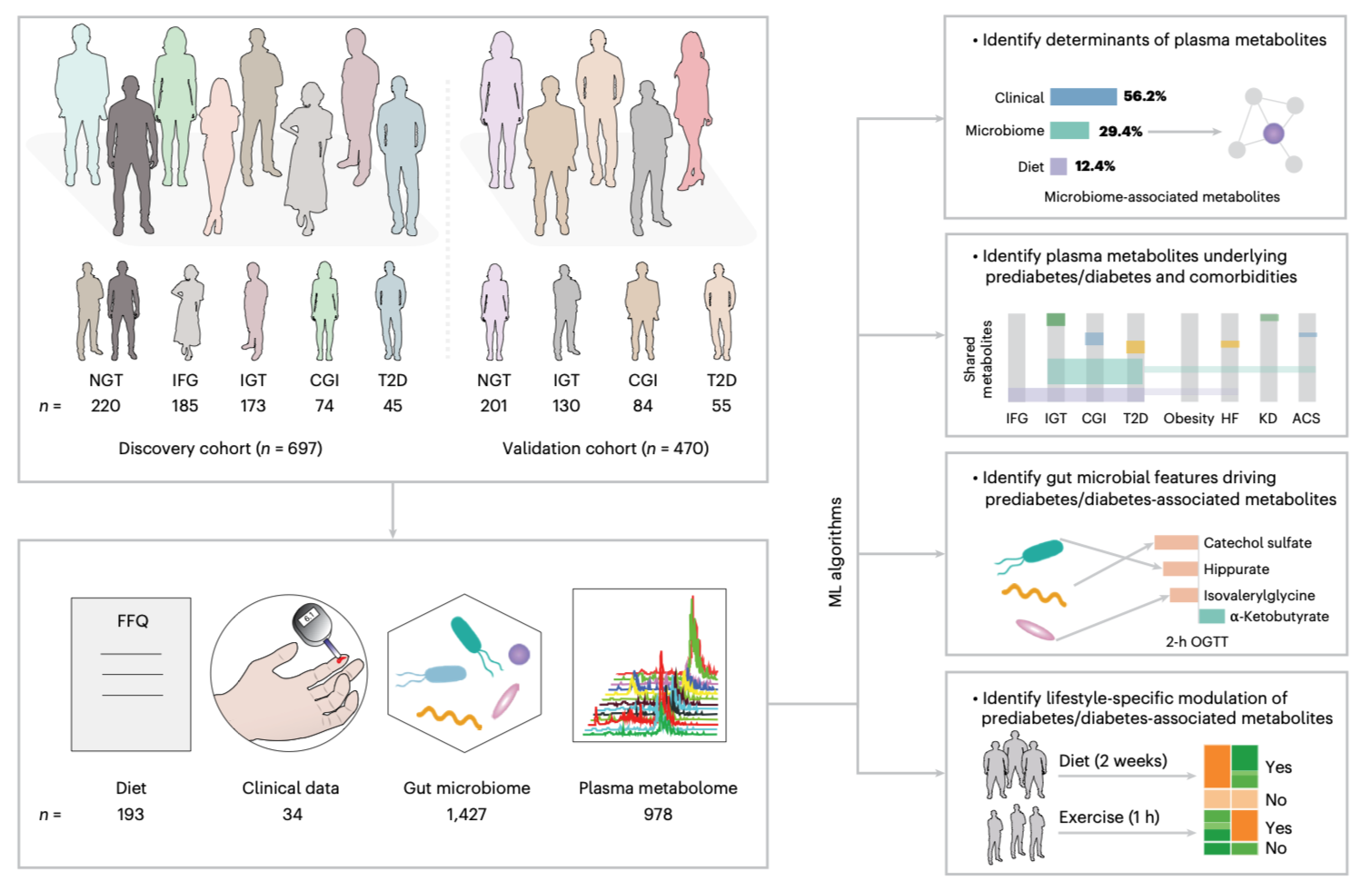
图1|肠道菌群、血液代谢物与血糖控制状态的综合分析框架
包括样本采集流程、菌群与代谢组整合分析及生活方式干预实验。
研究团队通过宏基因组测序与质谱代谢组分析,识别出 532 种血液代谢物 与血糖控制相关,其中约三分之一的变化可由肠道微生物解释。换言之,我们血液里那些微小的化学信号,有相当一部分来自肠道“同居者”。
更引人注目的是两种微生物的对抗关系。
一种是 Blautia wexlerae——健康人群中常见的丁酸生成菌,被认为具有抗炎与改善胰岛素敏感性的潜能;另一种是新近命名的 Hominifimenecus microfluidus,它的存在与高血糖、低代谢灵活性密切相关。研究发现,两者在代谢网络中呈强烈的负相关:前者减少时,后者几乎必然增多。而它们争夺的“信号分子”,正是一个看似平凡的代谢物——马尿酸(hippurate)。
马尿酸是肠道微生物分解芳香族化合物后与肝脏代谢相连的产物,在健康状态下能促进抗氧化与能量代谢。研究发现,B. wexlerae 的减少与血浆马尿酸水平下降呈强正相关,而 H. microfluidus 的增多则与其下降同步出现。换句话说,代谢异常或许不是“糖吃多了”的结果,而是“好菌没了,坏菌上位”的生理信号。
研究团队进一步利用多时间点样本追踪了这一动态变化——
从正常耐糖人群到糖耐量受损,再到糖尿病,马尿酸水平逐步下降,而 H. microfluidus 的丰度则持续上升。通过因果推断模型,他们确定这种菌群—代谢物组合不仅是“伴随变化”,而可能具有预警价值。
在这一宏观发现之下,研究者还揭示了令人鼓舞的事实——这些分子信号是可逆的。
在 6 个月的生活方式干预试验中(包括控制饮食、增加运动与睡眠优化),受试者的肠道微生物群和代谢组谱发生显著重塑。
特别是那些通过干预成功改善血糖控制的人,B. wexlerae 的丰度显著上升,而 H. microfluidus 明显下降,同时马尿酸和多种苯丙酸衍生物恢复至接近健康水平。
这些分子变化不仅是实验室数据的波动。
研究显示,在干预组中,肠道菌群与代谢物的恢复程度解释了血糖改善效应的约 41%。也就是说,运动和饮食并不是“直接降糖”,而是通过重新激活微生物代谢链路,恢复机体与肠道之间的化学对话。
为了更清晰地理解这一机制,研究者进一步进行了因果网络建模。结果显示,马尿酸通路位于整个网络的“中央节点”,连接着芳香酸代谢、氨基酸转运和能量生成三个关键模块。当这一节点受损,胰岛素信号传导与氧化还原平衡便被破坏;而生活方式改善能使该网络重新联通。
这项研究的意义远超“发现两种菌”。它让人们第一次看到,血糖控制背后是一场复杂的分子合奏:
菌群在肠道演奏,代谢物是乐谱,而生活方式是指挥。
当饮食不当、压力过高、睡眠紊乱时,指挥失去了节奏,乐团便走音,血糖曲线开始波动;而规律的生活习惯,则让这支微生物乐团重新回到和谐的节拍。
作者在论文最后写道:“肠道菌群与代谢物不仅反映了代谢状态,更是生活方式干预的作用载体。”
这句话或许是对糖尿病研究方向最深刻的提示。未来的“生活方式治疗”将不再只是卡路里的计算,而是一场微生物生态的修复工程——
当我们重新喂养那些被现代生活饿坏的好菌,健康的化学旋律,也许就会重新奏响。
参考文献
Wu H, Wu Y, Sun X, et al.
Microbiome–metabolome dynamics associated with impaired glucose control and responses to lifestyle changes.
Nature Medicine. 2025. doi:10.1038/s41591-025-03642-6
来源: 合康谱精准医学科普基地


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 合康谱精准医学科普基地
合康谱精准医学科普基地 
