过去十年里,几乎所有关于自闭症肠道菌群的研究都聚焦在“细菌”层面。然而,肠道生态并非单一王国——它还包括真菌、病毒、古菌和原生生物等“多界微生物”。2024 年发表在 Nature Microbiology 的一项研究,用前所未有的规模描绘出这张复杂的生态图谱,揭示出自闭症谱系障碍(ASD)儿童体内隐藏的多界微生物密码。
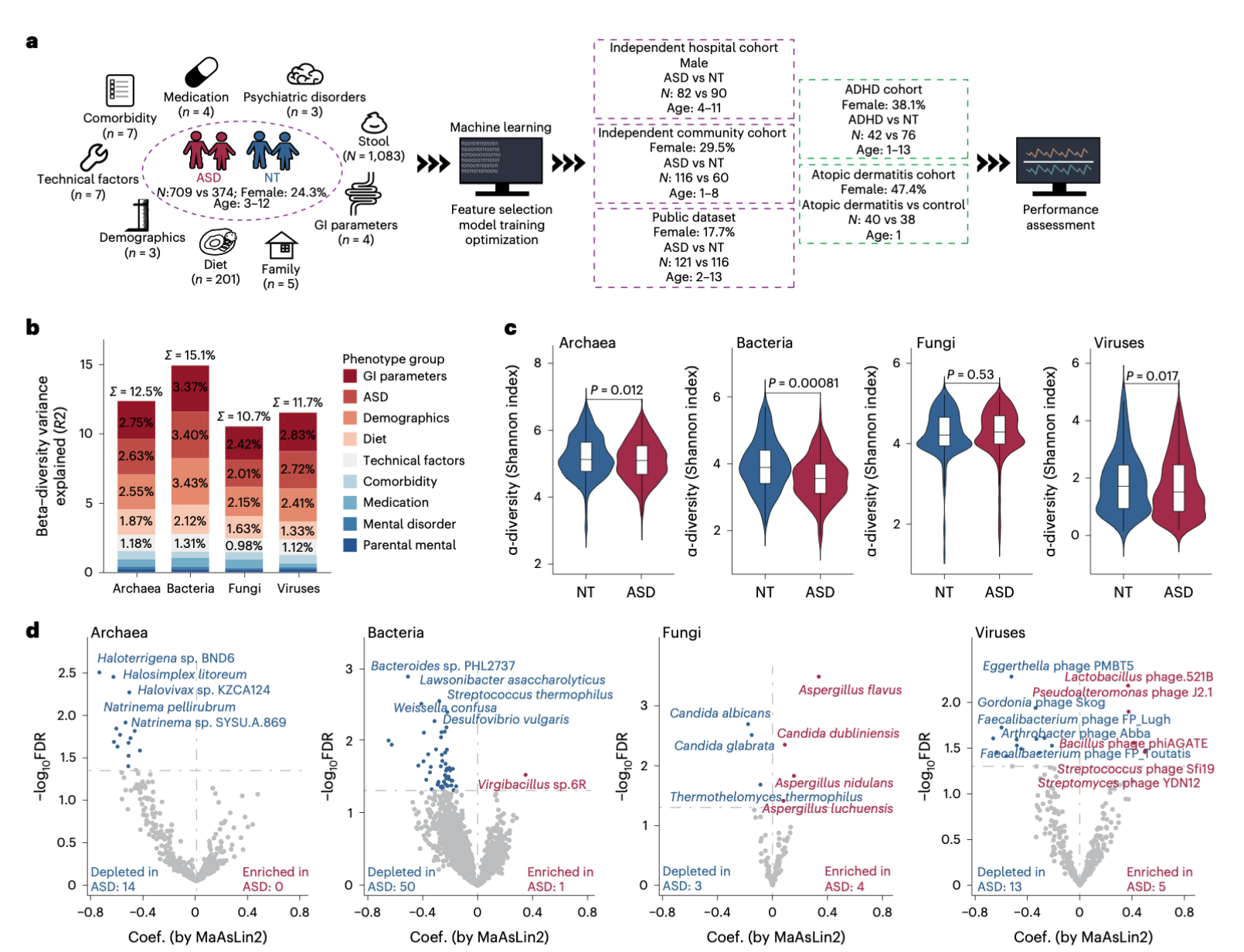
图1|研究设计与样本分布。研究涵盖1,600名儿童,利用多界宏基因组测序描绘自闭症的微生物生态特征。
研究团队整合了来自七个国家、超过1,600名儿童的多中心粪便样本,涵盖自闭症、发育迟缓以及典型发育组。不同于以往只研究“菌群多样性”的方法,他们同时分析了细菌、真菌、病毒和古菌的基因组信息,形成了首个“多界微生物组”(multikingdom microbiome)数据库。这种跨界整合让研究者第一次能观察到——不仅细菌在变化,整个肠道生态系统都在以协调的方式“走向失衡”。
结果显示,ASD 儿童肠道中存在显著的多界紊乱模式:
●细菌层面:产短链脂肪酸的 Faecalibacterium 和 Roseburia 明显减少,而潜在致炎菌 Escherichia 增多;
●真菌层面:酵母样真菌 Candida 丰度升高,与炎症反应和免疫激活相关;
●病毒层面:噬菌体多样性下降,提示细菌生态的调控网络受损。
这种协同的“多界漂移”,构成了自闭症特有的微生物印记。
为了进一步探明这些变化是否具有生物学意义,研究者构建了一个整合机器学习模型,通过 500 多个多界功能特征进行训练。结果表明,仅依靠微生物的代谢通路特征,模型即可实现超过 85% 的自闭症识别准确率。最具代表性的功能变化包括:GABA 代谢下降、短链脂肪酸生成减弱、硫代谢增强——这些正是影响神经发育与免疫稳态的关键通路。
更令人关注的是,这些变化不仅局限于细菌。研究者发现某些真菌与噬菌体可通过代谢互作放大这些信号。例如 Candida albicans 促进乳酸积累,从而抑制丁酸菌生长;噬菌体感染则削弱宿主细菌的 GABA 生成通路。换句话说,肠道的“跨界通信故障”或许正是行为改变的生态底色。
这项研究的价值不仅在于发现新的微生物群,更在于提供了一个多界整合的视角。长期以来,我们试图用单一细菌或益生菌来解释行为和神经发育,但这项研究提醒我们:自闭症可能是一场生态系统级的失衡。未来的诊断与干预,也许要从“重建多界平衡”入手,而非仅补充某一类菌株。
从某种意义上说,这是一场关于沟通的研究——不仅是孩子与世界的沟通,也是不同生命界之间的沟通。当这些微观的语言断裂,大脑的语言或许也随之变得模糊。
参考文献
Wang Y, et al. Multikingdom and functional gut microbiota markers for autism spectrum disorder. Nature Microbiology. 2024;10(4):712–726. doi:10.1038/s41564-024-01739-1.
来源: Nature Microbiology


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 合康谱精准医学科普基地
合康谱精准医学科普基地 