在健康话题中,间歇性禁食(intermittent fasting, IF)已成为热词。
人们惊讶于它能改善血糖、减脂、延寿,却少有人追问:为什么“吃与不吃”的节律本身,也是一种代谢信号?
2025年发表在 eBioMedicine 的研究揭示了一个更深层的机制——间歇性禁食和饮食转换共同重建了“肠道菌群–短链脂肪酸(SCFA)–代谢节律”的回路。
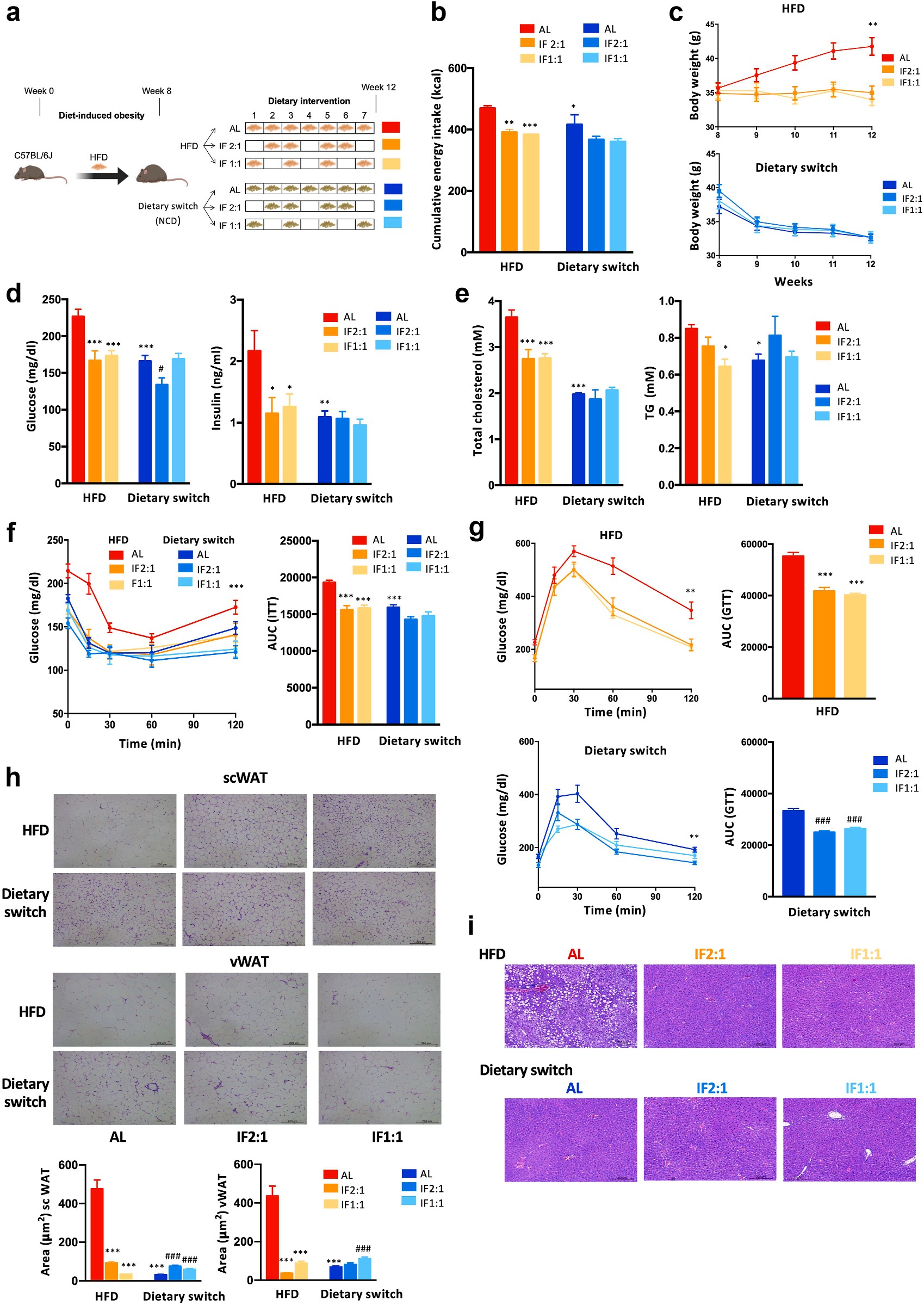
图1|研究设计:不同禁食节律与饮食转换的组合干预。
研究团队在肥胖小鼠中设置了多组对照:
●正常饮食组(ND);
●高脂饮食组(HFD);
●饮食转换组(HFD→ND);
●间歇性禁食组(IF 1:1 与 IF 2:1);
●联合干预组(HFD→ND + IF)。
实验持续 12 周,重点测定了体重、血糖、血脂、胰岛素敏感性,以及粪便与血液中的短链脂肪酸(SCFA)浓度。
结果令人惊讶:即便体重不变,间歇性禁食也能显著改善葡萄糖耐量与脂质代谢。
单独的饮食转换能降低脂肪堆积,而禁食则重建了肠道微生态的昼夜节律——两者联合时效果最强。
特别值得注意的是,研究者发现了一种关键现象:
健康小鼠的短链脂肪酸呈现明显的“进食后高峰”,而肥胖小鼠这一节律消失;禁食或饮食转换可使其恢复。
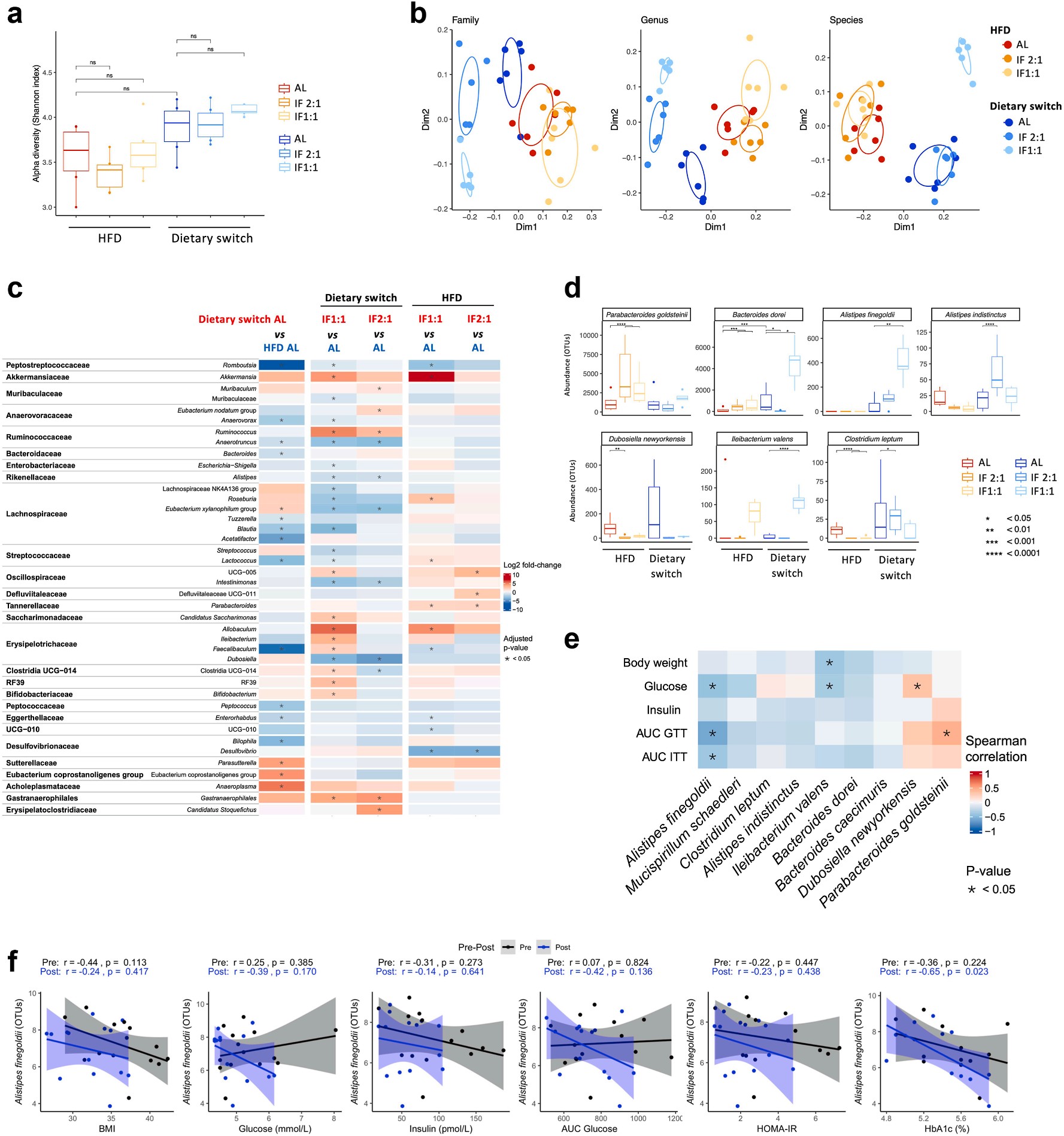
图2|间歇性禁食恢复了餐后短链脂肪酸(SCFA)波动的节律。
这意味着,SCFA 生成不仅取决于“吃什么”,还取决于“何时吃”。
在健康状态下,肠道菌群与宿主的代谢信号保持同步,进食后产酸菌活跃、能量利用高效;
而肥胖状态下,这一“代谢拍点”失调,肠菌活动与宿主信号脱节。
间歇性禁食像是“重新校准了钟表”,让微生物代谢与身体节律重新对齐。
进一步的 16S rRNA 与代谢组分析揭示了关键菌种:
一种名为 Alistipes finegoldii 的菌在禁食组显著富集。
它与粪便丁酸、丙酸水平呈正相关,也与胰岛素敏感性改善高度一致。
功能注释显示,它能参与氨基酸代谢与丙酸合成途径,可能是连接“禁食–菌群–代谢”链条的核心节点。
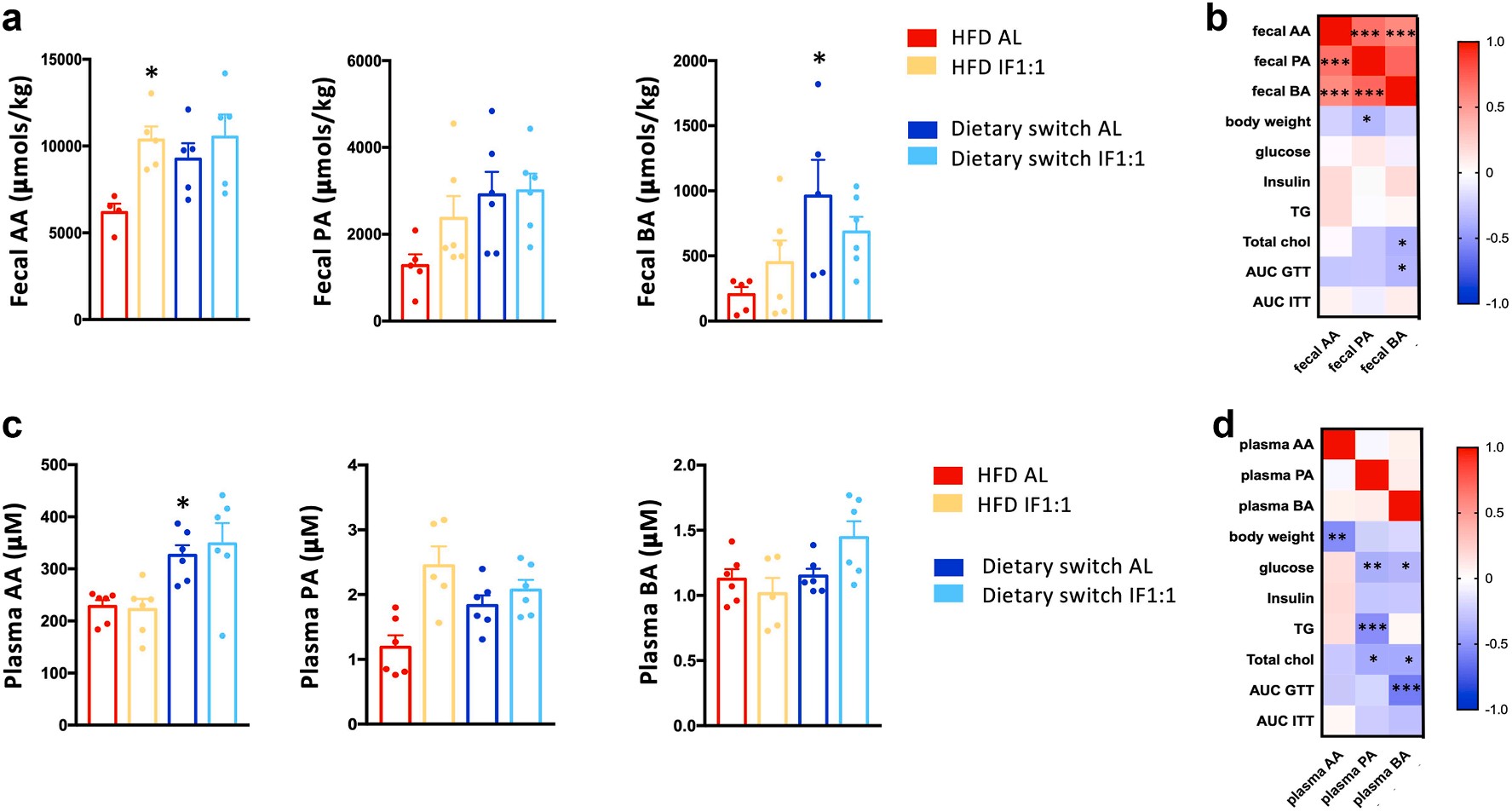
图3|禁食促进 Alistipes finegoldii 富集,并增强丁酸/丙酸通路。
值得一提的是,研究者通过时序采样还发现:
SCFA 的动态变化比绝对含量更能反映代谢健康。
在代谢稳定的小鼠中,丁酸与丙酸在进食后数小时升高、禁食后下降,呈现出“呼吸式节奏”;
而代谢紊乱组中,这一波动被削平,显示出“代谢疲劳”的状态。
这种“SCFA 节律指数”未来或许能成为代谢健康的新型生物标志。
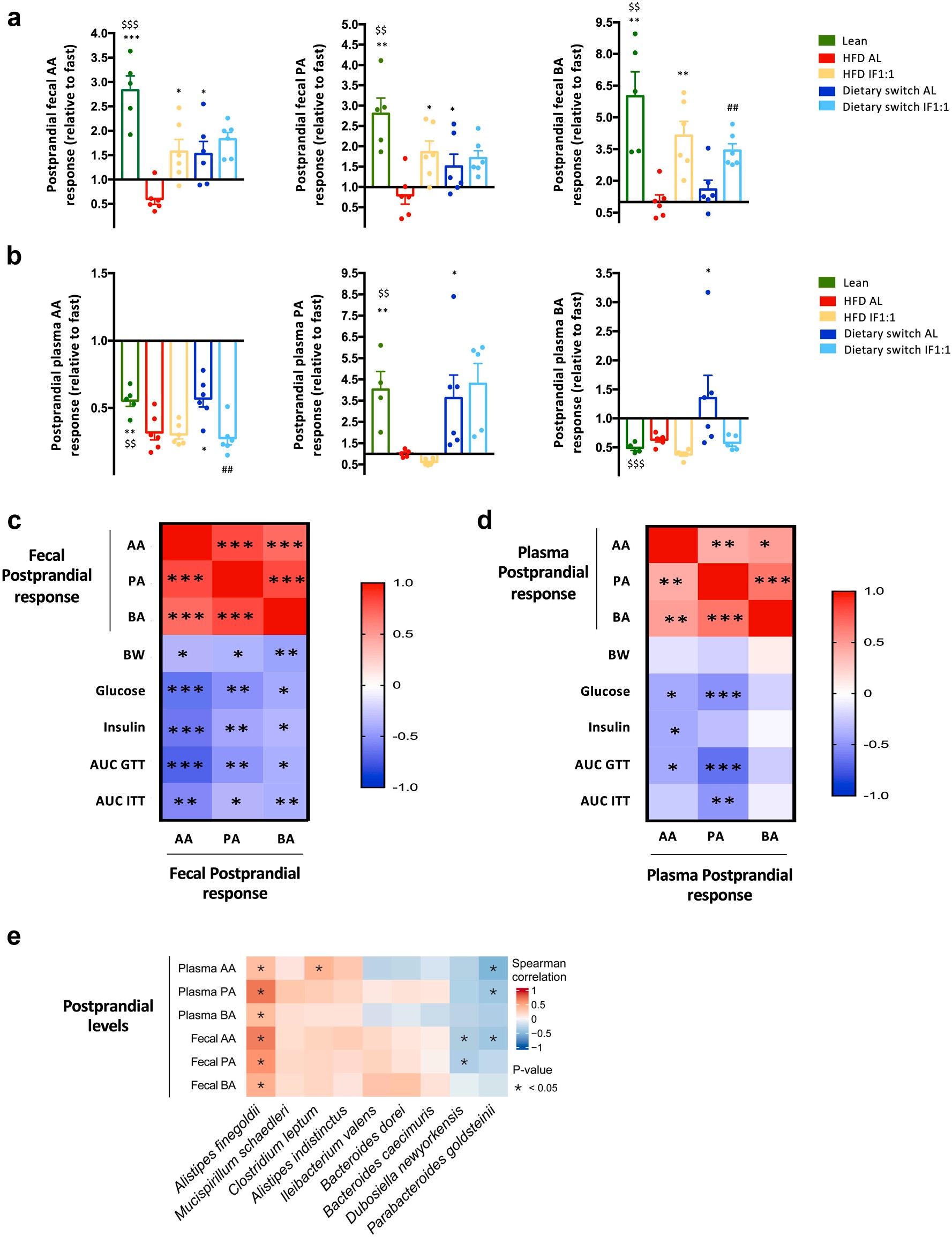
图4:瘦型和肥胖小鼠以及饮食干预后的短链脂肪酸餐后反应。
总体来看,这项研究提出了一个新的代谢模型:
●饮食转换 提供“原料修正”,重塑菌群组成;
●间歇性禁食 提供“时间信号”,重建菌群功能节律;
●两者结合,使肠道菌群重新形成代谢共振,从而改善系统性代谢稳态。
结语
肠道菌群不仅在“吃什么”时发挥作用,更在“什么时候吃”中维持节奏。
间歇性禁食之所以有效,不只是因为减少热量,而是让微生物与宿主重新“合拍”。
未来的营养干预,或许会像音乐一样,需要找到正确的节奏——那就是“肠道的代谢拍点”。
参考文献
Liu Y, Zhang H, et al. Dietary switch and intermittent fasting reshape gut microbiota rhythms and short-chain fatty acid metabolism in obesity. eBioMedicine. 2025;103:105632. doi:10.1016/j.ebiom.2025.105632.
本文所用图片均为文献内Figure
来源: 合康谱精准医学科普基地


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 合康谱精准医学科普基地
合康谱精准医学科普基地 
