出品:科普中国
作者:吕泽龙(中国科学院动物研究所)
监制:中国科普博览
2025年5月,一头体重26公斤的克隆犏牛犊于在西藏自治区拉萨市曲水县实验站顺利降生。这是全球首例体细胞克隆犏牛,标志着我国在高原家畜克隆领域迈入世界领先行列。就在今年,我国还成功培育生产了一头体细胞克隆的延边牛及牦牛。这三种牛分别代表了优良肉牛(延边牛)、杂交优势品种(犏牛)和高原良种牛(牦牛)。这一系列成果背后的技术就是体细胞克隆。

出生后两个月的体细胞克隆犏牛
(图片来源:中国农业科学院北京畜牧兽医研究所)

克隆延边牛
(图片来源:中国新闻网)
自从1996年体细胞克隆的绵羊多莉诞生之后,越来越多的动物被成功克隆——从2001年中国克隆的渤海黑牛品系“康康”诞生,再到之后的普通猕猴、黑足鼬、北极狼以及警犬,甚至是已灭绝的比利牛斯山羊。克隆技术正在悄然地改变着动物保护和育种的未来。

北极狼。克隆的北极狼(原名玛雅)本体出生于2005年,卒于2021年,其克隆个体“玛雅”随后诞生;2022年秋天,另一只克隆北极狼“哈尔”在江苏省出生。图片中的北极狼并非克隆个体。
(图片来源:作者拍摄于北京野生动物园)
那么,什么是克隆技术?为什么要克隆动物呢?这看似简单的两个问题背后,却蕴含着生物科技发展的重大意义。让我们从科学原理到实际应用,来一探这项神奇技术的究竟。
克隆及其操作过程
要理解克隆技术,我们得先回到1996年。那一年,一只叫“多莉”的绵羊诞生,她是世界上第一只用体细胞克隆技术成功培育出的哺乳动物。曾经引起过全世界的关注,其案例还出现在了诸多教科书中。
哺乳动物体细胞克隆的过程简单来说,就是把一只动物的体细胞(例如皮肤细胞)的细胞核,植入到另一只去除了卵细胞的细胞核里面,形成一个人工授精的胚胎。再将这个胚胎移植到受孕母体里发育成长。出生的个体,与提供细胞核的原型动物在细胞核基因上几乎一模一样。
注解:上文提到的“把动物体细胞的细胞核植入是卵细胞内”有两种方式,第一种是直接取出体细胞细胞核(用微型注射针),然后注入卵细胞里面。第二种是让整个供体细胞在电脉冲等方式下和卵细胞融合。克隆羊多莉使用的是后者。
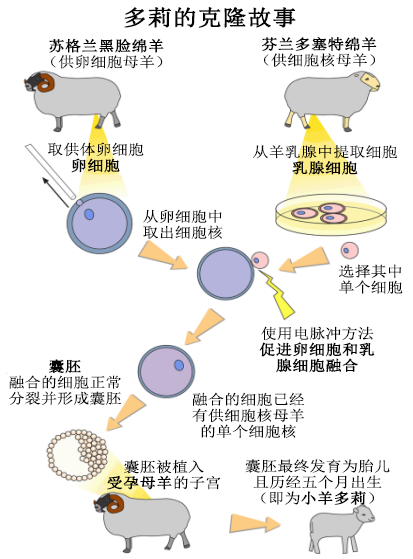
绵羊多莉克隆图
(图片来源:Ask a Biologist)
如今,这个方法已经成功应用于多种哺乳动物,如黄牛、狼、家猫,甚至猕猴。那其他的动物呢?其实在20世纪下半叶,克隆的鱼类和无尾目就已经诞生——虽然它们没有子宫,但是它们的胚胎可以在水体内自己发育。1962年,英国的戈登就已经把蛙类克隆成功。

蛙克隆过程,和克隆羊多莉过程相对类似。不过有些不一样的是,它是直接把体细胞细胞核植入卵细胞里面,而非让体细胞和卵细胞进行细胞融合
(图片来源:Brainly)
但克隆鸟类就很困难了——因为克隆技术涉及到对卵细胞的操作,而鸟类的卵黄太大,结构复杂,不像哺乳动物那样容易处理。以鸡蛋为例,我们常吃的鸡蛋不少是鸡产下来的未受精卵(也有受精卵)。相比之下,没有太多卵黄和卵壳保护的蛙类卵就很好操作了。而且,鸟类也没有子宫,无法像哺乳动物一样通过子宫孕育胚胎,这使得胚胎移植几乎无从谈起。
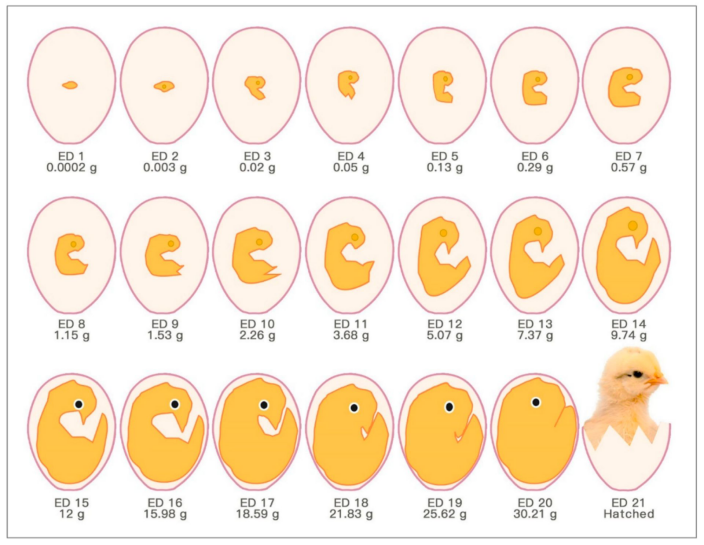
鸡胚胎在蛋里面发育
(图片来源:ar.inspiredpencil)
所以,鸟类真的不能被克隆吗?有些科学家选用了另一种方式——不是复制整个细胞,而是将珍稀鸟类的原始生殖细胞(如精原细胞或卵原细胞)转移到一只普通家禽体内。例如,把绿孔雀的精原细胞移植至家鸡的睾丸里,让家鸡代为生成孔雀的精子。这种方法虽然还在实验阶段,但已经在不同品种鸡之间成功实现了间接克隆。

绿孔雀(非克隆个体)
(图片来源:作者拍摄于北京动物园)
例如,扬州大学的团队把黑色羽毛的狼山鸡的体细胞(准确来说是鸡身上的成纤维细胞)“诱导”逆转为原始生殖细胞。然后,将其移植到了白洛克鸡品系的体内负责受孕,生下了狼山鸡。

狼山鸡品系
(图片来源:The Livestock Conservancy)
克隆技术目前的局限性及破解方法
不过想要克隆动物,也面临着不少技术操作和科学伦理的问题。除了上文提到的鸟类克隆面临着生殖细胞操作的问题以外,也有人发现,部分物种的克隆并不是我们要做的那么简单。
比利牛斯山羊(属于西班牙山羊Capra pyrenaica的亚种)在灭绝之后被克隆了。2000年,它们被宣告灭绝,但好消息是,科学家们保留住了部分个体的冷冻细胞样本,这就是它们复活的希望。
2003年,研究人员尝试利用这些冷冻保存的细胞进行克隆。他们将山羊细胞的细胞核植入了家山羊的卵细胞中,并把实验中培育出的208个胚胎移植到57只受孕母羊体内(受孕的个体有西班牙山羊的其他亚种)。结果显示,仅有7只成功妊娠,但其中6只羊在孕期中途发生胚胎流产。最后,仅有1只比利牛斯山羊出生,然而该幼羊刚出生没多久就因为肺部先天畸形而死。
由于重新克隆的比利牛斯山羊早逝,比利牛斯山羊也成了为数不多的灭绝两次的动物。这次实验是人类首次尝试用克隆技术“复活”已经灭绝的哺乳动物,虽然以失败告终,却也揭示了一个现实:哪怕掌握了克隆技术,想要真正让灭绝动物重返世界,依然困难重重。

比利牛斯山羊
(图片来源:维基百科)
从中,我们也不难看出,一些动物克隆时可能存在胚胎流产或者克隆胚胎无法受孕的情况。并且,如果使用了近缘物种的卵细胞,可能会导致新克隆出来的动物掺杂了其他动物的细胞质基因(卵细胞的细胞质也有基因,线粒体基因就是例子),造成基因混杂。正是由于克隆涉及的技术繁杂以及存在受孕失败风险,使得在拯救濒危物种的实践中,传统的交配繁殖、种群交换和个体转移往往更高效。

一只克隆猫咪
(图片来源:Britannica)
值得注意的是,即便对于一些数量正常的家畜,克隆技术也面临特殊挑战。以犬类为例:其卵母细胞对于外界刺激相对敏感,如果要进行去除和植入细胞核的显微操作,可能会导致卵母细胞的“意外去世”。犬类卵细胞细胞质的脂肪也会影响原有细胞核的移除。另外,犬类每年的排卵次数也不多,且不能通过激素干预。
正是因为如此,克隆部分物种的推广普及还在发展之中,而对于繁殖饲养技术相对匮乏的濒危物种,那就更难一些。
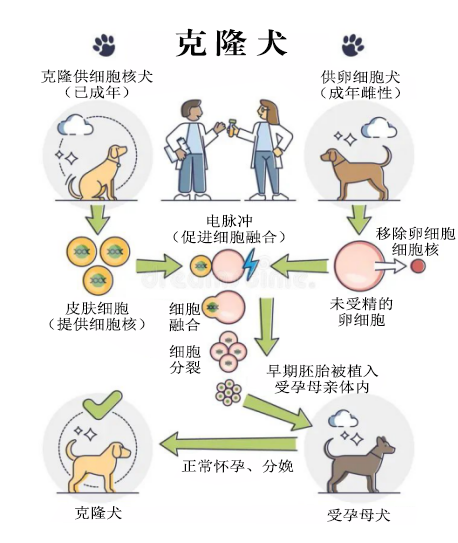
克隆犬类过程。过程看似简单,但是右侧去除卵细胞细胞核部分曾一度困扰人。
(图片来源:Dreamstime)
纵然克隆技术存在诸多挑战,但也有人选择开始克隆身边的警犬,敢为人先,不过培育警犬也存在一定失败率。通过克隆训练有素的好警犬或者其他工作犬,或许可以得到更多和原犬一样具备优秀训练潜质的个体。韩国曾克隆过优秀的工作犬。

左侧为首个克隆犬(来自韩国),右侧是的它受孕母亲。
(图片来源:参考文献[9])
而在中国的2018年冬天,昆勋这条克隆的昆明狼犬诞生。不过,要使其性格和工作能力和原犬一样,还需要警察同志的后天培养教育。北京等地也有克隆警犬来自于功勋的警犬细胞。

克隆的昆勋
(图片来源:文汇报)
您可能还会好奇:前文提到犬类卵细胞操作困难,这一问题如何解决?青岛农业大学赵明辉博士开发出AI辅助显微操作系统——用AI帮助识别和预测卵细胞中细胞核的位置,辅助取出细胞核。

AI辅助去核克隆犬
(图片来源:青岛农业大学)
在一些珍稀黄牛品系保护方面,克隆技术同样展现出显著价值——西藏地区数目不足百只的樟木牛和阿沛甲咂牛都是典型的例子,它们就曾在2024年初被克隆。之前创造了克隆牛“康康”的教授夫妇,还助推了肉牛胚胎移植产业化的可能性。

克隆的珍贵黄牛品系
(图片来源:新华社)
此外,关于克隆动物的常见误解需要澄清——很多人错误地认为“克隆的动物可能没法自己繁殖,寿命短”,这一观点其实不太对。2017年相应的科学研究表明,多莉这只克隆绵羊因为关节炎没活到预期寿命,背后的原因并不是因为克隆。还有克隆牛康康和双双也在繁殖能力上没有什么问题(人工授精已经成功了)。日本也有体细胞克隆牛寿终正寝。
克隆是因为生育障碍吗?为啥不能生?
克隆的动物确实很多,那为什么要克隆它们呢?可能是要增加它们的数目,也可能是——被克隆的动物压根无法繁殖。
没错,本次克隆的犏牛就是一个例子:公犏牛不育,只有母犏牛可育。2003年还诞生过克隆的骡子,然而,不论公母骡子都基本无法生育。此外,雄狮和雌虎生下来的狮虎兽也是雄性不育而雌性可育。为什么会这样呢?

狮子狮虎兽(狮子和雌性狮虎兽杂交后代)
(图片来源:Ligerworld官网)

犏牛
(图片来源:ar.inspiredpencil)
这种现象背后的科学原理与亲本物种的分化时间密切相关。以骡子为例(通常指母马和公驴杂交所生的马骡,若杂交亲本反过来——母亲是驴,父亲是马,产生的后代则称之为驴骡,其体型和力气比起骡子小),它们的父母——家马和家驴的物种分化时间比起黄牛牦牛(也就是犏牛父母)的分化时间长。不过也有极少数例外:曾有母骡子和公驴或公马交配成功繁殖的报道。

克隆骡子
(图片来源:参考文献[8])
更深层的原因还涉及到兽类的性染色体。我们哺乳动物多是雄性XY两个不一样的性染色体,而雌性则是XX两条一样的染色体。而X染色体是有自己基因拷贝的,这样一来,雌性有“两份”X染色体基因拷贝和表达量,但是雄性只有一份基因拷贝,理论上表达量就会下降,影响雄性个体生存。
为了解决这个问题,就需要“剂量补偿效应”提升雄性的X染色体相应基因表达的“产量”。而产量需要顺式调控元件和反式调控因子来进行,前者来自X染色体,后者在性染色体以外的其他染色体上面。这个因子和原件用来做什么?顺式调控元件像是一个“智能水龙头”。而反式调控因子则是可调节水龙头的智能设备,“智能设备”也就只能识别和调节特定的水龙头——这就意味着不同物种间的设备和水龙头就有区别。
当性染色体调控系统在雄性狮虎兽身上出现识别失败时,问题就变得尤为棘手。由于雄性的狮虎兽同时继承了狮子和老虎染色体上面的“智能设备”,还有老虎X染色体的“水龙头”,但却没有狮子X染色体上面的“水龙头”。最后由于“水龙头”数目太少,而设备的调节又非常混乱识别失败,可直接导致基因表达失调——或者过多或者过少。特别值得注意的是,受影响最严重的恰恰是控制雄性生殖系统发育的关键基因,这正是导致雄性狮虎兽不育的根本原因。

海南岛某动物园的狮虎狮兽(狮子和雌性虎狮兽的杂交后代,这只狮虎狮兽的“姥爷”“姥姥”分别是雄虎和雌狮)。
(图片来源:messybeast官网)

雌性狮虎兽和公老虎生的“虎狮虎兽”
(图片来源:messybeast官网)
相比之下,如果是雌性狮虎兽,父亲狮子和母亲老虎的“水龙头”和“智能设备”都是一半一半。这样一来,虽然父亲的X染色体上面的“水龙头”和母亲的“智能设备”放一起会有点问题(反之也有),但由于雌性狮虎兽有两个X染色体,因此其基因表达错误会在一定程度上缓冲跨物种调控系统的兼容性问题,使其生殖功能受到的干扰相对雄性显著减轻。

雌性狮虎兽
(图片来源:Ligerworld官网)
在性染色体决定性别方面,还存在着与哺乳动物XY系统截然不同的ZW模式——这一系统广泛存在于部分两栖动物、蜥蜴、蛇类、鳞翅目昆虫、鱼和鸟类中。其中,ZW为雌性,ZZ两个一样染色体的则是雄性。这种机制导致了一个有趣的现象:两种有生殖隔离的鸟杂交出来的后代往往是雌性不育而雄性可育。那就是因为Z染色体承载着“水龙头”(顺式调控元件),而杂交的雌性鸟只有父方来的“水龙头”,而父母双方的“智能设备”(反式调控因子)直接会把它的相关基因“调节混乱”。

科莫多巨蜥,染色体类型为ZW。
(图片来源:作者拍摄于上海动物园)
说回到刚刚不能繁殖的犏牛,由于体内基因的“水龙头”和“设备调解失败”的原因,出现了产生精子的问题。
中学时代的生物有提及,产生精子需要减数分裂,而减数分裂需要精原细胞来进行,精原细胞会先分裂增加数量并演变为初级精母细胞,初级精母细胞经过二次减数分裂形成精细胞,精细胞再度变形成为蝌蚪状的精子。
犏牛自己却出现了精原细胞的形成问题,而精原细胞变作初级精母细胞的数目,也比同龄正常繁殖的牦牛少。此外,它们的减数分裂还被阻断了:减数分裂中所需要的一些蛋白质,例如CDK1和SETX等参与了细胞分裂等生命活动的蛋白,可以在牦牛的精母细胞里面找到,但在犏牛中却找不到。缺少这些必需的蛋白,犏牛自然出现了繁殖困难问题。面对这样的情况,克隆技术为保存犏牛这一兼具产奶与产肉价值的特殊畜种提供了全新思路。
从克隆牛到杂交不育机制,这些研究不仅揭示了生殖生物学的精妙复杂,更展现了现代生物技术在保护优良畜种、工作犬和濒危物种方面的巨大潜力。于此,也希望克隆技术能在更多的动物中得到应用。随着技术不断进步,我们有理由期待克隆技术能为生物多样性保护开辟更广阔的道路。
参考文献:
[1]Payseur BA, Presgraves DC, Filatov DA. Introduction: Sex chromosomes and speciation. Mol Ecol. 2018;27(19):3745-3748.
[2]Johnson NA, Lachance J. The genetics of sex chromosomes: evolution and implications for hybrid incompatibility. Ann N Y Acad Sci. 2012;1256:E1-E22.
[3]Lenormand T, Roze D, A single theory for the evolution of sex chromosomes and the two rules of speciation.Science,2025;389(6756): eado9032
[4]Wu SX, Wan RD, Wang GW, Zhang YW, Yang QE. Comparative proteomic analysis identifies differentially expressed proteins associated with meiotic arrest in cattle-yak hybrids. Proteomics. 2023;23(12):e2300107.
[5]Wu SX, Wang GW, Fang YG, Chen YW, Jin YY, Liu XT, Jia DX, Yang QE. Transcriptome analysis reveals dysregulated gene expression networks in Sertoli cells of cattle-yak hybrids,Theriogenology,2023;23:33-42.
[6]Zhao R, Zuo Q, Yuan X, et al. Production of viable chicken by allogeneic transplantation of primordial germ cells induced from somatic cells [retracted in: Nat Commun. 2023 Jun 19;14(1):3625. doi: 10.1038/s41467-023-39170-5.]. Nat Commun. 2021;12(1):2989.
[7]Korody ML, Ford SM, Nguyen TD, et al. Rewinding Extinction in the Northern White Rhinoceros: Genetically Diverse Induced Pluripotent Stem Cell Bank for Genetic Rescue. Stem Cells Dev. 2021;30(4):177-189.
[8]Woods GL, White KL, Vanderwall DK, et al. A mule cloned from fetal cells by nuclear transfer. Science. 2003;301(5636):1063.
[9]Lee BC, Kim MK, Jang G, et al. Dogs cloned from adult somatic cells. Nature. 2005;436(7051):641.
[10]Kim MJ, Oh HJ, Kim GA, et al. Birth of clones of the world's first cloned dog. Sci Rep. 2017;7(1):15235.
[11]Wu S, Mipam T, Xu C, Zhao W, Shah MA, Yi C, et al. Testis transcriptome profiling identified genes involved in spermatogenic arrest of cattleyak. PLoS ONE.2020; 15(2): e0229503.
[12]Schaetzlein S, Lucas-Hahn A, Lemme E, et al. Telomere length is reset during early mammalian embryogenesis. Proc Natl Acad Sci U S A. 2004;101(21):8034-8038.
[13] Folch J, Cocero MJ, Chesné P, et al. First birth of an animal from an extinct subspecies (Capra pyrenaica pyrenaica) by cloning. Theriogenology. 2009;71(6):1026-1034.
[14] Corr SA, Gardner DS, Langley-Hobbs S, Ness MG, Kitchener AC, Sinclair KD. Radiographic assessment of the skeletons of Dolly and other clones finds no abnormal osteoarthritis. Sci Rep. 2017;7(1):15685.
[15] Tian XC, Kubota C, Enright B, Yang X. Cloning animals by somatic cell nuclear transfer--biological factors. Reprod Biol Endocrinol. 2003;1:98.

来源: 中国科普博览
内容资源由项目单位提供


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 中国科普博览
中国科普博览 
