导读
近日,英国布里斯托尔大学Varinder K. Aggarwal与Adam Noble课题组报道了一类兼具稳定性与高还原活性的硼基-联吡啶自由基,其可通过联吡啶与二硼试剂简单混合生成。研究发现,这类自由基的激发态还原电势超越迄今报道的最强光还原剂。此外,此类双线态光氧化还原催化剂可以促进烷基溴化物的硼基化及多种其他转化反应。
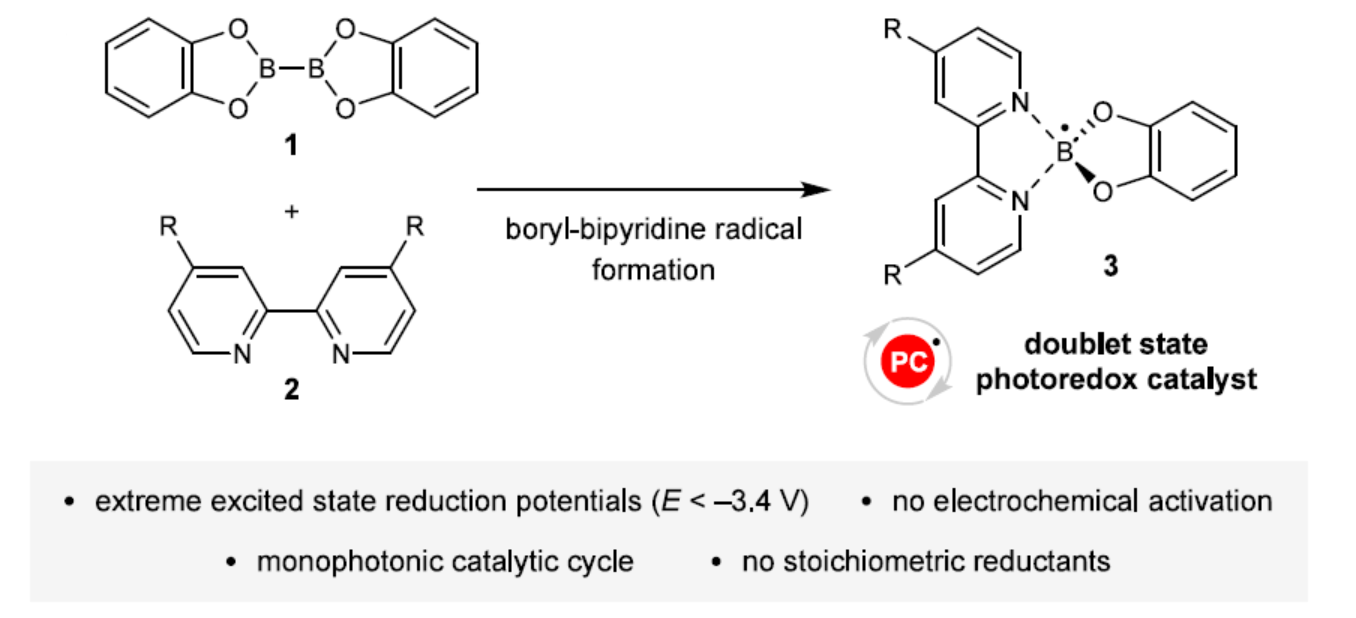
(图片来源:J. Am. Chem. Soc.)
正文
自由基化学的研究主要集中于高活性有机自由基的反应,此类物种通常仅作为瞬态中间体存在。然而,当自由基具备足够的空间位阻效应或电子稳定性时,其反应活性可显著减弱,从而能够长期稳定存在。早在1900年,Gomberg团队在合成三苯甲基自由基时,首次发现了这一现象。此后,多种具有持久性且稳定(对氧气呈惰性)的自由基陆续被报道(Figure 1a)。这些自由基的长寿命特性引发了学术界对其独特性质的显著关注,其作为试剂或催化剂应用于有机合成领域则相对罕见,但通常用作氧化反应催化剂的氨基氧(aminoxyl)自由基(如TEMPO)除外。在过去的十年里,光氧化还原催化已成为有机合成中用于产生瞬态自由基的主要方法。在激发态下,光氧化还原催化剂与多种底物发生单电子转移(SET),这些反应的成功很大程度上取决于催化剂是否具有足够高的氧化还原电位以实现热力学有利的SET。因此,对于氧化还原电位极高的底物,传统光氧化还原催化均失效。最近,化学家们开发了一种克服这一局限性的策略,即在光激发前对有机光氧化还原催化剂进行单电子氧化或还原,称为电子引发光氧化还原催化(Figure 1b)。其中,初始的单电子转移过程将闭壳层单线态催化剂转化为开壳层双线态的持久性自由基,该中间体具有增强的激发态氧化还原电势,从而可与通常惰性的底物发生SET过程。然而,形成双线态的关键SET反应必须通过电化学(电光催化)或涉及额外PET与化学计量氧化剂/还原剂的双光子过程进行。相反,到目前为止,尚未有文献报道使用持久性有机自由基作为活性光氧化还原催化剂的具体案例,特别是无需通过单线态预催化剂的电化学或光化学活化来持续生成自由基的体系(Figure 1c)。这类双线态光氧化还原催化剂既可提供基于电子预活化的光氧化还原催化模型所需的高氧化还原电势,又能简化实验装置并提升反应效率。近日,英国布里斯托尔大学Varinder K. Aggarwal与Adam Noble课题组研究发现,通过将B2cat2(1)与联吡啶类化合物(2)简单的混合,可生成持久性硼基-联吡啶自由基(3)。该自由基在基态下高度稳定,但在蓝光照射下可发挥异常强效的光还原剂功能(Figure 1d)。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。
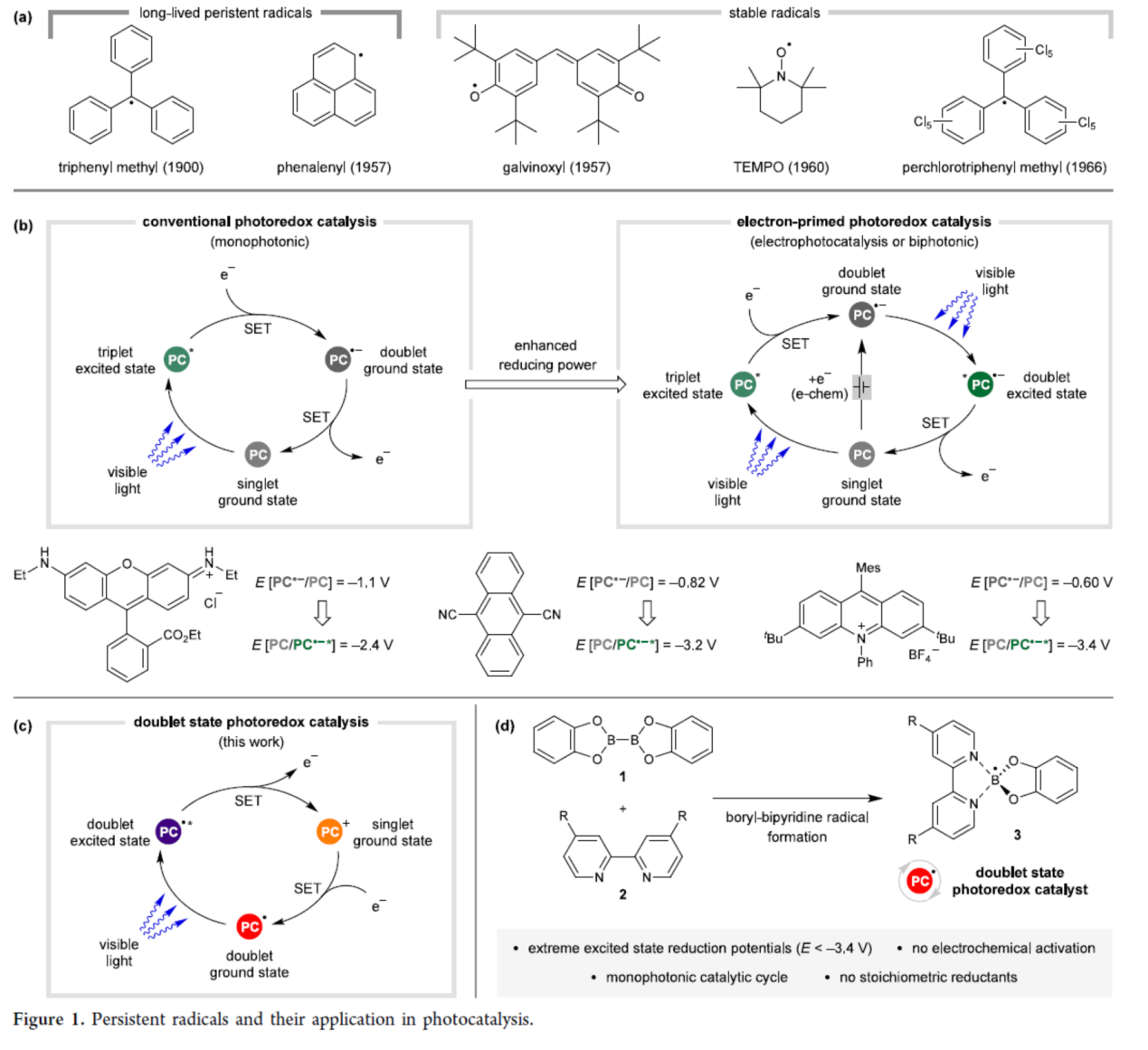
(图片来源:J. Am. Chem. Soc.)
首先,作者通过使用有机超电子供体(SEDs)作为光催化剂,可解决脱卤硼基化反应中的挑战,这一思路受基于二氢联吡啶的SED(4)在紫外光(UV)照射下是一种强力光还原剂的启发(Figure 2a)。尽管SED(4)无法实现催化循环,但相关SED(5)能催化热促进N-烷基吡啶鎓盐的硼基化反应,其中SED(5)通过B2cat2与4,4′-二叔丁基-2,2′-联吡啶(2a)在高温下原位反应生成。作者推断,若SED(5)能够像SED(4)一样实现光激发,其将为高挑战性的脱卤硼基化反应提供有价值的光催化剂。当在配体2a(20 mol%)存在下,4-溴哌啶(6a)可与B2cat2在蓝光照射下反应,可以80%收率得到硼酸酯产物7a(Figure 2b)。当体系中不添加2a或在无光条件均未能有效的反应,证实了联吡啶配体在生成光活性物种中的关键作用。当使用二甲氨基取代的联吡啶配体2b时,可将收率提升至92%,这归因于其供电子胺基可生成还原能力更强的催化剂。
其次,作者将无色固体2a和B2cat2在THF-d8中混合后,溶液立即变为黄色,25小时后转变为深绿色(Figure 2c)。令人惊讶的是,对该反应的1H NMR分析显示,2a的消耗率超过90%,但未检测到二氢联吡啶5或其他联吡啶衍生物。由于溶液在整个实验中保持均相状态,作者推测2a可能转化为核磁沉默(NMR-silent)的自由基,该推论通过EPR光谱得到证实。后续辐照实验导致硼鎓离子8a的生成,不仅证明了该自由基的光氧化还原活性,还暗示其结构可能为硼基-联吡啶自由基3a。同时,通过用镁还原硼鎓盐8a·PF6的独立合成进一步证实了上述的发现(Figure 2d)。上述结果表明,该反应体系中的光催化活性物种实为硼基-联吡啶自由基3。此外,CV实验结果表明,硼自由基3a具有稳定性,并能促进8a和二氢联吡啶-硼酸根阴离子9a之间的氧化还原循环(Figure 2e)。同时,自由基3a在基态是一种中等强度的还原剂,该性质支持了相关硼基-联吡啶自由基参与热促进硼基化反应的机理。
基于上述的研究以及相关文献的查阅,作者提出了一种合理的催化循环过程(Figure 2f)。首先,联吡啶2与B2cat2反应,生成硼基自由基催化剂3。其次,催化剂3经光激发生成强还原性的双线态激发态3*,其可与烷基溴6发生单电子转移,生成烷基自由基10和硼鎓盐8·Br。在DBU促进下,烷基自由基10与B2cat2进行硼基化反应,生成硼酸酯11及DBU稳定的硼基自由基12。基于Lewis碱稳定化硼基自由基的强还原能力,自由基12还原8的过程在热力学上有利,最终再生催化剂3并形成DBU·BrBcat 13。
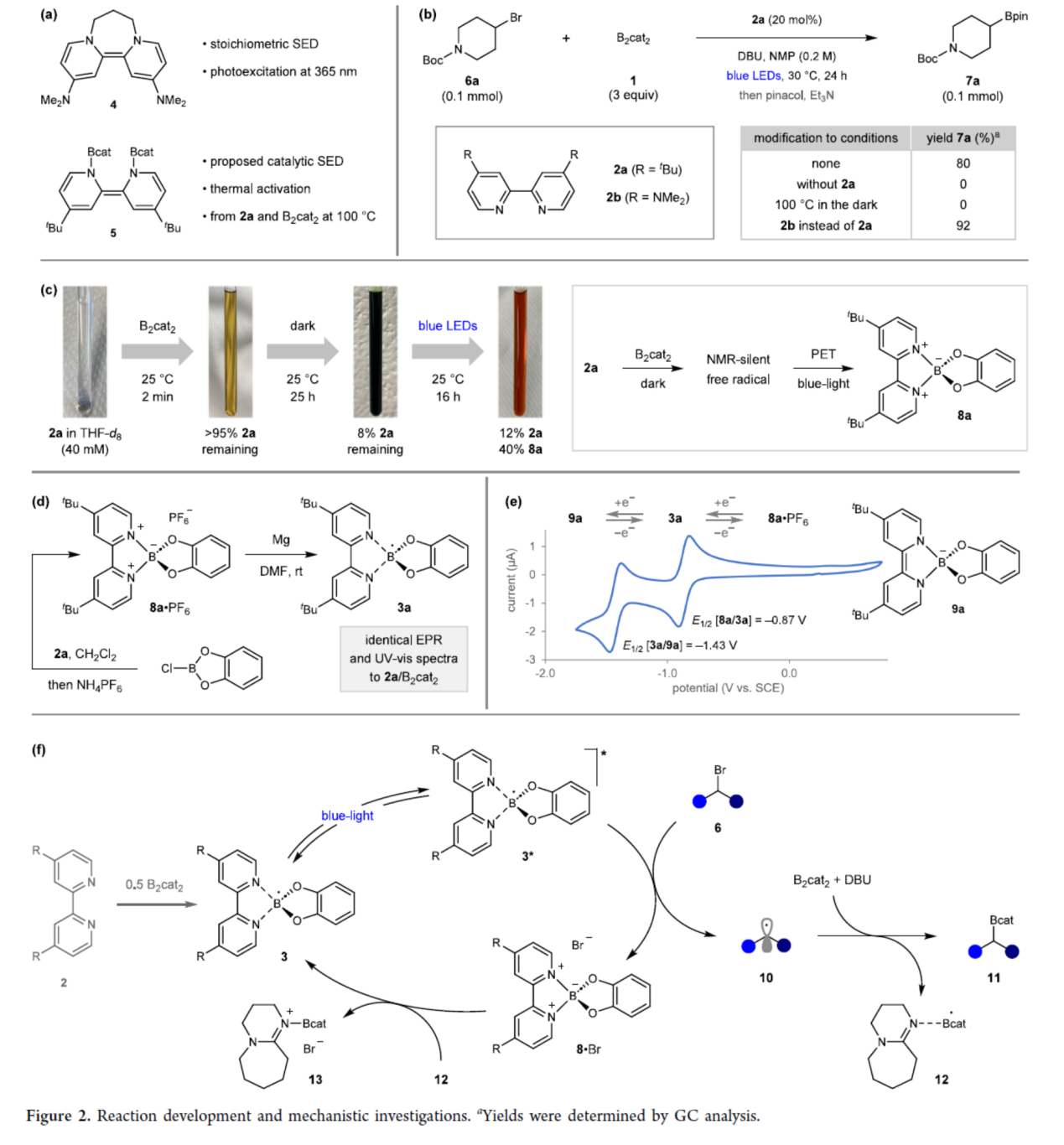
(图片来源:J. Am. Chem. Soc.)
在获得上述最佳反应条件后,作者对底物范围进行了扩展(Scheme 1)。首先,环状和非环状二级烷基溴与一级烷基溴,均可顺利反应,获得相应的产物7a-7r,收率为43-91%。值得注意的是,一系列含有烯基、羟基、烷氧羰基等活性的基团,均可体系兼容。对于环丙基取代的甲基溴,可以22%的收率得到开环产物7s,从而证实了反应涉及烷基自由基中间体的形成。其次,三级烷基溴,也是合适的底物,分别获得相应的产物7t(82%)和7u(74%)。1,1-二溴环丙烷衍生物,可进行双重脱溴硼化反应,可以63%的收率得到1,1-双硼酸酯产物7v。无环三级烷基溴化物,也能够进行反应,可以44%的收率得到产物7w。此外,一系列天然产物衍生的烷基溴化物,如(−)-降龙涎香醚、表雄酮、薯蓣皂素、剑麻皂素、Hecogenin等,均能够顺利进行反应,获得相应的产物7x-7z和7aa-7ae,收率为28-90%,具有优异的对映选择性。其中,在二级烷基溴与一级烷基溴代物共存体系中,反应展现出良好的区域选择性,优先生成产物7ae;但同时也分离到双硼基化副产物及烯酮还原产物。
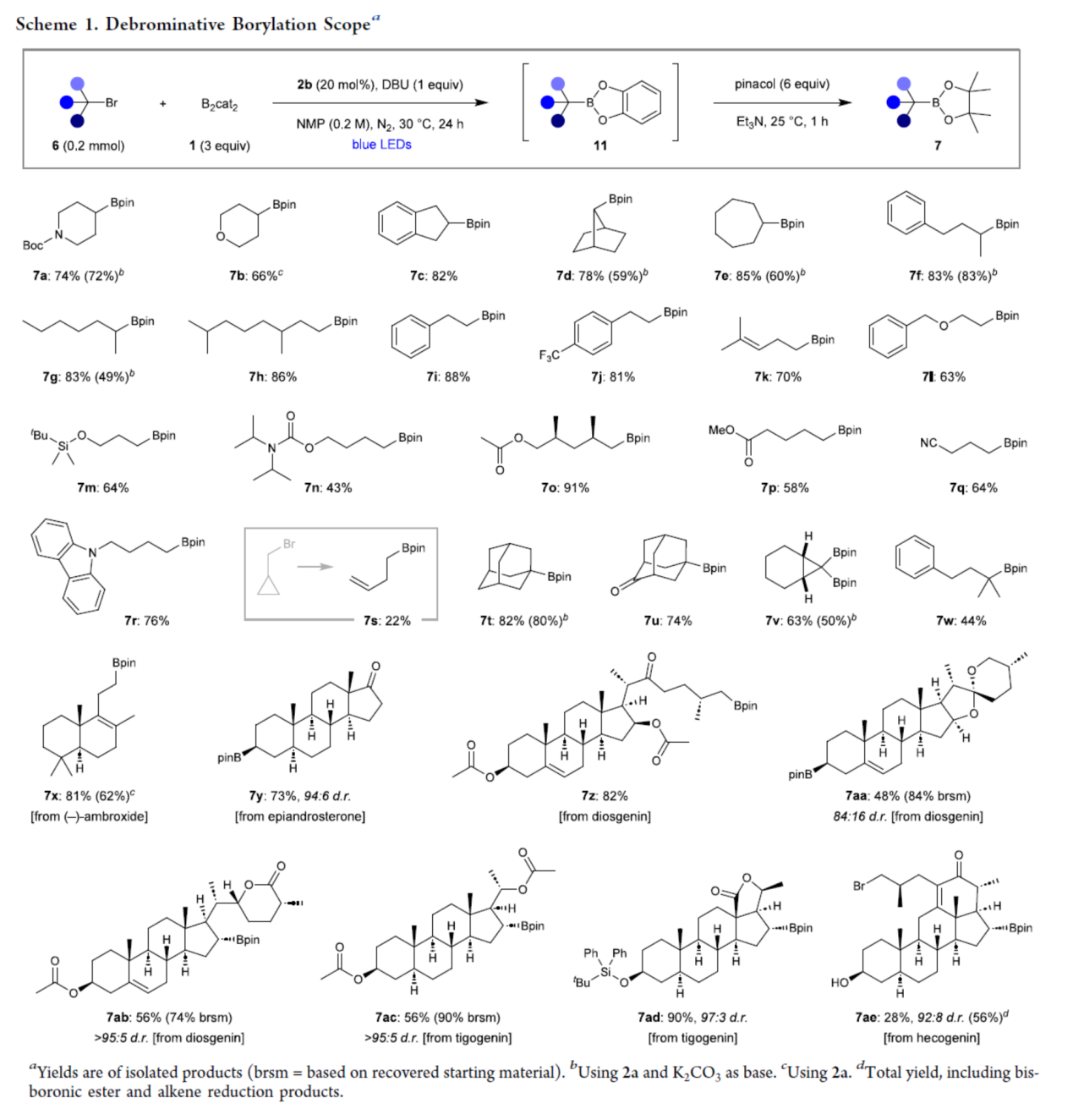
(图片来源:J. Am. Chem. Soc.)
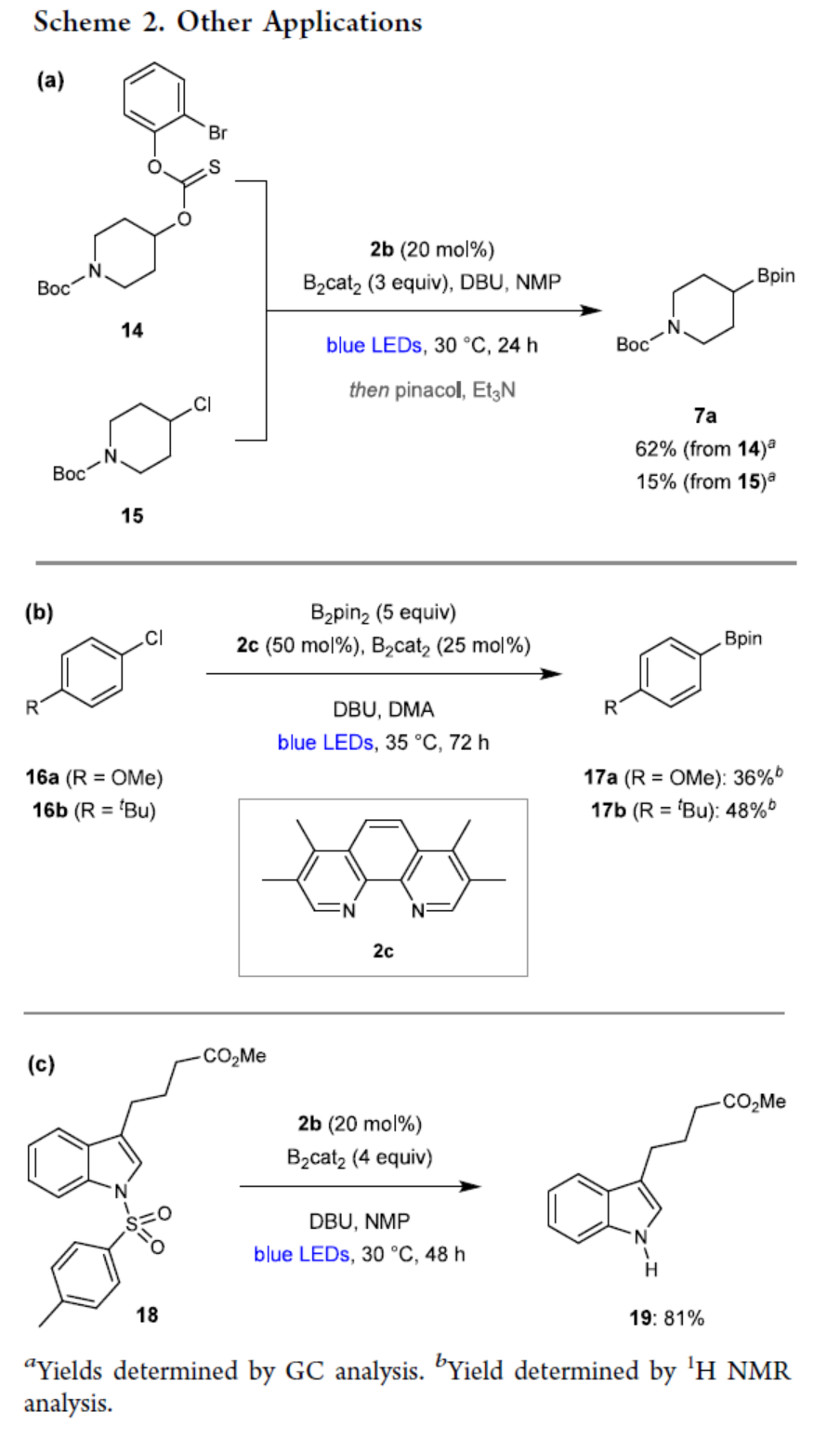
最后,作者对反应的实用性进行了研究(Scheme 2)。首先,催化剂3b可高效促进2-溴苯基硫代碳酸酯14发生脱溴反应生成芳基自由基,继而实现脱氧硼基化反应(Scheme 2a)。该体系对氯代烷烃15同样有效,虽然转化率较低,但仍成功获得硼基化产物7a(Scheme 2a)。其次,硼基自由基可成功催化氯代芳烃16的硼基化反应(Scheme 2b)。相较于配体2b,四甲基菲啰啉2c显著提升了反应产率,证实硼基自由基的形成不局限于联吡啶类配体。同时,由于芳基自由基的高活性,可采用B2pin2替代硼源,仅需亚化学计量的B2cat2即可生成催化剂3c。尽管脱氯硼基化反应的转化率中等,但其成功实施证明了硼基自由基3能催化高挑战性的单电子还原过程。此外,通过对反应条件的优化,还可实现N-对甲苯磺酰基吲哚18的脱磺酰化反应,以81%的收率得到产物19(Scheme 2c)。
(图片来源:J. Am. Chem. Soc.)
总结
英国布里斯托尔大学Varinder K. Aggarwal与Adam Noble课题组发现并表征了稳定持久性的硼基-联吡啶自由基,证实其可作为高效光氧化还原催化剂。该自由基仅需通过2,2'-联吡啶与B2cat2简单混合即可生成,且表现出超强的激发态还原能力。实验证明,这类双线态光氧化还原催化剂可驱动温和且操作简便的溴代烷烃的脱溴硼基化反应。最后,通过硼基-联吡啶自由基在脱氧、脱氯及N-脱磺酰化反应中的成功应用,彰显了此类自由基作为强还原型光催化剂的合成潜力。
文献详情:
Persistent Boryl Radicals as Highly Reducing Photoredox Catalysts for Debrominative Borylations.
Jingjing Wu, Hui Wang, Huaquan Fang, Kevin C. Wang, Deborin Ghosh, Valerio Fasano,Adam Noble,* Varinder K. Aggarwal*.
J. Am. Chem. Soc.2025
DOI:10.1021/jacs.5c03864
来源: 化学加


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 化学加
化学加 
