科学突破!创新中药制剂能化疗增敏!癌症患者有福了!
自噬指在饥饿、缺氧及能量应激状态下,细胞通过膜结构降解胞质细胞器和大分子的动态过程,其回收利用的降解产物能帮助细胞度过应激状态。有关研究表明,化疗可以杀死大部分的肿瘤细胞,但少数细胞可通过提高自噬活性从逆境中生存下来,一旦生长条件有利,细胞会恢复活力并导致肿瘤复发,是诱导肿瘤耐药并引起复发的重要原因。
金蓉颗粒(消癖颗粒,XPS)是一种国家批准用于乳腺癌高风险患者的处方药,以往研究发现它可以通过抑制CXCL1的表达来抑制乳腺癌的转移,并认为通过“癌细胞自噬”可能是其最核心的抗癌机制之一。但是,金蓉颗粒能否与化疗药物同时应用,其协同作用机制尚不清楚。
一篇名为“XIAOPI formula promotes breast cancer chemosensitivity via inhibiting CXCL1/HMGB1-mediated autophagy”的研究论文验证了金蓉颗粒通过抑制CXCL1/HMGB1介导的自噬作用提高乳腺癌化疗敏感性

图1 论文首页
一、金蓉颗粒能增强乳腺癌细胞对紫杉醇的敏感性
研究通过CCK-8试验和集落形成试验,观察金蓉颗粒对MDA-MB-231(基底样)和MCF-7(腔样) 乳腺癌细胞株增殖的影响。CCK-8及集落形成试验显示,金蓉颗粒能够抑制MDA-MB-231和MCF-7两种乳腺癌细胞的增殖,同时对正常乳腺细胞株无毒性。金蓉颗粒与紫杉醇联用,CCK-8检测结果显示,金蓉颗粒能明显增强紫杉醇诱导的MDA-MB-231和MCF-7细胞死亡、显著抑制集落生长(图2A和B)。同时药物外排实验表明金蓉颗粒可抑制乳腺癌细胞中表阿霉素外排。可见,金蓉颗粒在不损伤正常细胞的同时,还能提高乳腺癌细胞化疗敏感度。
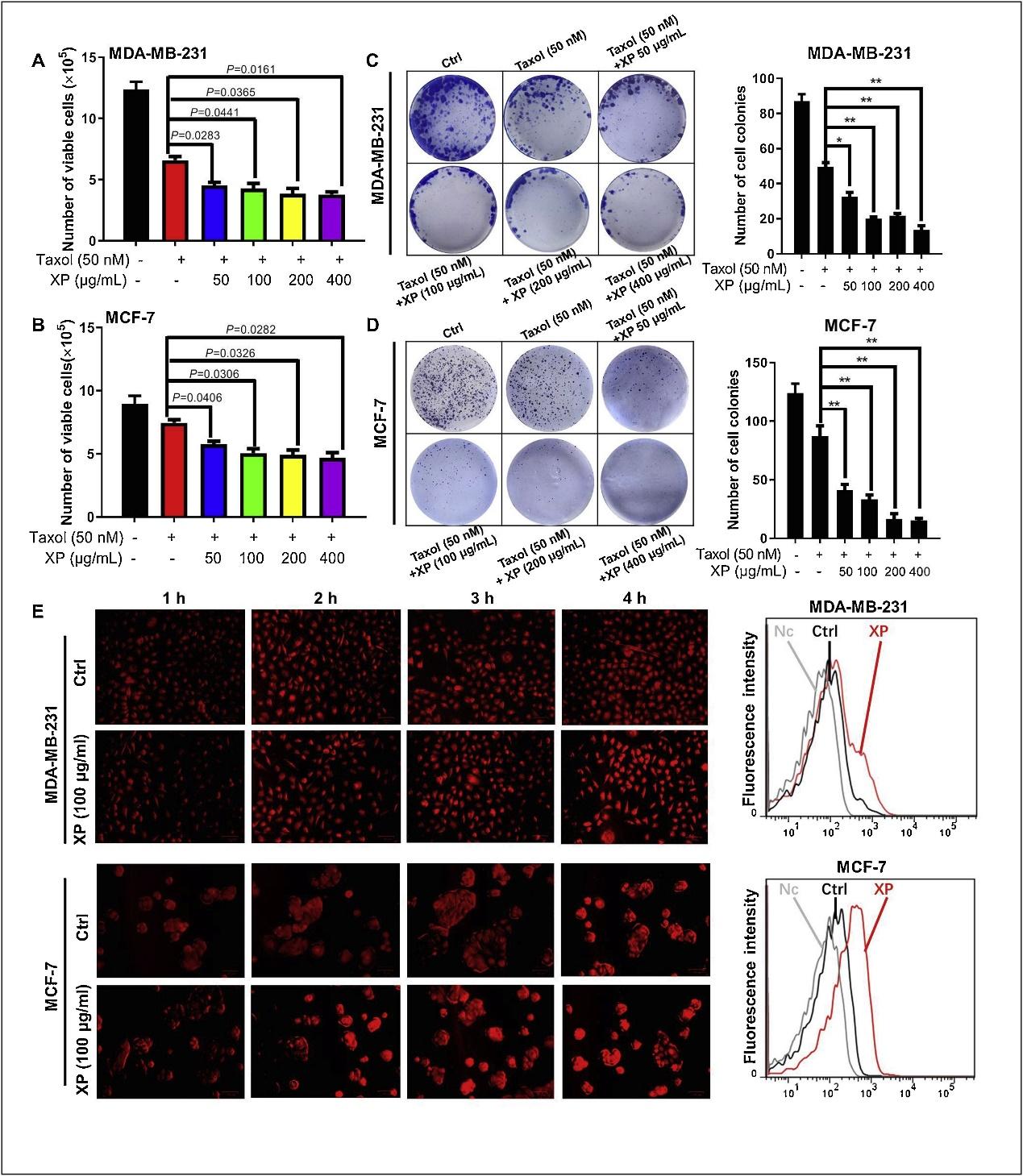
图2 金蓉颗粒能显著提高乳腺癌细胞的化疗敏感性
二、金蓉颗粒对雷帕霉素治疗后乳腺癌细胞自噬的影响
基于网络药理学与生物学过程分析,推测“癌细胞自噬”是金蓉颗粒核心抗癌机制之一。为验证此假设,研究金蓉颗粒与自噬激活剂雷帕霉素在10nm浓度下相互作用。透射电镜观察显示,有雷帕霉素时,金蓉颗粒可明显减少自噬泡数量(图3A)。蛋白质印迹法分析表明,金蓉颗粒与雷帕霉素联合处理组的自噬通量标记物LC3-II积累低于单用雷帕霉素组,且相关蛋白表达变化提示金蓉颗粒抑制雷帕霉素诱导的自噬通量(图3B)。自噬双标腺病毒基因检测也证实,金蓉颗粒能使雷帕霉素诱导的自噬体和自噬溶酶体数量减少(图3C)。所以,金蓉颗粒能够削弱雷帕霉素对乳腺癌细胞自噬的影响。
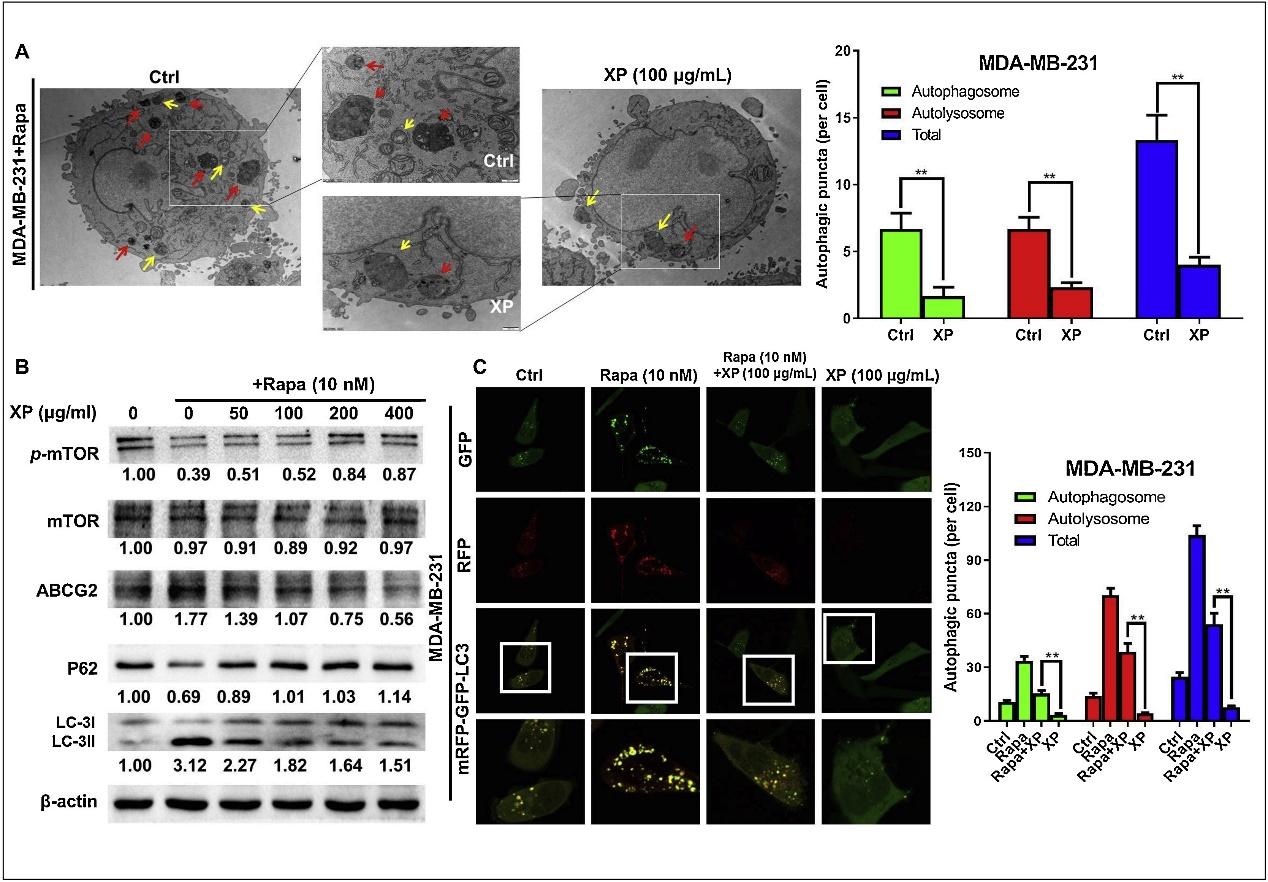
图3 金蓉颗粒抑制雷帕霉素诱导的乳腺癌细胞自噬
三、增强的自噬削弱金蓉颗粒的化疗增敏作用
已知自噬和癌症化疗耐药性存在关联,所以推测自噬增强会削弱金蓉颗粒的化疗增敏效果。实验显示,用雷帕霉素治疗后,金蓉颗粒的增敏作用降低。金蓉颗粒与紫杉醇联用,能抑制紫杉醇诱导的自噬,相关蛋白表达变化可证明这点。自噬双标腺病毒基因检测也有相同发现,在紫杉醇处理过的对照细胞中加入金蓉颗粒,可阻断自噬点的增多,但雷帕霉素能扭转金蓉颗粒减少自噬点的效果。不同浓度金蓉颗粒联合紫杉醇治疗时,相关蛋白表达以剂量依赖性呈现规律改变(图4E)。电子显微镜结果表明金蓉颗粒能减少自噬泡数量及细胞内蛋白水解(图4F-H)。总体而言,金蓉颗粒可抑制自噬,让乳腺癌细胞对紫杉醇更敏感。
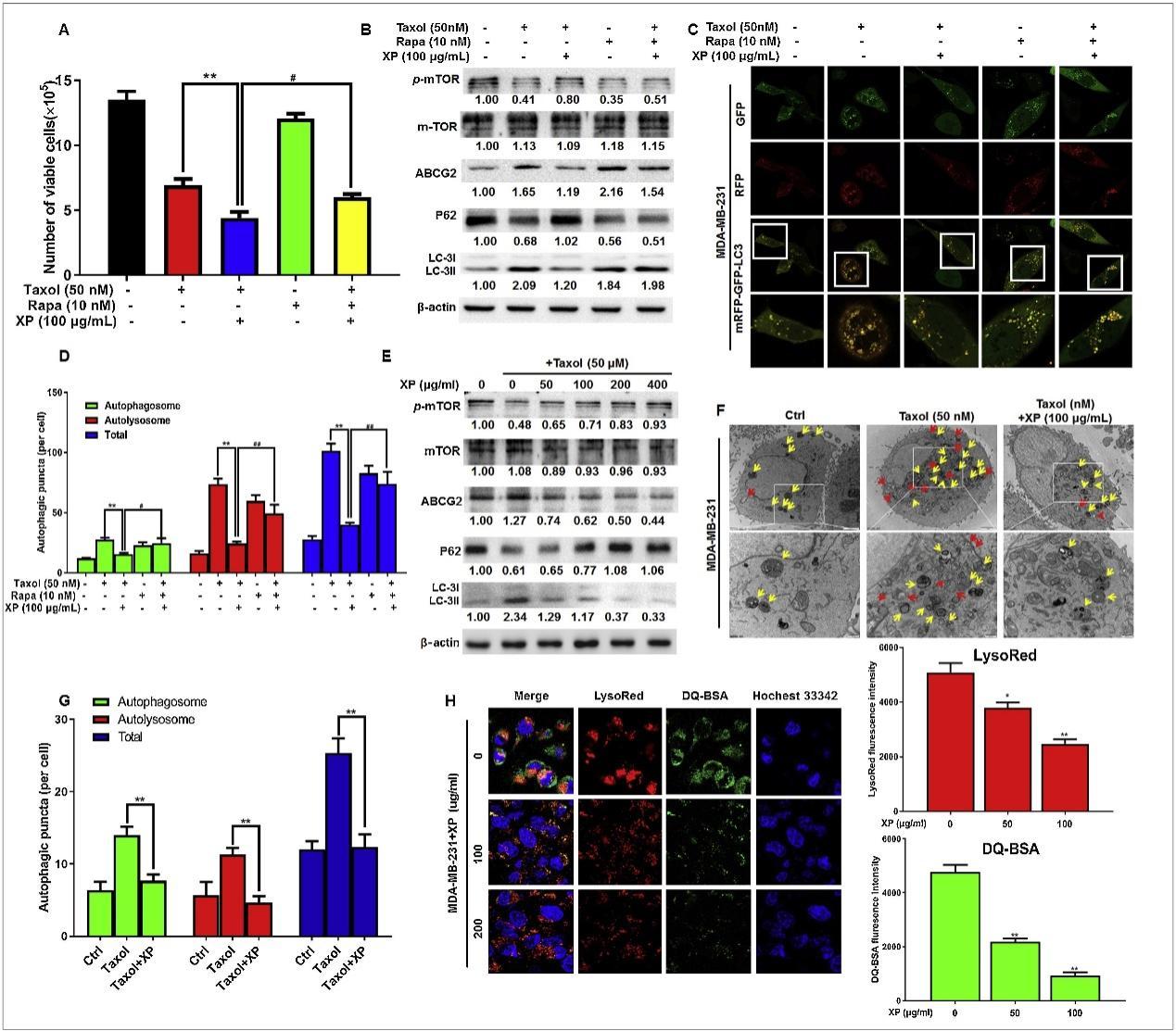
图4 增强的自噬降低了乳腺癌细胞对金蓉颗粒的化学敏感
四、金蓉颗粒抑制CXCL1介导的自噬活性增强化疗敏感性
以往研究发现,CXCL1是金蓉颗粒防治乳腺癌的关键靶点之一。因为金蓉颗粒能降低紫杉醇诱导的自噬,提高化疗效果,可以猜测CXCL1在自噬和耐药性方面意义重大。
实验结果显示,CXCL1的含量水平以剂量依赖性方式提高乳腺癌细胞在紫杉醇作用下的存活率,降低其含量则抑制癌细胞增殖。而且,CXCL1过多会促使自噬体等形成,降低其含量则抑制自噬体生成,这说明CXCL1触发自噬会让乳腺癌细胞产生耐药性。进一步研究发现,金蓉颗粒与紫杉醇协同抑制MDA-MB-231细胞增殖。当CXCL1水平升高,金蓉颗粒和紫杉醇的协同抑制效果消失,对相关信号的抑制也变弱。自噬双标腺病毒(mRFP-GFP-LC3)基因检测也证实了类似现象。综上,这些数据暗示金蓉颗粒的化疗增效作用中,CXCL1是关键的靶点之一。
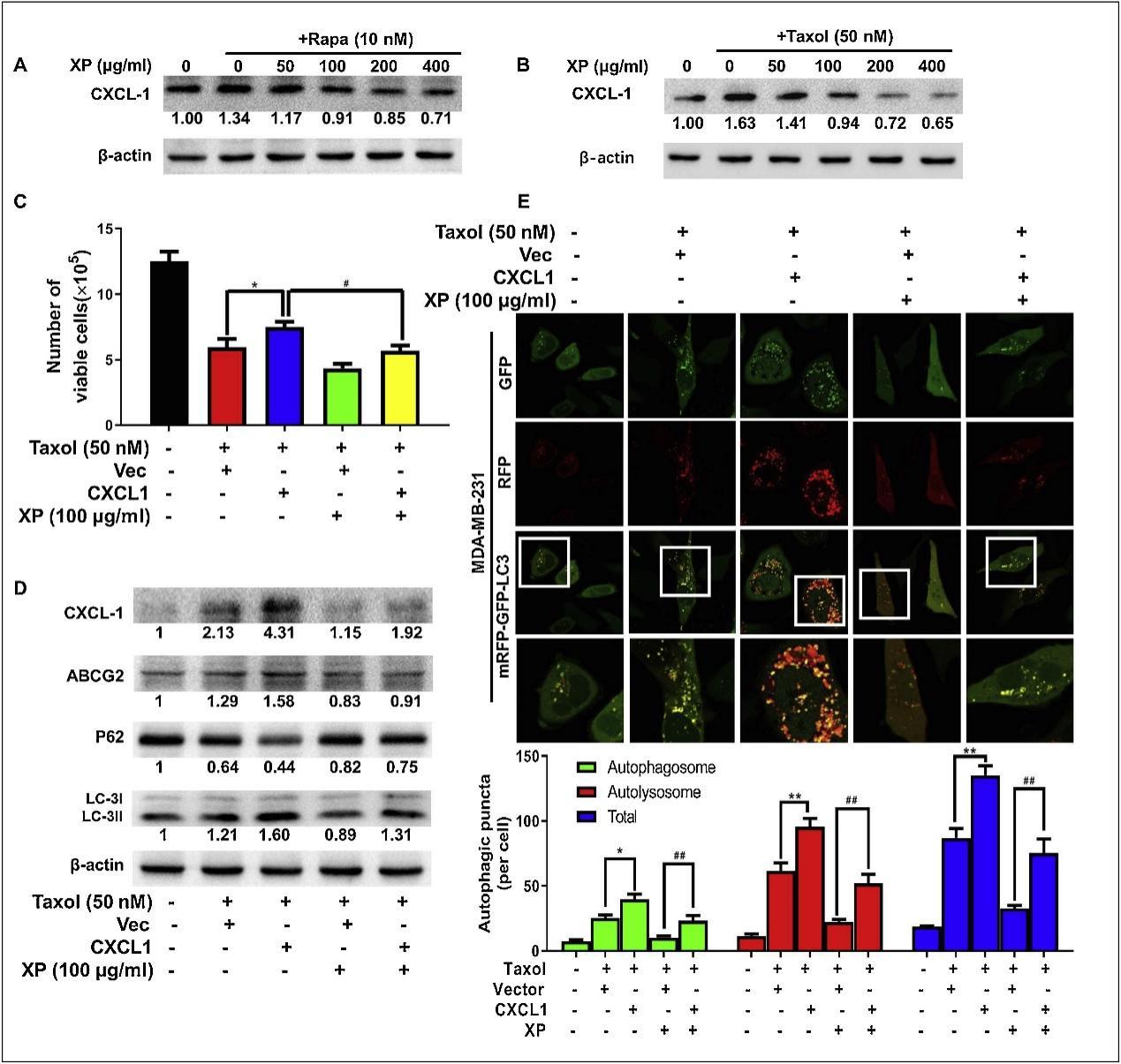
图5 金蓉颗粒抑制CXCL1导致乳腺癌细胞自噬活性降低,随后抑制化疗敏感性
五、金蓉颗粒主要通过CXCL1/HMGB1自噬轴发挥化学敏感性
研究采用高通量qPCR法检测了对照组、紫杉醇组、金蓉组和紫杉醇+金蓉组,四组细胞中自噬相关基因的mRNA水平。初步研究显示,紫杉醇会增强细胞自噬活性,而金蓉颗粒能削弱这一作用。自噬过程中多种关键基因都受到明显影响。其中,HMGB1在紫杉醇与金蓉颗粒共同处理后表达水平变化最大,RT-qPCR结果也证实了这一点。进一步蛋白质印迹结果显示,金蓉颗粒可抑制特定信号诱导的HMGB1表达,CXCL1与HMGB1呈正相关关系。通过干扰HMGB1,发现其缺乏能减弱CXCL1介导的LC3-II和ABCG2过表达减弱。综合来看,金蓉颗粒或许通过CXCL1/HMGB1自噬轴增强化疗效果。
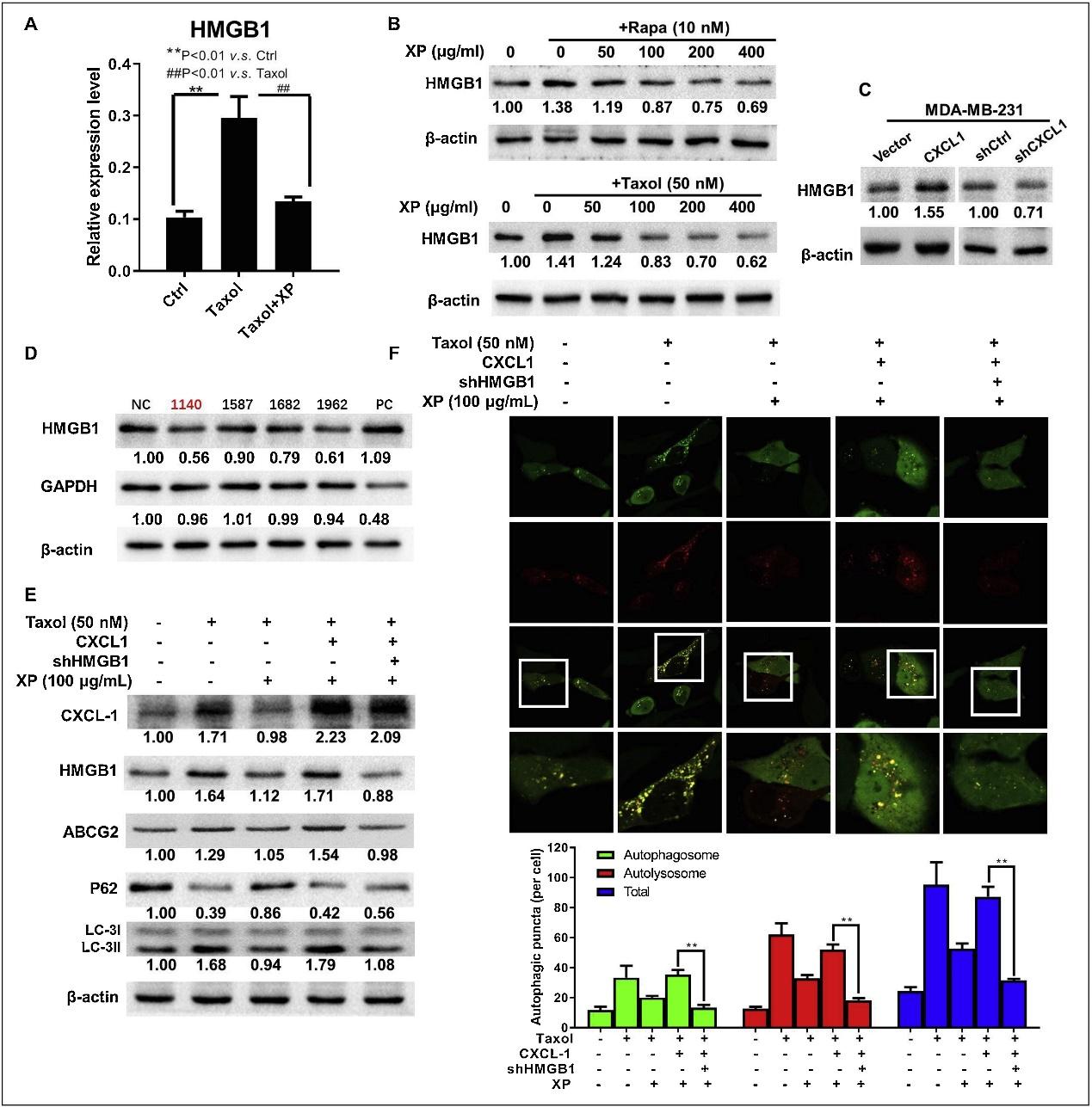
图6 金蓉颗粒主要通过CXCL1/HMGB1自噬轴发挥化学敏感性
六、金蓉颗粒增强体内紫杉醇对乳腺癌的化疗敏感性
基于体外研究成果,验证金蓉颗粒在体内的抗癌增效作用很有必要。研究将MDA-MB-231细胞注射到裸鼠乳腺,构建了乳腺癌模型。结果显示,单独使用紫杉醇或金蓉颗粒都能缩小肿瘤体积并抑制肿瘤生长,而联合组作用效果最好。和单紫杉醇组相比,联合治疗组的肿瘤坏死和出血现象更少(图7A-C)。同时在整个实验过程中,联合组也未导致显著的体重减轻(图7D),也没出现食欲差、毛发状态不佳等其他不良事件。免疫组织化学分析显示,金蓉颗粒能显著降低肿瘤组织内CXCL1、LC3、HMGB1和ABCG2等自噬相关蛋白的表达水平(图7E),同时进一步增强紫杉醇对细胞增殖抗原Ki67的抑制作用。这说明金蓉颗粒有潜力成为安全有效的新型抗癌增效药物。
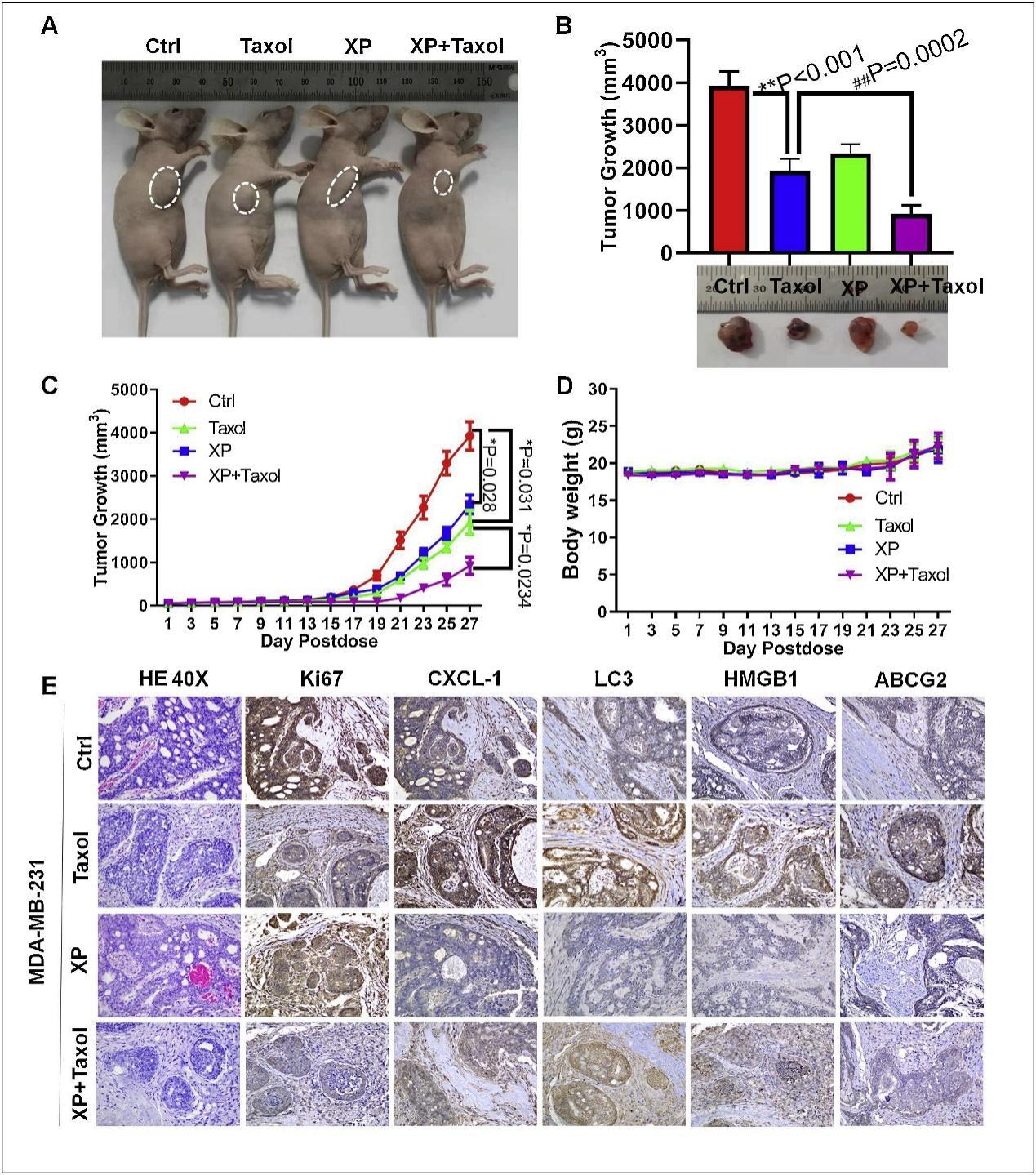
图7 金蓉颗粒增强了对携带乳腺癌细胞MDA-MB-231的小鼠异种移植物的体内紫杉醇化学敏感性
七、金蓉颗粒对斑马鱼乳腺癌异种移植模型中的乳腺癌化疗敏感
研究采用斑马鱼胚胎检测金蓉颗粒体内应用的安全性,研究结果显示金蓉颗粒单独使用没有显著影响斑马鱼的胚胎孵出率、胚胎活性和致畸率,同时金蓉颗粒和紫杉醇联合应用也没有增加紫杉醇对胚胎的毒性,联合用药组孵出率、胚胎活性和致畸率无显著变化。
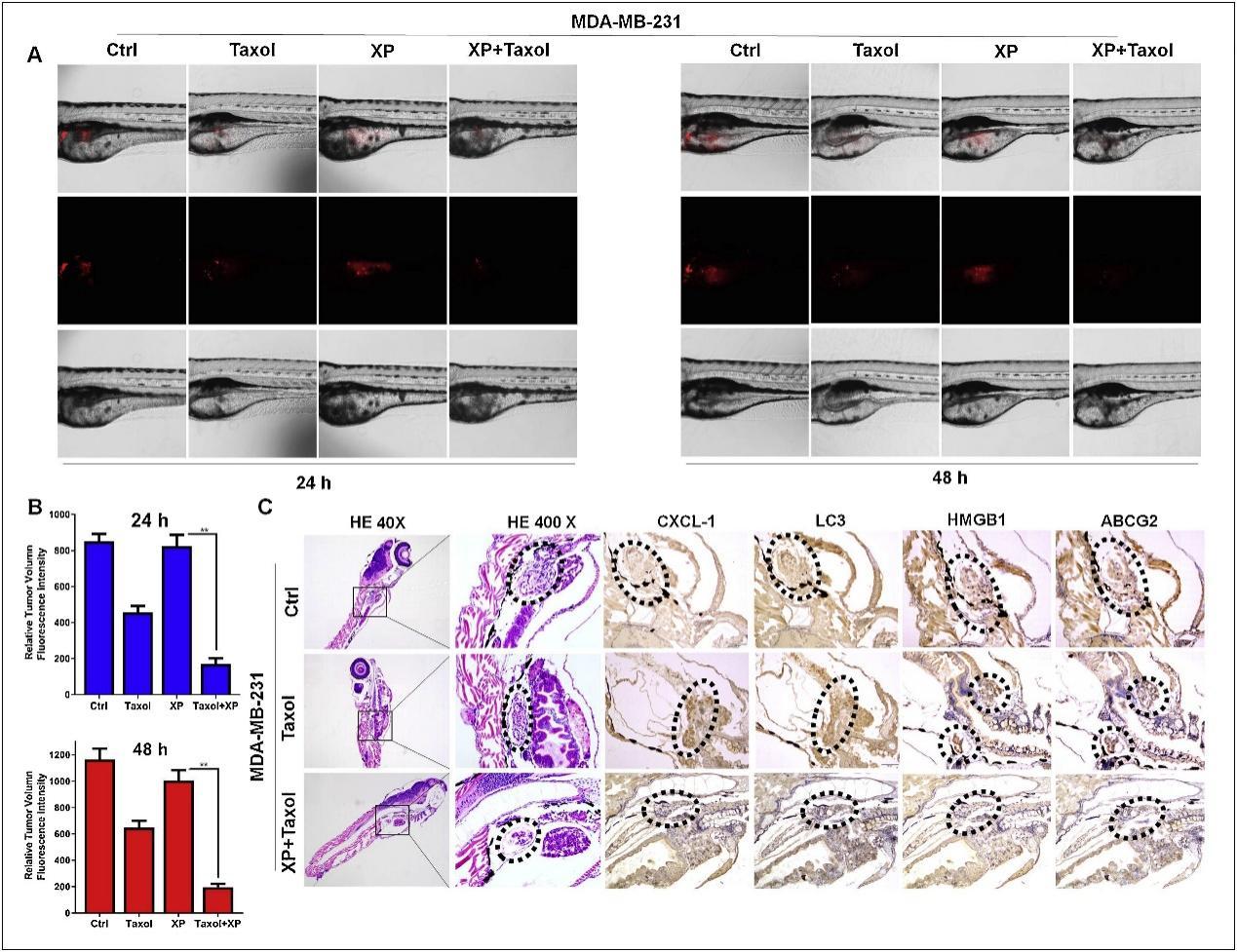
图八 斑马鱼乳腺癌异种移植模型中金蓉颗粒对乳腺癌的化疗增敏作用
综上所述,以自噬为切入点建立起宿主整体与肿瘤局部之间的共调节关系,解析肿瘤微环境对肿瘤化疗耐药形成的作用和分子机制,为抗肿瘤药物耐药性开辟了一条完全不同的新道路。金蓉颗粒能够通过抑制CXCL1/HMGB1通路调控的自噬作用,提高乳腺癌化疗的敏感性,为支持金蓉颗粒在化疗期间的应用提供了新的证据,为乳腺癌的临床治疗提供了新的思路和依据。
(本文内容源自公开发表的科学研究,用药请遵医嘱)
参考文献:Wang N, Yang B, Muhetaer G, et al. XIAOPI formula promotes breast cancer chemosensitivity via inhibiting CXCL1/HMGB1-mediated autophagy [published correction appears in Biomed Pharmacother. 2022 May;149:112867. doi: 10.1016/j.biopha.2022.112867.]. Biomed Pharmacother. 2019;120:109519. doi:10.1016/j.biopha.2019.109519
关注我们:获取更多抗癌资讯与健康科普!
来源: 奇绩金蓉


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 奇绩仟金方
奇绩仟金方 
