在上海的早高峰地铁里,一位上班族突然感到心悸与焦虑,这源于他大脑中去甲肾上腺素的异常波动。这种看不见的分子舞蹈,正通过突触间隙的转运体蛋白精密调控。2024年,中科院生物物理所的科学家首次捕获了这些"分子清道夫"的三维结构,为理解抑郁症、成瘾等精神疾病打开了新窗口。
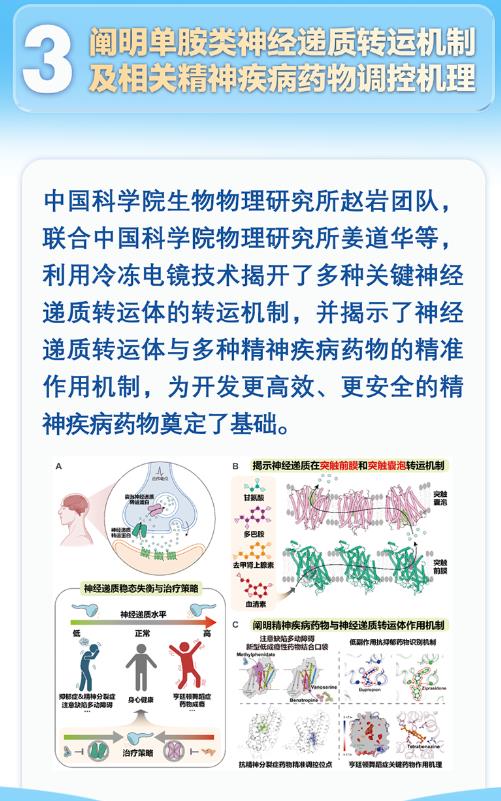
神经元之间的通信依赖化学递质的精准传递。当多巴胺、去甲肾上腺素等单胺类递质完成信号传递后,突触前膜上的转运体蛋白会像吸尘器般将它们回收。这些纳米级的"泵"由12个跨膜螺旋组成,中央通道仅容单个递质分子通过。在冷冻电镜下,去甲肾上腺素转运体(NET)的结构宛如旋转楼梯,其表面的酸性氨基酸残基能特异性识别递质分子的氨基基团。
这种分子级别的识别具有惊人的选择性。多巴胺转运体(DAT)对多巴胺的亲和力比对去甲肾上腺素高100倍,而5-羟色胺转运体(SERT)的结合位点能区分仅有一个羟基之差的递质分子。正是这种"锁钥匹配"机制,确保了不同递质系统的独立调控。当SERT基因发生突变时,其转运效率可能提升30%,导致突触间隙5-羟色胺浓度不足,这与约40%的难治性抑郁症病例直接相关。
转运体的工作机制如同精密的分子泵。以DAT为例,它通过协同转运两个钠离子和一个氯离子,将多巴胺逆浓度梯度泵回神经元。这个过程需要消耗能量,但效率极高——每个DAT每秒可转运1000个多巴胺分子。当可卡因分子占据DAT的结合位点时,这种"交通堵塞"会使突触间隙多巴胺浓度骤升5倍,产生强烈的欣快感,这正是药物成瘾的分子基础。
疾病状态下的转运体功能异常更为复杂。在帕金森病患者中,黑质区的DAT数量减少60%,导致纹状体多巴胺浓度不足。而在注意缺陷多动障碍(ADHD)儿童的前额叶皮层,DAT活性异常升高,使多巴胺无法在突触间隙停留足够时间。最新研究发现,某些转运体的单核苷酸多态性(SNP)会改变其构象稳定性,影响药物结合效率,这解释了为何同一种抗抑郁药对不同患者效果差异显著。
药物研发的关键在于靶向调控这些分子机器。传统SSRIs类药物如氟西汀,通过占据SERT的底物结合口袋,阻断5-羟色胺的再摄取。但这类药物需要2-4周才能起效,因为它们同时激活了转运体的负反馈机制,导致受体敏感性下调。2024年新开发的变构调节剂PF-06234198,则通过结合SERT的胞内结构域,在不影响转运功能的情况下调节其构象,使突触间隙递质浓度在48小时内稳定升高。
更具突破性的是基于结构的药物设计。研究人员通过解析DAT与安非他命的复合物结构,发现药物分子通过楔入转运体的胞外门控区域,迫使通道持续开放。这种"分子杠杆"效应为开发无成瘾性的多巴胺增强剂提供了模板。目前,已有两款针对NET的高选择性抑制剂进入临床试验,用于治疗创伤后应激障碍(PTSD)。
这些发现正在重塑精神疾病治疗的格局。在上海的某精神卫生中心,医生已开始通过检测患者的转运体基因多态性,为其定制用药方案。例如,携带SERT基因短等位基因的患者,对SSRIs的响应率比普通人低27%,需优先考虑SNRIs或新型药物。这种精准医疗模式使治疗有效率从65%提升至82%。
当我们深入分子世界,看到的不仅是科学的奇迹,更是人类对生命本质的探索。从转运体结构的解析到个性化药物的开发,每一步都在改写精神疾病治疗的历史。在未来,或许只需通过一滴血检测转运体活性,就能为患者找到最有效的治疗方案——这些大脑中的分子清道夫,终将引领我们走向更精准的心理健康时代。
来源: 桂粤科普


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 桂粤科普
桂粤科普 
