3D打印技术已经悄然走进了我们生活的各个角落——从房屋建筑到精密的纳米制造,它正改变着传统生产方式。今天,我们要聊聊一项前沿应用:利用纳米级3D打印技术,打造能够精确控制疫苗释放的黑科技系统。
从宏观到微观:3D打印技术的多维应用
大家都知道,3D打印技术可以打印出各种各样的物品:在大尺度上,可以用来打印房屋;在微尺度上,它甚至可以打印纳米和微米级别的部件。尤其在生物医药领域,微米级的打印技术正被用于制造精准的疫苗递送系统。

图1. 3D打印房屋(Printerra公司)
传统疫苗注射的挑战
目前,大多数疫苗是通过直接肌肉注射来实现免疫应答。这种方式虽然简单,但也存在不少问题和不足:
1.多次免疫的需求:有些疫苗需要多次注射才能建立起足够的免疫保护。
2.免疫应答难以控制:注射后,体内的抗原释放情况无法精确调控,导致产生的免疫应答类型不易把握。例如,如何平衡TH1和TH2型免疫反应,直接影响疫苗的保护效果。
正是因为这些问题,科学家们一直在寻找一种能够精确控制疫苗释放速率和持续时间的新方法,而纳米级的3D打印技术正为我们提供了全新的解决方案。
纳米3D打印技术:打开精准递送的新大门
随着二维双光子聚合(2PP)3D打印技术的不断发展,我们已经能够实现纳米和微米尺度的高精度打印。例如,德国Nanoscrib公司的多款打印机已具备极高的分辨率,能够制造出微小而复杂的结构。
然而,要将这种技术应用到疫苗递送上,还存在一大难题:传统树脂往往缺乏生物相容性、快速聚合和可调控的降解动力学。这些特性正是精确控制疫苗释放所必须的。

图2. 纳米3D打印机(Nanoscrib公司)
SCRIBE树脂:帝国学院Molly团队的创新之作
为了解决这一瓶颈,近期伦敦帝国学院Molly团队开发出一种全新的、可生物降解的2PP打印墨水——SCRIBE树脂。该研究以“Nanoscale Biodegradable Printing for Designed Tuneability of Vaccine Delivery Kinetics” 为标题发表于Advanced Materials期刊上。这款优化后的树脂具有多项突破性优势:
1.亚微米分辨率打印:SCRIBE树脂支持极高的打印精度,使得复杂的微结构(如空心微粒)得以制造。
2.快速打印速度:相比传统2PP方法,SCRIBE树脂能够实现更高效的打印,大大提高了生产效率。
3.可调控的溶胀与降解特性:通过改变共聚单体的组成,不仅不会影响打印分辨率,还能精确调整材料的溶胀和降解行为。
4.高丙烯酸酯转化率和良好生物相容性:其降解产物对人体细胞友好,具有很好的生物安全性。
利用SCRIBE树脂,研究人员成功设计并制造出结构独特的空心微粒,这些微粒能够高效负载抗原蛋白,并实现长期封装,成为疫苗递送系统的重要核心部件。
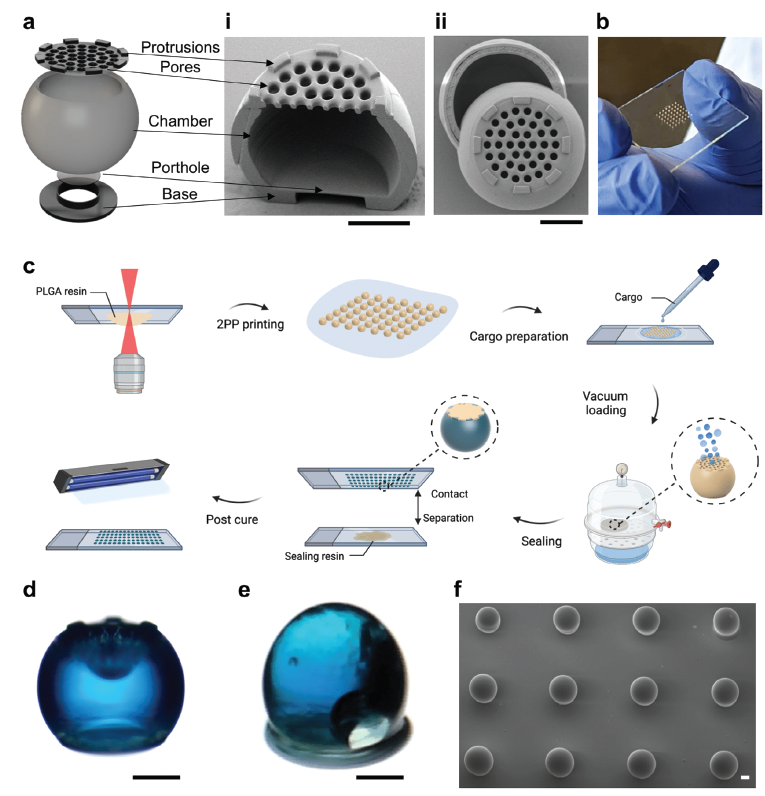
图3. SCRIBE树脂中空微粒的设计与微细加工(参考文献6)
体内实验:释放速率与免疫应答的精密调控
实验结果显示,SCRIBE颗粒的厚度和化学组成直接影响了疫苗释放的动力学,持续释放时间可以从数周延长到数月。小鼠模型体内实验显示释放速率影响免疫反应类型,慢释放的配方更倾向于诱导TH2相关反应,而快释放的配方则偏向TH1相关反应。此外,对比传统的初免-加强免疫方案,1μm大小的NVP颗粒只需单次注射,就能诱导出与双次注射可溶性疫苗相似的抗体滴度,而且免疫反应启动更快。更重要的是,SCRIBE颗粒在体内能完全降解或展现出极高的生物相容性。
通过直接激光写入技术,SCRIBE树脂不仅实现了对疫苗递送微粒的精准制造,还成功确定了持续释放与最大抗体滴度和亚型转换之间的相关性,为未来的单注射疫苗开发提供了可能性。
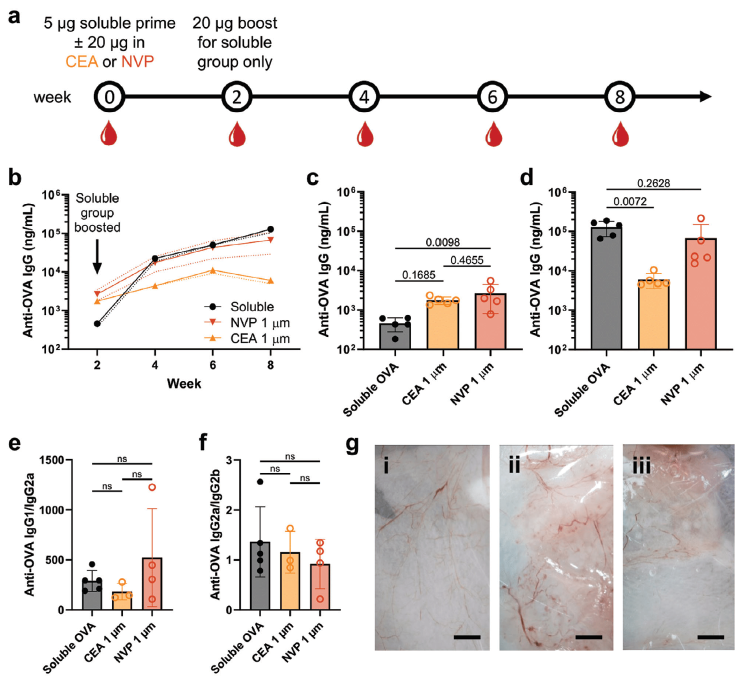
图4. SCRIBE 技术的单剂疫苗接种效果(参考文献6)
展望未来:智能疫苗递送的新方向
SCRIBE技术的成功为疫苗递送系统带来了革命性的改变。通过纳米级3D打印技术和SCRIBE树脂,科学家们正迈出一步,实现疫苗递送系统的精密控制。这不仅有望简化免疫程序,降低疫苗接种的次数,还可能带来更理想的免疫效果,为全球公共卫生事业开辟全新的发展道路。
参考文献:
1.Kronenfeld, J. M., L. Rother, M. A. Saccone, M. T. Dulay and J. M. DeSimone (2024). "Roll-to-roll, high-resolution 3D printing of shape-specific particles." Nature 627(8003): 306-312.
2.Tran, K. T. M., T. D. Gavitt, N. J. Farrell, E. J. Curry, A. B. Mara, A. Patel, L. Brown, S. Kilpatrick, R. Piotrowska, N. Mishra, S. M. Szczepanek and T. D. Nguyen (2021). "Transdermal microneedles for the programmable burst release of multiple vaccine payloads." Nat Biomed Eng 5(9): 998-1007.
3.Sangesland, M., A. Torrents de la Pena, S. Boyoglu-Barnum, L. Ronsard, F. A. N. Mohamed, T. B. Moreno, R. M. Barnes, D. Rohrer, N. Lonberg, M. Ghebremichael, M. Kanekiyo, A. Ward and D. Lingwood (2022). "Allelic polymorphism controls autoreactivity and vaccine elicitation of human broadly neutralizing antibodies against influenza virus." Immunity 55(9): 1693-1709 e1698.
4.Lavelle, E. C. and C. P. McEntee (2024). "Vaccine adjuvants: Tailoring innate recognition to send the right message." Immunity 57(4): 772-789.
5.Ma, Y. F., K. Chen, B. Xie, J. Zhu, X. He, C. Chen, Y. R. Yang and Y. Liu (2024). "Enhanced Antibody Response to the Conformational Non-RBD Region via DNA Prime-Protein Boost Elicits Broad Cross-Neutralization Against SARS-CoV-2 Variants." Emerg Microbes Infect: 2447615.6.Peeler, D. J., R. Sun, C. Kutahya, P. Peschke, K. Zhou, G. Brachi, J. Yeow, O. Rifaie-Graham, J. P. Wojciechowski, T. F. F. Fernandez Debets, V. LaLone, X. Song, K. Polra, P. F. McKay, J. S. Tregoning, R. J. Shattock and M. M. Stevens (2025). "Nanoscale Biodegradable Printing for Designed Tuneability of Vaccine Delivery Kinetics." Adv Mater: e2417290.
来源: 马云飞(中国医学科学院医学生物学研究所)


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 云兮疫苗科普
云兮疫苗科普 
