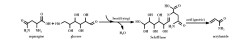
丙烯酰胺(Acrylamide,简称AM),是食物发生“美拉德反应”时的一个副产物42。香味越浓郁,丙烯酰胺的产量就会越高42。丙烯酰胺对人和动物都具有神经毒性43,相对分子质量71.08、化学式为C3H5NO、分子式为CH2=CH-CONH2。是一种不饱和酰胺,熔点84.5℃、沸点125℃。常温常压下为白色结晶状固体,不易挥发。易溶于水、乙醇、丙酮、醚和三氯甲烷等极性溶剂,在84.5℃以上高温或在光和氧化剂作用下易聚合。丙烯酰胺是丙烯酰胺系中最重要、最简单的一种,可用作有机合成及高分子材料的原料,主要用于生产聚丙烯酰胺。
日常生活中,丙烯酰胺可见于化妆品6、吸烟、经高温(>120℃)烹饪的富含淀粉食物及饮用水中7。丙烯酰胺水溶性强,可通过皮肤、黏膜、呼吸道和胃肠道等进入体内具有遗传毒性、免疫毒性、神经毒性、生殖毒性、致癌性,国际癌症研究机构(IAF)于1994年将其定为二类致癌物,并被列入REACH法规第二批高关注度物质之一。2017年10月27日,世界卫生组织国际癌症研究机构公布致癌物清单:丙烯酰胺在2A类致癌物中1。
相关历史
技术发展历程
1893年德国学者Moureu通过丙烯酰-氯氨化法合成AM获得成功8,但工业上都是使用丙烯腈(AN)水合来生产AM的9。
1954年,美国氰氨公司开发出硫酸催化合成AM技术,推动了其工业化进程,在此后近20年时间内一直是唯一的AM工业化生产技术,但其流程复杂,设备腐蚀严重,产品精制困难,对环境污染也严重。
20世纪70年代初,日、美同期开发出铜系催化剂催化合成AM技术,此法在20世纪70年代中期基本取代硫酸法。与硫酸法相比产品纯度及转化率均有很大的提高,流程短且腐蚀小,环境污染也较少。本法又分为固定床催化水合法和悬浮床催化水合法。固定床催化水合法以美国道化学公司为代表,采用Cu-Cr催化剂,该法具有催化剂易活化、易再生的特点,系统全封闭;是浮床催化水合法以日本三菱化成公司和三井东压公司为代表,采用Cu-Ni催化剂,该法催化剂可连续再生、补充,反应稳定,但设备结构复杂、工艺流程长10。
1973年,法国学者Galzy等发现了能催化水解的微生物Brevbacterium R312,可用于催化合成AM。
1985年日东化学公司采用自行选育的Rhodococcus sp. N-774建立了产能为4 000 t/a的试生产装置。
1988年京都大学山田秀明教授研发团队选用的Pseudomonaschlororaphis B23应用于工业化生产丙烯酰胺。
1992年选育出酶活性更高的R.rJ1菌种,使AM生产规模提升至万吨级,R.rJ1是微生物法生产AM的第三代生物催化剂。
我国生物法生产丙烯酰胺工业化技术
第一代工业化技术
由上海农药研究所在“八五”科技攻关期间开发的“离心分离细胞+固定化细胞催化反应+离心分离产物”工艺,其工业化应用单位有:浙江桐庐汇丰、江苏南天、江西昌九、河北万全和山东胜利油田长安实业等公司11。
第二代工业化技术
由上海农药研究所在“九五”科技攻关期间开发的“离心分离细胞+游离细胞催化反应+超滤膜分离产物”工艺:其工业化应用单位有:北京恒聚和山东胜利油田长安实业等公司。
第三代工业化技术
基于Suntar公司生产的Ultra-floTM膜系统,开发出“微滤膜分离细胞+游离细胞催化反应+超滤膜分离产物”的连续化生产工艺。早期工业化应用单位有:吉化集团环保实业和大庆油田东吴实业等公司。当前,此“双膜分离提取法”技术已发展成为生物法生产丙烯酰胺的主流工艺12,选用的中空纤维膜,在单位体积膜组件中有效膜面积最大,具有结构简单、分离效率高、操作方便、易于清洗、价格低廉、不产生二次污染等优点,含腈水合酶菌体收率>98%,远高于第一、二代工业化技术中的离心分离方法。
基于生物法生产AM的诸多优势,当前国内工业化生产AM的方法几乎均采用生物法技术,提取精制采用“双膜法-离子交换”工艺。我国生物法生产AM的第三代工业化技术经过多年的改良与优化,在产能规模和工艺技术方面均位于世界前列。
食品中的丙烯酰胺
2002年4月,瑞典科学家在油炸马铃薯中首次发现AM存在13,随后英国等一些国家相关机构对AM在食品中的含量进行了测定并证实瑞典科学家的发现。因AM的毒性和潜在的致癌作用而迅速在世界范围引起研究热潮。
 2003年美国食品药物管理局(foodanaDrug Administration,FDA)公布的数据显示,常见食品中AM质量浓度约在0~2510ug/kg之间14,尤其在一些含高碳水化合物食物(如马铃薯、饼干、咖啡等)经高温(>120°)处理,如烹饪、煎炸、烘烤,AM含量最高可达2300ug/kg 15,远超过世界卫生组织规定的日常饮用水中AM的限值0.5ug/kg,因此,环境和食物中的AM暴露严重影响着人类的健康。
2003年美国食品药物管理局(foodanaDrug Administration,FDA)公布的数据显示,常见食品中AM质量浓度约在0~2510ug/kg之间14,尤其在一些含高碳水化合物食物(如马铃薯、饼干、咖啡等)经高温(>120°)处理,如烹饪、煎炸、烘烤,AM含量最高可达2300ug/kg 15,远超过世界卫生组织规定的日常饮用水中AM的限值0.5ug/kg,因此,环境和食物中的AM暴露严重影响着人类的健康。
分子结构数据
1、摩尔折射率:19.23
2、摩尔体积(cm3/mol):73.9
3、等张比容(90.2K):174.6
4、表面张力(dyne/cm):31.0
 5、极化率(10-24cm3):7.62
5、极化率(10-24cm3):7.62
计算化学数据
1、疏水参数计算参考值(XlogP):-0.7
2、氢键供体数量:1
3、氢键受体数量:1
4、可旋转化学键数量:1
5、互变异构体数量:2
6、拓扑分子极性表面积(TPSA):43.1
7、重原子数量:5
8、表面电荷:0
9、复杂度:57.9
10、同位素原子数量:0
11、确定原子立构中心数量:0
12、不确定原子立构中心数量:0
13、确定化学键立构中心数量:0
14、不确定化学键立构中心数量:0
15、共价键单元数量:1
理化性质
物理性质
外观:白色或淡黄色结晶
气味:无气味
pH: 5.0-6.5(50%水溶液)
熔点/凝固点(℃): 84.5℃
沸点(℃): 125(3.33kPa): 192.6
密度/相对密度(水=1):1.13g/cm3
闪点: 138℃(闭杯)
粘度(mPa.s):2.71(25°℃)50%水溶液
蒸汽压(kPa):20℃时1Pa
饱和蒸气压(kPa):0.21(84.5°C)
蒸汽相对密度(空气=1): 2.45
辛醇、水分配系数的对数值: -1.65~-0.67
临界压力(MPa):5.73
自燃温度(℃):424℃
爆炸上限%(V/V):20.6
爆炸下限%(V/V):2.7
水溶性:25℃时204g/100mL
溶解性:溶于水、乙醇、乙醚、丙酮,不溶于苯、已烷
化学性质
由于-C=ONH2和C=C的存在,使得丙烯酰胺的化学性质很活泼,容易进行加成、还原、水解、共聚等反应。
1、加成反应
与羟基化合物的加成反应:在碱性条件下,丙烯酰胺可以与羟基化合物发生加成反应,生成醚。例如,丙烯酰胺与乙醇在碱性条件下反应生成醚。
与胺的加成反应:丙烯酰胺可以与伯胺、仲胺和叔胺发生加成反应,生成一元加成物、二元加成物或季铵盐。例如,丙烯酰胺与胺反应生成亚胺。
与无机化合物的加成反应:丙烯酰胺可以与亚硫酸钠、亚硫酸氢钠、氯化氢、溴化氢等无机化合物发生加成反应。
聚合反应 丙烯酰胺聚合反应是指将丙烯酰胺单体通过化学反应聚合成聚丙烯酰胺的过程。丙烯酰胺聚合反应主要分为自由基聚合和离子聚合两种类型。

2、还原反应
通过还原剂将丙烯酰胺中的碳氧键还原成其他化合物。常见的还原剂包括碱金属和金属氢化物,例如钠、钾、氢化铝锂等。
3、水解反应
在酸性或碱性条件下,丙烯酰胺分子中的酰胺键断裂,生成相应的羧酸和氨(NH3)的反应。反应方程式如下:丙烯酰胺+水 →丙烯酸+胺化合物。丙烯酰胺的水解反应受多种因素影响:
温度:提高温度可以加速水解反应的速率。
pH值:酸性条件下,水解速率随pH降低而加快;碱性条件下,氢氧化钠的浓度和pH值对反应速率有显著影响。
催化剂:在某些情况下,可以使用催化剂来加速水解反应。
4、共聚反应
丙烯酰胺的共聚反应通常在引发剂的作用下进行18。引发剂分解产生自由基,这些自由基与丙烯酰胺单体反应,打开单体分子中的双键,形成活性中心。活性中心不断与其他单体分子结合,进行链增长反应,最终形成高分子量的聚合物。不同的聚合方法和反应条件会影响聚合物的分子量和结构。
丙烯酰胺的共聚反应类型
无规共聚:单体在聚合过程中无规律地插入到大分子链中,形成无规共聚物。
交替共聚:单体以1:1的比例交替插入到大分子链中,形成交替共聚物。
嵌段共聚:单体按一定的顺序连接形成嵌段共聚物。
接枝共聚:一个单体为主链,另一个单体作为侧链接枝到主链上,形成接枝共聚物。
合成方法
世界上工业化生产丙烯酰胺,无论是化学法(硫酸水和法、催化水和法),还是生化法,均采用丙烯腈原料,在一定的温度、压力和催化剂存在条件下,与水进行水合反应生产丙烯酰胺。
化学法的主要特点是技术成熟、产品质量较好,环境污染少,生产成本低,但生产过程较为复杂,操作难度较大。
生化法工艺技术采用特制的生物酶做催化剂,具有较高的催化活性、较高选择性和较高产品收率的特点,产品中消除了铜离子等对聚合有害的杂质,被认为是丙烯酰胺第三代生产工艺技术。15
生物法生产丙烯酰胺,因腈水合酶(NHase)具有催化效率高、反应条件温和、产物品质高、环境友好等优点,作为第三代工业化生产丙烯酰胺技术已替代铜系催化剂催化水合法,且当前业内此法生产技术已较为成熟。41
序号 | 厂商名称 | 建设规模(10't/a) | 技术来源 | 备注 |
1 | 山东宝莫生物化工有限公司 | 2.5 | 上海生化所 | 自用 |
2 | 新多效胜化工有限公司 | 2.4 | 中科院 | 外销 |
3 | 新多市新昌化工有限公司 | 0.6 | 中科院 | 外销 |
4 | 江西昌九农科中科院 | 3.0 | 上海生化所 | 外销 |
5 | 大庆炼化公司 | 1.6 | 上海生化所 | 自用 |
6 | 北京恒聚化工集团有限公司 | 2.0 | 上海生化所 | 自用 |
检测方法
丙烯酰胺的常用检测方法主要有:气相色谱法19、液相色谱法20、电化学法21、光谱法22、液相色谱-质谱联用法23、气相色谱-质谱联用法24、离子排斥色谱法(IEC) 25和酶联免疫吸附法(ELISA)26。
其中,离子色谱作为高效液相色谱的一个重要发展分支,具有分析速度快、多离子同时分析、灵敏度高、选择性好等优点而被广泛应用于水质分析、食品分析、环境分析等领域。27
酶联免疫吸附法(ELISA)则是一种比较新型、快速、可靠和高通量的分析方法,可替代食品和环境痕量分析中使用的仪器方法,满足筛选方法的性能和验证标准,已用于检测许多食品和环境有毒污染物。
相关标准
 AM相关的国际标准及国家标准(右图),目前唯一涉及AM检测的ISO标准是ISO 18862:2016《咖啡和咖啡制品丙烯酰胺的测定衍生后使用HPLC-MS/MS和GC-MS法》,由ISO食品技术委员会归口制订。28
AM相关的国际标准及国家标准(右图),目前唯一涉及AM检测的ISO标准是ISO 18862:2016《咖啡和咖啡制品丙烯酰胺的测定衍生后使用HPLC-MS/MS和GC-MS法》,由ISO食品技术委员会归口制订。28
另外15项标准皆是国家标准(GB),其中GBZ表示职业卫生标准。在15项国家标准中,有6项强制性标准,9项推荐性标准。按照中华人民共和国食品安全法(2018修正)第二十五条的规定:食品安全标准是强制执行的标准,除食品安全标准外,不得制定其他食品强制性标准。因此,食品安全标准是强制执行的标准。
用途
丙烯酰胺为丙烯酰胺系中最重要及最简单的一种,用途十分广泛,用作有机合成的原料及高分子材料的原料。以下是一些具体的应用领域:
工业领域:丙烯酰胺可用于生产聚丙烯酰胺,聚丙烯酰胺是一种高分子聚合物,具有很好的絮凝、增稠、降阻等性能,广泛应用于水处理、石油开采、纺织等领域。
用作土壤改良剂时,可增加土壤的水渗透性和保湿性;
用于土木工程的隧道开掘、油井钻探、矿井和水坝等工程的堵漏;
用作纤维改性剂,可改善合成纤维的物性;
用作防腐剂,可用于地下构件的防腐;
用于食品工业的添加剂、颜料的分散剂、印染糊剂。
与酚醛树脂溶液配合,可制成玻璃纤维的粘合剂,与橡胶一起可制成压敏性粘合胶等。
与乙酸乙烯、苯乙烯、氯乙烯、 丙烯腈等单体聚合,可制备许多合成材料。
生活领域:丙烯酰胺及其衍生物可用于制备各种日用化学品,如洗发水、护发素、化妆品等,赋予这些产品良好的性能。
健康影响
代谢与膳食
AM是一个具有亲电基团的有机小分子,水溶性强,可通过皮肤、黏膜、呼吸道、胃肠道等进入体内。 食物中的AM通过肠道完整的吸收,而环境中暴露的AM约25%被皮肤吸收。 吸收后的AM通过血液循环系统广泛分布于体内各个组织,并在此过程中对机体造成损害。29
代谢与吸收
研究表明,在摄入低剂量AM的情况下,约50%会转化成GA, 而高剂量的AM则大部分与GSH反应,约13%转化成GA。代谢生成的AAMA、GAMA、异GAMA和1,2-二羟基丙酰胺均随尿液排出,而在尿液中检出的时间顺序及含量不同,如:AM摄入2h后即可检测出本身和AAMA;由于AM向GA转化过程中需要时间,所以4h后才检出GAMA 和异GAMA。29
AAMA和GAMA在人体内通常48h后完全排出体外,总尿液中AAMA占总AM的51%,是AM的主要代谢产物;GAMA和异GAMA占总AM的5%,是AM的次要代谢产物,其中异GAMA的含量远小于GAMA。生成的GAMA等在排出前的代谢过程是否对肌体造成毒害未见报道。29
日膳食暴露评估
经口摄入被认为人体吸收AM最迅速、 完整及主要的途径,一些研究根据不同地区食品中AM的含量来评估该地区普通人群AM的摄入量。29
2011年FAO/WHO食品添加剂联合专家委员会(Joint FAO/WHO Expert Committee on Food Additives,JECFA)对除非洲以外世界范围内8个代表国家中丙烯酰胺膳食摄入量进行评估,结果表明普通人群的日摄入量平均约为1μg/(kg bw·d),最高摄入量约为4μg/(kg bw·d)。由于不同国家烹饪、饮食习惯的不同,各国的摄入量有所差异。英国最新公布的日摄入量为0.61μg/(kg bw·d),法国为0.43μg/(kg bw·d),而中国在最新膳食研究中得出的摄入量为0.319 μg/(kg bw·d),仍显著低于世界的平均水平,这与我国传统的食品加工工艺(低于100 ℃的蒸煮加工)和近年来饮食习惯略有改变有很大关系。29
有学者基于生理学的毒素代谢动力学模式和非线性剂量反应法确定丙烯酰胺的神经毒性日摄入边际剂量为40 μg/(kg bw·d),丙烯酰胺日致癌边际剂量为2.6 μg/(kg bw·d)。29
毒性机制
丙烯酰胺的毒性主要包括神经毒性、 生殖毒性、遗传毒性、免疫毒性及潜在致癌性,在人体中得到证实的是神经毒性。29
神经毒性
许多研究表明丙烯酰胺具有显著的神经毒性, 在人类的职业暴露以及动物实验中均有明确证据: 我国自20 世纪70年代开始报道AM的中毒病例,尤其在职业暴露上屡见不鲜。研究发现AM中毒者主要的症状体征为皮肤脱皮红斑、四肢麻木、手足多汗、体重减轻及远端触痛觉减退、深反射减退等神经功能受损的症状;而猫、大鼠、小鼠、豚鼠、兔和猴等实验动物暴露AM后则会表现出共济失调、后肢足呈八字、骨骼肌无力,并最终导致运动障碍。近年研究表明,AM诱导神经毒性的可能机制如下:29
氧化损伤与神经细胞凋亡调控
研究表明,活性氧族(reactive oxygen species,ROS)对细胞膜脂质、蛋白质和DNA不断攻击并造成相应靶分子累积氧化变性或损伤,是造成细胞代谢紊乱和功能异常的重要生理基础。当体内自由基和活性氧的产生与消除间不平衡时会产生氧化应激,从而引发许多疾病。中枢神经系统(central nervous system, CNS) 是机体氧代谢较活跃的部位,其抗氧化酶活性低于其他组织,这使之易成为氧化损伤的主要靶器官。AM可能会通过诱导和影响氧化应激来引起神经损伤。同时,AM刺激也会激活细胞中的免疫通路并对产生的氧化应激进行防御。29
另外,共轭α-β不饱和羰基衍生物,如丙烯醛(acrolein)和4-羟基-2-壬烯醛(4-hydroxy-2-nonenal)等一类属于II型烯烃, 研究表明这种II型烯烃可能与内源性产生的不饱和醛协同作用,从而加大细胞损伤,加速了在涉及氧化应激的急性神经损伤(如脊髓创伤)和某些慢性神经疾病如阿尔兹海默症(Alzheimer disease,AD)、帕金森综合征(Parkinson’s syndrome,PD)等的过程。 而AM在结构上也属于共轭α-β不饱和羰基衍生物。氧化应激可能是AM造成神经毒性,从而引发神经性疾病的一个主要机制。29
血脑屏障功能损害
血脑脊液屏障(blood-cerebrospinal fluid barrier)主要由脉络丛(choroidplexus)上皮细胞之间的紧密连接构成,负责血液和脑脊液之间的物质转运。完整的血脑脊液屏障是保证中枢神经系统内环境稳定的重要条件。有学者发现鼠腹腔注射AM后脑脊液中甲状腺水平下降,瘦素(leptin,LP)转运水平被抑制,LP水平降低。由于瘦素具有促进大脑生长发育,降低促凋亡因子水平的作用,因此AM诱导的神经细胞凋亡也有可能是因血脑屏障中 LP水平的降低引起的。另外,AM还会造成紧密连接相关蛋白(zonula occludens-1,ZO-1)表达减少,屏障通透性增加,从而容易引起血清蛋白或其它神经毒物即可进入脑组织中,使神经系统的代谢及功能发生紊乱。29
能量代谢障碍
有学者采用酶分析法发现AM染毒后大鼠脑组织匀浆中ATP合成酶活力下降,ATP水平明显降低,ADP和AMP增加,肌酸激酶(Creatine Kinase,CK)活力明显受到抑制,由于CK是轴突运输上的一个重要组成,因此推测能量代谢障碍可能是AM产生神经元损伤、神经病变的生化基础。29
神经递质的改变与抑制
AM也可能通过改变神经递质水平和功能导致神经毒性,如阻碍神经末梢的膜融合过程。 N-乙基顺丁烯二酰亚胺敏感性的融合蛋白(N-ethylmaleimide sensitive factor,NSF)是参与神经递质释放的一种ATP酶。29
研究表明NSF可能是A的靶位点,在神经递质传递过程中AM与NSF蛋白264位甲硫氨酸位点(NSF Cys264)形成加合物来抑制突触小体对神经递质的释放, 阻碍神经末梢膜融合,最终导致神经末梢变性;同时,AM 还会导致纹状体多巴胺的含量显著降低, 突触囊泡对多巴胺的摄取能力减弱,导致神经递质的存储障碍,进而也会引发递质的释放障碍。29
来源: 百度百科
内容资源由项目单位提供


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 百度百科
百度百科 