两性氧化物(Amphoteric Oxide)两性氧化物是指遇强酸呈碱性,遇强碱呈酸性的氧化物,既能与酸作用,又能与碱作用。都生成盐和水。两性元素的氧化物和变价金属的中间价态的氧化物通常是两性氧化物。
例如氧化锌ZnO能与盐酸作用生成氯化锌ZnCl2和水,又能与氢氧化钠作用生成锌酸钠Na2ZnO2和水,除氧化锌还有氧化铝等。1
两性氧化物的组成
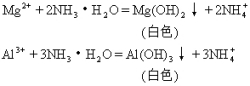 主要由活动性较低的金属的氧化物组成。
主要由活动性较低的金属的氧化物组成。
两性氧化物有BeO、Al2O3、Cr2O3、ZnO等。
两性氧化物的特点
1、两性氧化物属于两性化合物,它们既能跟酸反应,又能跟碱反应。
2、典型的两性氧化物有Al2O3、ZnO和有些过渡元素中间价态的氧化物(如Cr2O3、Mn2O3),它们都表现两性。
一些示例
-
氧化铝:
-
与酸:Al2O3 + 6HCl = 2AlCl3 + 3H2O
-
与碱:Al2O3 + 2NaOH = 2NaAlO2+H2O
-
氧化铅
-
与酸:PbO + 2HCl = PbCl2 + H2O
-
与碱:PbO + Ca(OH)2 = CaPbO2+H2O
-
氧化锌
-
与酸:ZnO + 2HCl = ZnCl2 + H2O
-
与碱:ZnO + 2NaOH = Na2ZnO2+H2O
Be、Ti、V、Fe、Co、Zn、Ge、Zr、Ag、Sn、Au、Mn等元素可生成两性氧化物。
两性氧化物的“两性”也可以理解为既能表现酸性氧化物的性质,又能表现碱性氧化物的性质。有时我们也把既能表现氧化性.又能表现还原性的物质也叫“两性”物质。
除以上氧化物外,还有一种氧化物如CO、NO等,它们和酸、碱和水不起反应。这类氧化物叫做不成盐氧化物或惰性氧化物。
特别提醒:SiO2不是两性氧化物,SiO2能同时与HF/NaOH反应,但它是酸性氧化物。
来源: 百度百科
内容资源由项目单位提供


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 百度百科
百度百科 