我们知道,生物多样性监测是生物多样性保护的基础。许多传统方法,如实地观察、陷阱监测(如相机捕捉和坑道陷阱)等,虽然在一些特定环境下仍然有效,但它们通常需要大量的时间和资源,且难以覆盖广泛的地区或进行频繁的监测。随着物种保护工作的推进,科学家们亟需开发一种更快速、高效、可扩展的监测工具,以便实时评估物种的分布和种群动态,及时发现物种衰退的迹象,并为保护决策提供科学依据。eDNA技术作为一种这样的工具,将在陆生脊椎动物监测中发挥越来越重要的作用。“海洋与湿地”(OceanWetlands)小编注意到,2025年1月20日,来自澳大利亚科廷大学的Joshua P. Newton等研究人员在《环境DNA》期刊上发表了一项关于环境DNA(eDNA)在陆生脊椎动物监测中的应用研究。这项研究综述了eDNA在陆地生态系统中的应用趋势,探讨了采样方法的最佳实践,并总结了陆生脊椎动物监测过程中面临的主要挑战。随着全球范围内陆生脊椎动物种群的急剧下降和灭绝,如何有效保护这些物种成为全球生物多样性保护面临的重大挑战。为应对这一问题,传统的物种监测方法需要得到改进和补充。传统的监测方法,如直接观察和使用陷阱设备(如相机捕捉和坑道陷阱),在一些环境下仍然发挥着重要作用,但其数据获取周期长、工作强度大且受限于环境条件,难以满足快速、持续监测的需求。因此,开发新的监测技术显得尤为迫切。eDNA技术,作为一种新兴的生物监测手段,近年来在水生物种监测中取得了显著进展。eDNA是从环境中提取的DNA,不需要直接接触或观察目标物种即可获得其遗传信息。这一技术不仅为水生物种的监测提供了新方法,也逐渐应用于陆生脊椎动物的监测中。环境DNA技术的优势在于其高效性和无创性,能够在不干扰生态系统的前提下,快速获得物种分布和种群动态信息。利用实时定量PCR(qPCR)和液滴数字PCR(ddPCR)等技术,研究人员能够检测到隐秘物种、稀有物种及受威胁物种的存在,并通过高通量DNA测序技术和DNA条形码技术进行大规模的物种鉴定和多样性评估。

这张图片通过四个案例展示了环境DNA(eDNA)技术在陆生脊椎动物监测和生物多样性影响评估中的应用潜力:(a)通过土壤eDNA监测哺乳动物,(b)通过水体eDNA监测两栖动物,(c)通过空气eDNA监测鸟类,(d)通过特定环境介质监测爬行动物。这些案例表明,eDNA技术是一种高效、非侵入性的监测工具,能够用于评估陆生脊椎动物的生物多样性和环境影响。图片分别来源于Newton et al. (2022)、Piaggio et al. (2014)、van Beeck Calkoen et al. (2019)和Von Duyke et al. (2023),(CC BY-SA 4.0)
但是,将eDNA技术应用于陆生脊椎动物的监测依然面临诸多挑战。这些挑战主要源于陆地生态系统中eDNA的生态特性。与水生环境不同,陆地环境中的eDNA更容易受到降解、污染及物理环境变化的影响,从而影响其在采样过程中的稳定性和可靠性。因此,如何开发出适用于陆地生态系统的eDNA采样方法,成为目前研究的重点。通过对2012至2023年间143篇相关研究文献的回顾,研究人员发现,随着eDNA技术的不断发展,陆生脊椎动物的监测研究数量逐年增加。尤其是近年来,随着技术的进步和应用领域的扩展,越来越多的研究聚焦于温带森林等特定生态系统中的陆生哺乳动物。同时,研究人员发现,eDNA技术在监测陆生脊椎动物时,已逐渐从传统的物种检测扩展到动物行为学和种群遗传学等新兴领域。不过,尽管eDNA技术的应用前景广阔,陆生脊椎动物监测中的采样方法仍然缺乏统一标准。根据现有研究,eDNA采样的策略和方法存在较大差异。研究人员总结了三种主要的采样策略,包括空气采样、土壤采样和水源采样;同时,针对不同的生态环境和物种需求,采用的采样基质也不尽相同,如植物残体、泥土和沙土等。在样本的保存方面,研究中提到的保存方法包括冷冻、冷藏和化学固定等多种技术,以确保DNA样本的稳定性。
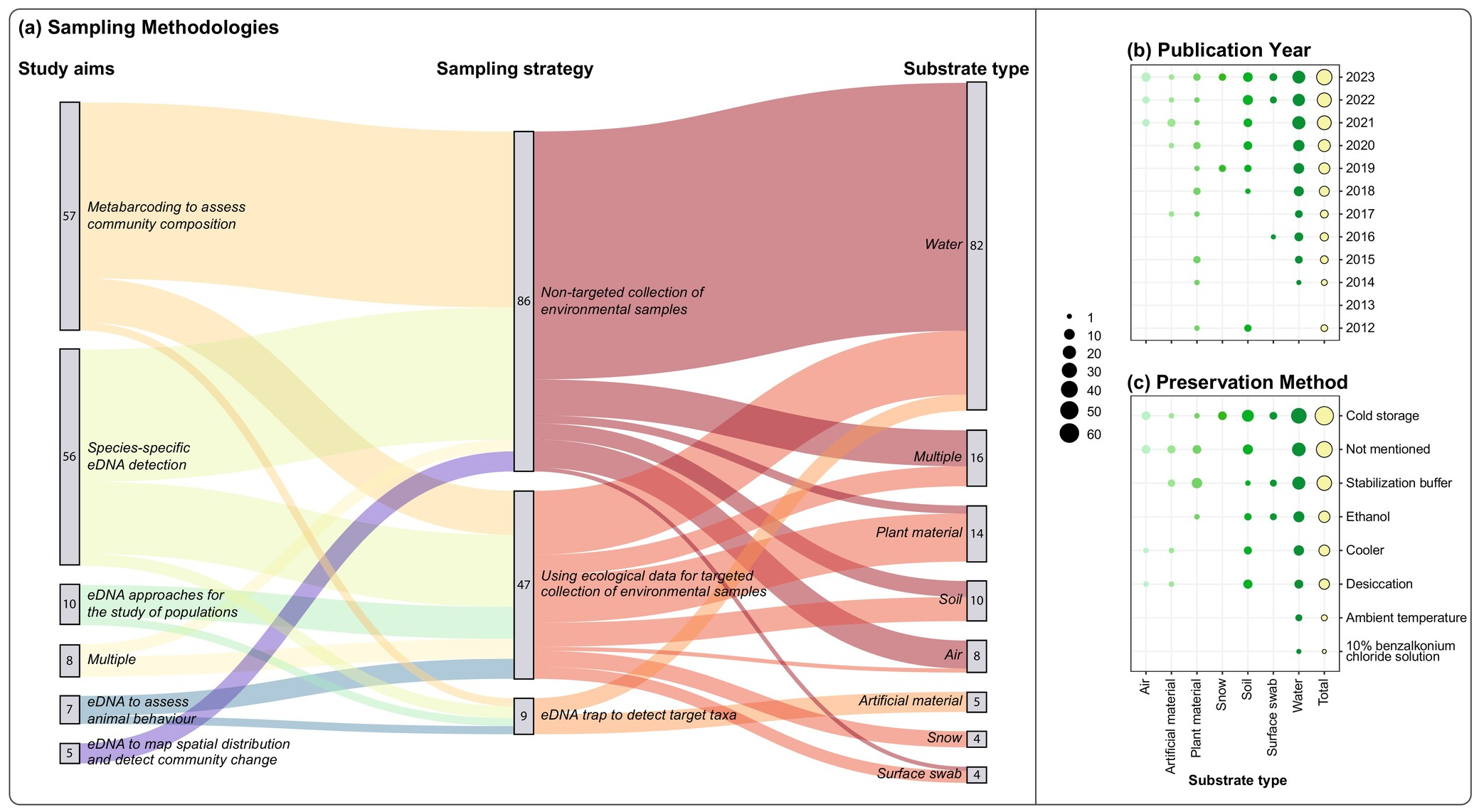
上面这张图片通过冲积图和气泡图,概括展示了2012~2023年间陆生脊椎动物(不含两栖动物)eDNA研究的综合分析,揭示了研究目标、采样策略、基质类型、年份趋势以及保存方法等关键信息,反映了该领域的研究特点和技术应用。全面展示了2012至2023年间陆生脊椎动物(不包括两栖动物)eDNA研究的综合分析:(a):冲积图(alluvial plot)汇总了研究目标、采样策略和基质类型,清晰地展示了不同因素之间的关联。(b):气泡图显示了各年份研究中不同基质类型的使用比例,揭示了研究趋势的时间变化。(c):气泡图展示了不同保存方法在研究中的应用比例,突出了常用的保存技术。图源:Newton J P, Allentoft M E, Bateman P W, et al. (2025)
研究人员指出,尽管目前已有一些采样方法,但由于陆地生态系统的多样性和eDNA降解速度的复杂性,尚未形成“一刀切”的标准采样方法。为了推动eDNA技术在陆地生态系统中的应用,未来的研究需要更加深入地探讨不同环境条件和目标物种对eDNA检测的影响。特别是在选择采样地点、采样时间、采样频率以及样本保存等方面,研究人员需根据物种的生态需求进行灵活调整。
在这项研究中,研究团队通过文献回顾的方法,系统性地总结了环境DNA(eDNA)技术在陆生脊椎动物监测中的应用。研究的主要目标是深入分析当前陆生脊椎动物eDNA研究中的采样策略、使用的基质类型、污染控制方法等多个方面。为确保研究的全面性,团队专门限制了研究对象的范围,仅涉及“陆生有胎盘四足动物”,即排除了两栖类(如青蛙)物种,因其在幼虫期和成体期的生态特征使其与陆生环境的联系复杂,且其皮肤的高渗透性可能导致eDNA沉积速率与其他脊椎动物不同,这需要进一步单独探讨。研究团队在2024年1月进行了文献检索,搜索了2012年至2023年间,使用“环境DNA”或相关关键词的同行评审论文。通过这一检索方法,他们共发现了2682篇潜在相关文献,并根据研究内容、目标物种、研究方法等因素对这些文献进行了筛选。最终,留下了143篇专注于陆生脊椎动物eDNA研究的论文。这些文献涉及了全球各大洲和不同的生态环境,为本研究提供了丰富的样本和数据来源。为了对现有文献进行系统化分析,研究团队记录了每篇论文的多个关键信息,包括研究的物种、研究所在的国家与生态区域、采样策略、所采样的基质类型、减少污染的策略、使用的负对照方法、样本保存方法等。所有这些数据都被整理到统一的数据库中,并通过统计分析软件R进行数据可视化处理,以便更清晰地展示不同采样方法和生态区域的研究趋势。研究团队特别关注了三类采样策略:第一类是非针对性的环境基质采样,即通过收集环境样本来检测物种多样性,常见的如从河流中收集水样来监测陆生哺乳动物;第二类是使用专门设计的eDNA陷阱,这些陷阱用于捕获特定物种的DNA,如“纸衬巢管”用于检测树栖哺乳动物;第三类是基于生态数据的针对性采样,这种方法通过了解动物的行为或微生境,选择性采集环境样本,如在寻找爬行动物时采集覆盖物样本,或在寻找吸蜜物种时采集花朵样本。非针对性的环境基质采样是目前最为常用的采样策略,占所有研究的60%。研究人员还分析了不同基质的使用情况。水是最常见的采样基质,约66%的研究选择了水样作为采集对象,这一趋势反映了水生环境对陆生物种的生物多样性的重要性。此外,土壤和植物样本也在一部分研究中得到应用,而一些新兴研究则探索了空气和表面等新型基质。尽管如此,水仍是最受欢迎的基质类型,因为它不仅在水生环境中应用广泛,也在许多陆生生态系统中起着关键作用。为了确保采样结果的准确性,该研究团队还特别关注了采样过程中的污染控制问题。研究发现,约74%的研究专门考虑了采样设备的去污问题。常见的去污方法包括使用漂白水、紫外线灭菌、火焰灭菌等,而使用一次性产品减少污染的策略也在多个研究中得到应用。此外,尽管大多数研究都会在实验室阶段使用负对照样本,但只有43%的研究在田野采样时使用了现场负对照样本。负对照样本能够有效检测采样过程中的潜在污染源,保证采样结果的可靠性。

巨板蜥(学名:Broadleysaurus major),又称苏丹盾甲蜴,属于大盾甲蜥科,是一种生活在非洲的蜥蜴。它的分布范围涵盖了埃塞俄比亚、坦桑尼亚、多哥、马拉维、南非等非洲地区。它们主要栖息于非洲的干旱地区,体色通常为暗深的棕色或灰色,与其所处的环境相协调,有助于伪装和隐蔽。摄影:Linda©绿会融媒·“海洋与湿地”(OceanWetlands)工作组
eDNA技术在陆生脊椎动物物种监测和研究中展示了巨大的应用潜力,但在实际应用过程中,仍面临着许多挑战。尤其是对于物种缺失的解读问题,仍然是eDNA研究中的一个长期难题。影响这一问题的因素包括采样策略和目标物种的选择,比如样本的数量与采样地点、环境条件、生物量以及DNA脱落速率等,这些因素均可能对物种的检测概率产生影响。因此,尽管eDNA技术在物种监测方面具有显著优势,但数据解读仍需谨慎。这一挑战并非eDNA独有,所有监测数据的解读都应保持警惕和审慎。
随着技术不断发展,许多技术性采样问题有望得到解决或显著减少。为此,科学家们正在设计便捷的采样设备,比如Smith-Root eDNA采样器,能够优化采样速度并提高重复性,同时减少污染问题。除此之外,3D打印采样器和自动化采样技术也在水域研究中取得了一定应用,并正在陆地研究中进行测试。目前,研究人员正尝试以空气作为DNA载体,进行eDNA的采集,这一创新为样本采集的可及性和规模提供了新的可能。结合移动实验室、实时PCR热循环仪以及基因测序技术,这些新型工具为生物多样性评估和入侵物种检测提供了更加高效的手段。例如,Smith-Root eDNA采样器与移动DNA提取设备结合,可以在一个小时内完成水域入侵物种的eDNA采样与检测,这种便携式工具极大提高了入侵物种检测的响应速度。通过这种技术,管理者能够在物种入侵被发现后,迅速采取相应的管理措施,及时应对环境变化。
但尽管这些技术能够在现场有效识别物种,特别是在偏远地区或者急需数据的情况下,它们也存在一定的局限性。当前,这些创新方法主要应用于水样或空气样本采集,而在其他基质类型中,仍然面临技术上的限制。例如,对于需要复杂组织裂解或提取技术才能分离遗传物质的情况,便携式技术的应用将受到限制。相比之下,水或空气样本由于不需要复杂的组织裂解,或者可以通过便携设备如物理粉碎进行处理,能够更容易地适配便携式实验室技术。该研究团队指出,现有的研究表明,在eDNA采样策略、目标基质和样本保存方法的选择上,并没有一种适用于所有情况的“万能法则”。这一现象反映了研究领域的多样性、研究问题的复杂性以及技术进步的迅速发展。虽然eDNA技术在陆生脊椎动物物种监测中的应用潜力非常巨大,但科研人员始终强调,技术的运用应当服务于科学问题的解决,而非单纯追求技术本身。真正的挑战在于,如何在适当的时机和条件下运用eDNA技术,并与传统的监测手段,如目视观察、捕捉及声学调查等方法相结合,从而为物种监测提供更加全面、准确的方案。
海湿·小百科
“纸衬巢管”(paper-lined nest tubes)是一种巧妙设计的生态监测工具,它模拟了天然树洞,为树栖哺乳动物提供了一个安全舒适的“家”。这种巢管内部巧妙地铺设了纸张,就像是为小动物们准备的“留言板”。当松鼠、鼯鼠或其他树栖动物进入巢管时,它们会留下毛发、粪便,甚至爪印等“蛛丝马迹”。这些痕迹都被纸张忠实地记录下来。所以,科学家们只需定期回收这些带有痕迹的纸张,就可以通过DNA分析或其他方法,轻松识别出哪些物种曾到访过巢管。通过长期监测,科学家们不仅能掌握这些树栖动物的种类、数量和分布情况,还能深入了解它们的活动规律和生态习性。这种方法既不会伤害野生动物、又能收集到宝贵的信息,堪称生态研究的“侦察兵”。采样策略(Sampling Strategy)是指在环境DNA(eDNA)研究中,研究人员根据研究目标和物种特性,设计和选择的样本收集方法。具体而言,采样策略决定了如何、何时以及在何种条件下采集环境样本,以最大限度地提高DNA的检测灵敏度和准确性。常见的采样策略包括非针对性采样、定向采样和使用eDNA陷阱。非针对性采样通常指随机收集环境中的样本,如水体、土壤或植物表面等,适用于广泛的物种多样性研究。定向采样则是依据物种的生态行为、栖息地特征或季节性活动来有针对性地选择采样点,从而提高目标物种的DNA检测率。此外,eDNA陷阱是一种专门设计的工具,通过模拟或诱导特定物种的栖息行为,如在树洞中安放纸质巢管来捕捉树栖哺乳动物的DNA。选择合适的采样策略,不仅能确保采集到足够的DNA信息,还能有效减少污染和环境干扰,提高eDNA监测的科学性和可重复性。
eDNA陷阱,顾名思义,就是捕捉环境DNA的“陷阱”。它是一种专门设计用于收集水体或其他环境中生物体释放的DNA片段(eDNA)的工具。这些DNA片段可能来自生物体的脱落细胞、排泄物或黏液等,漂浮在环境中,就像是生物留下的“足迹”。eDNA陷阱在提升检测灵敏度、减少环境污染干扰、以及降低对物种栖息地的干扰方面具有重要优势,尤其适用于难以观察和研究的动物或栖息环境。科学家们通过使用eDNA陷阱,能够更高效、更灵敏地检测特定物种的存在,甚至可以发现那些稀有或难以捕捉的生物。这种方法不仅是非侵入性的,对生物无害,而且成本效益高,在生物多样性监测、入侵物种检测和濒危物种保护等领域具有广泛的应用前景。负对照(Negative Control)是科学实验中用于验证实验结果是否受到外部污染或其他不相关因素干扰的一种重要控制手段。在环境DNA(eDNA)研究中,负对照通常指在采样过程中,不涉及目标物种的样本,用于检测是否存在任何来自环境、设备或操作过程中的DNA污染。负对照的设置可以帮助研究人员确认实验中观察到的DNA信号是否真正来源于目标物种,而不是外界污染的结果。在eDNA采样中,负对照可以分为两类:场地负对照和设备负对照。场地负对照是在采样地点使用与实际样本相同的采样设备和方法,但采样时避免接触目标物种的DNA,通常会在已知目标物种不在现场的区域收集样本;设备负对照则是通过对采样设备本身进行清洁和检测,确保设备在使用前没有残留的DNA。研究人员用这些负对照的设置,就能够比较有效的确保采集的DNA数据的准确性和可靠性,有效排除外部污染对研究结果的影响。例子1:在一项研究中,采用了负对照来检测水样中是否存在外部污染物。他们在研究佛罗里达州的入侵物种——缅甸蟒(Burmese python)的环境DNA时,使用了负对照来确认其采集的水样中是否有来自其他物种的DNA污染。在这项研究中,场地负对照样本是从不涉及目标物种的水域采集的,目的是确保采样过程没有污染源。结果显示,通过负对照分析,研究人员能够确保所有检测到的DNA信号都确实来自缅甸蟒,而非外部环境污染。例子2:另外一个研究中,研究团队对采集水样的设备进行消毒处理,并在每次采样前后都进行了设备负对照。具体来说,他们在每次使用设备之前,先收集一个不含目标物种DNA的空白水样,用来检测是否存在来自设备的污染。通过设备负对照,他们能够排除设备本身可能存在的污染干扰,确保水样中的eDNA确实来源于目标物种。
海湿声明: 1.本文仅代表资讯,不代表平台观点。供参考。2. 因本平台斜体字拷贝至外部平台时常出现内容丢失的情况,
信息源 | Newton J P, Allentoft M E, Bateman P W, et al. (2025)
编译 | 王芊佳
编辑 | Maggie
排版 | 绿叶
参考资料略
来源: 海洋与湿地





 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 中国绿发会
中国绿发会 