最初出现轻微运动障碍,跑步、跳跃等动作变得吃力,后期逐渐出现无法行走、肢体无法正常抬起,需要借助轮椅行动,最终可能因呼吸衰竭或心力衰竭而死亡……
这段话描述描写的是杜氏肌营养不良症患者的一生。杜氏肌营养不良症(Duchenne Muscular Dystrophy, DMD),简称DMD,是一种严重的遗传性神经肌肉病,也是十分常见的致死性遗传病之一。
遗憾的是,这个疾病目前“无药可医”。
近日,浙江科学家,来自西湖大学的研究团队在该疾病的核心蛋白研究方面有了新突破。
北京时间2024年12月11日,西湖大学、西湖实验室吴建平团队联合闫浈团队在Nature在线发表题为“Structure and assembly of the dystrophin glycoprotein complex”的论文。该团队首次“看清”了肌营养不良症的核心蛋白,揭开了肌营养不良蛋白糖蛋白复合体(Dystrophin Glycoprotein Complex, DGC)的神秘面纱,展示了其独特的结构特征。

| 论文截图
此项研究填补了该领域近三十年的重要空白。这一发现为理解肌营养不良症的发病机制提供了全新的见解。
什么是肌营养不良症(DMD)?
据统计,目前全球有三亿多罕见病病人,中国现有各类罕见病患者2000余万人。DMD就是罕见病的其中一种。
1986年美国科学家发现,DMD的致病原因,是由dystrophine基因的缺陷所导致。由于这个DMD基因位于X染色体上,故DMD绝大多数仅发生于男孩,发病率约为每3500名男孩中有1例。
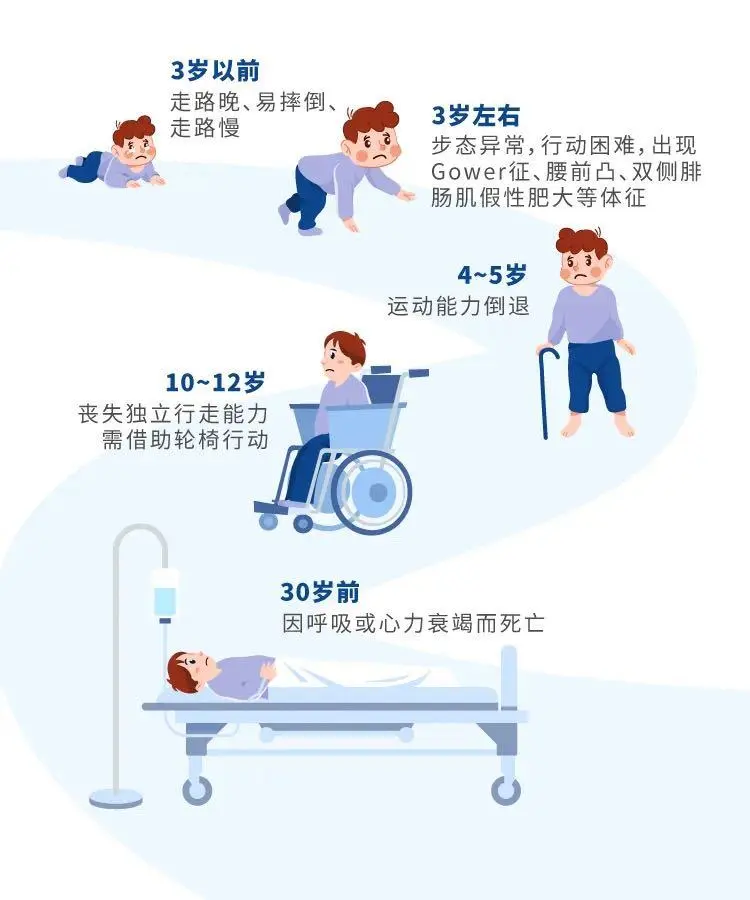
| DMD临床表现 图源:西湖大学
DMD患者会发生进行性骨骼肌无力和退化,致死率高。他们常在 3~5岁时出现运动迟缓、步态异常、站立困难等症状,随着年龄的增长而逐渐恶化,约12岁时就需要依赖轮椅出行,20岁左右可能因心肺功能衰竭而死亡。
因为该疾病仍旧无法被治愈,寻找安全有效的治疗手段一直是该领域研究中的终极目标。
这种核心蛋白
导致了DMD?
本次研究的其中一个主角,是一个名为Dystrophin的蛋白,全称肌营养不良蛋白。它是一种重要的细胞骨架蛋白,主要存在于骨骼肌和心肌细胞中,对维持肌肉细胞的结构和功能起着至关重要的作用。
当Dystrophin在体内与多个蛋白相互作用,就形成了DGC复合体。这个复合体主要分布在肌肉组织和神经系统。肌营养不良症,就与这个蛋白复合体上的突变有关。
如果说,肌肉细胞是一栋高楼大厦,那么DGC复合体既是大厦的“减震器”,也是“通讯设备”,它是连接细胞内外的纽带,l可以吸收和分散肌肉收缩时产生的机械力,进而帮助保护和维持肌肉细胞膜的完整性和稳定性。同时,DGC复合体也具备信号传导的作用,影响细胞的生长、分化和存活。
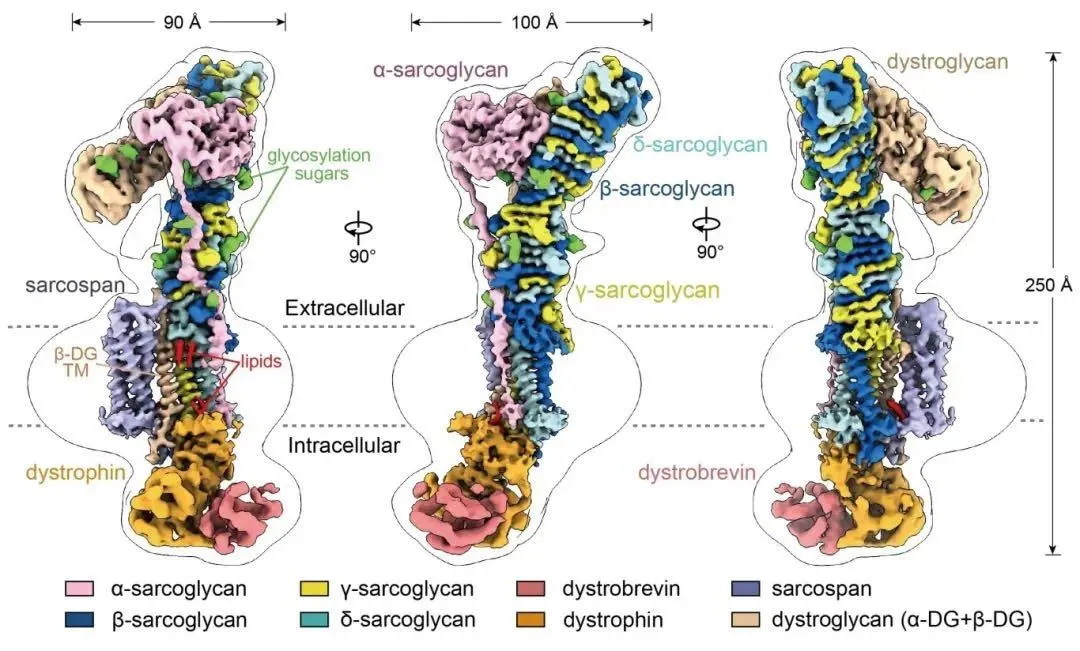
| 骨骼肌内源DGC复合体高分辨结构电子密度图 图源:西湖大学
首次看清
核心蛋白的“真面目”
西湖大学生命科学学院吴建平团队和闫浈团队,成功从小鼠骨骼肌组织中分离出了天然内源性DGC复合体,并利用冷冻电镜技术解析了其高分辨率结构(分辨率3.2-3.5 Å)首次看清了这个复合体的全貌,填补了该领域近三十年的空白。
之后,研究团队回到疾病本身,研究了与肌营养不良症相关的致病突变位点在哪里。他们分析了过去几十年临床研究中积累的大量与肌营养不良症相关的突变位点数据,发现与肌营养不良症相关的致病突变大多分布于三个区域,这些特定区域对于DGC发挥正常功能具有重要作用,为相关肌营养不良症的致病机制提供了深入的见解。

| 研究团队 图源:西湖大学
从微观领域,开发基因治疗方案也有了新线索。目前针对DMD患者的治疗手段非常有限,一种通用策略是通过基因治疗来修补功能异常的肌营养不良蛋白。但是,这个蛋白的基因是人体最长的基因之一,完整递送如此长的基因去替换致病基因十分困难。
而来自西湖大学的研究成果,为设计更加合理有效的蛋白递送作出了重要参考。未来,这个结构所提供的重要线索,或许能为肌营养不良症的治疗带来新的希望。
(来源:潮新闻、西湖大学)
来源: 浙江省科学技术协会


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 浙江省科学技术协会
浙江省科学技术协会 
