
2024年诺贝尔生理或医学奖得主维克多·安布罗斯和加里·鲁弗肯
导读:今年的诺贝尔奖再次将聚光灯投向了生命科学领域,表彰了两位在基因调控基本原理方面有卓越发现的科学家——安布罗斯和鲁弗肯,他们发现了microRNA。
这一发现不仅揭示了生命体如何精准地控制基因表达,从而塑造出复杂多样的生物形态和功能,更为我们理解生命本质、探索疾病治疗的新途径提供了宝贵的线索。
深究科学 | 撰文
两位miRNA发现者被授予诺奖
10月7日北京时间,2024年诺贝尔生理或医学奖揭晓,奖项授予维克多·安布罗斯(Victor Ambros)和加里·鲁弗肯(Gary Ruvkun)两位学者,他们因发现微小核糖核酸(miRNA)及其在转录后基因调控中的作用而获奖。这一发现对于理解基因表达调控机制具有重要意义,也为疾病的治疗提供了新的思路。

事实上,遗传信息就像一本精密的剧本,从DNA转录成信使RNA(mRNA),再经由细胞内的蛋白质生产机器,将遗传指令转化为实实在在的蛋白质。这一过程,自20世纪中叶以来,已被多项基础科学发现所揭示。
然而,尽管所有细胞都携带着相同的DNA遗传信息,我们的器官和组织却由多种不同类型的细胞构成,它们各自表达着独特的蛋白质组合。这一奇妙的现象,正是基因活性调控的杰作。
基因活性调控确保了每个特定类型的细胞都能激活正确的基因集,从而执行其特定的功能。如肌肉细胞、肠细胞和不同类型的神经细胞,正是通过这一机制,才能各司其职,共同维持着生命体的正常运转。
此外,基因活性还需不断微调,以适应我们体内和外界环境的不断变化。一旦这一调控机制出现偏差,就可能引发严重的疾病,如癌症、糖尿病或自身免疫性疾病。因此,理解基因活性的调控机制,一直是数十年来科学研究的重要目标。
早在20世纪60年代,科学家就发现了一种名为转录因子的特殊蛋白质,它们能够结合到DNA的特定区域,通过决定哪些mRNA被生产出来,从而控制遗传信息的流动。自那时以来,科学家已经发现了数千种转录因子,并一度认为基因调控的主要原理已经得到解决。
然而,1993年安布罗斯和鲁弗肯发表了一项颠覆性的发现——miRNA,随即开启了一个全新的领域。当时安布罗斯和鲁弗肯对不同细胞类型如何发育充满了兴趣,在他们的不断努力何探索中,最终发现了miRNA。这是一种全新的miRNA分子类别,这些分子在基因调控过程中扮演着重要的角色,不仅揭示了一个全新的基因调控原则,更证明了这一原则对于多细胞生物,包括人类在内的生命体系,具有重大的意义。

获奖后,维克多与夫人的合影
如今,我们知道人类基因组中编码着超过1000多种miRNA。这些微小的分子,以其独特的方式,在基因调控的舞台上大放异彩,它们通过复杂的相互作用网络,精确地调控着基因的表达,从而影响着生物体的发育和功能。
从研究小线虫到发现miRNA后,两位学者被冷落了7年
20世纪80年代末,安布罗斯和鲁弗肯是H. Robert Horvitz实验室的博士后研究员。Horvitz后来于2002年与Sydney Brenner和John E. Sulston共同获得了诺贝尔奖。Horvitz利用线虫作为研究对象,揭示了器官发育和细胞程序化死亡是如何受基因调控的。
也正受到导师的影响,在这个实验室里, 安布罗斯和 鲁弗肯研究了一种看似不起眼的1毫米长的秀丽隐杆线虫(C. elegans),这种虫子尽管体型微小,却拥有许多与更大、更复杂的动物体内相同的专门细胞类型,如神经细胞和肌肉细胞,此外它具有寿命短、易于控制生长条件、通体透明、体细胞数目恒定且特定细胞位置固定等优点,使其成为研究个体发生、发育生物学、遗传学以及神经生物学的理想模型。
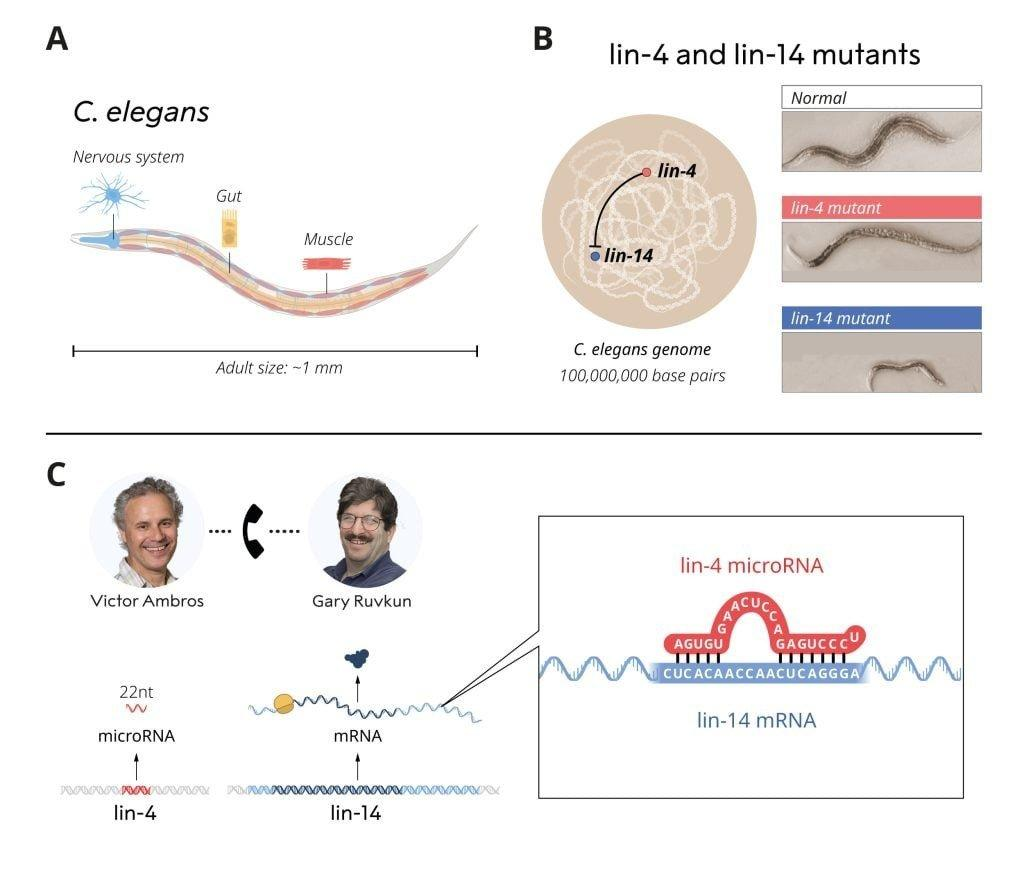
安布罗斯和鲁弗肯对控制不同遗传程序激活时间的基因非常感兴趣,这些基因确保了各种细胞类型在正确的时间发育。他们研究了两种突变体线虫——lin-4和lin-14,这两种线虫在发育过程中遗传程序的激活时间上存在缺陷。他们希望能识别出突变的基因并了解其功能。
在此前的研究中,安布罗斯已经证明lin-4基因似乎是lin-14基因的负调节因子。然而,lin-14活性是如何被阻断的,当时仍不得而知。安布罗斯和鲁弗肯对这些突变体及其潜在关系产生了浓厚兴趣,并着手解开这些谜团。
离开Horvitz实验室之后,安布罗斯在哈佛大学新建的实验室里对lin-4突变体进行了深入分析。通过系统的基因作图,他成功克隆了lin-4基因,并有了意外的发现。lin-4基因产生了一种异常短的RNA分子,这种分子缺乏编码蛋白质的代码。这些令人惊讶的结果表明,来自lin-4这种小分子RNA负责抑制lin-14。那么,这是如何工作的呢?
与此同时,鲁弗肯在麻省总医院和哈佛医学院新建的实验室里,他研究了lin-14基因的调控机制。与当时已知的基因调控机制不同,鲁弗肯发现并不是lin-14的mRNA产生被lin-4所抑制,调控似乎发生在基因表达过程的后期阶段,即通过关闭蛋白质生产来实现。实验还揭示了lin-14 mRNA中一段对于lin-4抑制其活性所必需的序列。
安布罗斯和鲁弗肯比较了他们的发现,并共同探索,从而取得了突破性进展。他们发现,短的lin-4序列与lin-14 mRNA关键段中的互补序列相匹配。他们进一步实验证明,lin-4 miRNA通过与lin-14 mRNA中的互补序列结合,从而关闭了lin-14,阻断了lin-14蛋白质的产生,接着他们发现了一种新的基因调控原理,这种原理是由一种以前未知的RNA类型——miRNA介导的。这一结果于1993年在《细胞》杂志上发表了两篇文章。
然而,这一发表的结果最初在科学界几乎没有得到回应。尽管结果很有趣,但这种不寻常的基因调控机制被认为只是秀丽隐杆线虫的一种特性,可能与人类和其他更复杂的动物无关。
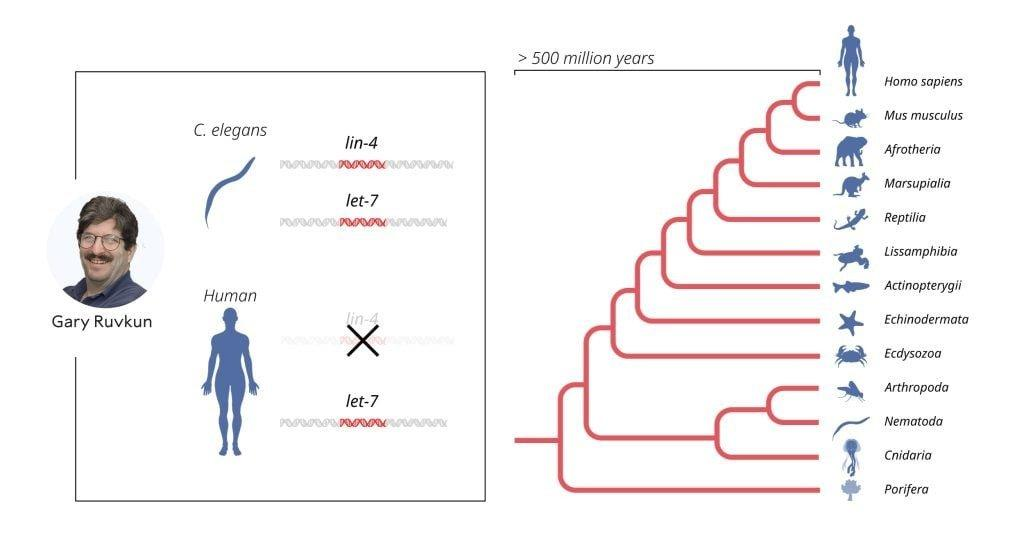
这种看法在2000年发生了改变,当时鲁弗肯的研究小组发表了他们发现的另一种由let-7基因编码的miRNA。与lin-4不同,let-7基因在整个动物界中高度保守。这篇文章引起了极大的兴趣,在接下来的几年里,人们发现了数百种不同的miRNA。如今,我们知道人类体内有超过一千种不同的miRNA基因,并且miRNA介导的基因调控在多细胞生物中是普遍存在的。
miRNA如何进行基因调控
miRNA是一类重要的非编码RNA分子,在基因表达调控中发挥着不可替代的作用。它们通过复杂的调控机制和精细的调控网络,实现对细胞生长、发育和疾病进程的精确控制。
miRNA的生物合成是一个复杂而精确的过程,它始于细胞核内的转录过程,主要包括编码作用和非编码作用两种路径。在编码作用中,miRNA的结构被编码在RNA聚合酶II转录的pri-miRNA中,经过加工形成预miRNA,再转运至细胞质中,通过核酸酶和Dicer酶的剪切作用,最终生成成熟的miRNA。而在非编码作用中,miRNA序列则存在于非编码RNA的内含子或外显子区域,通过内含子剪切或外显子剪切的方式产生成熟miRNA。
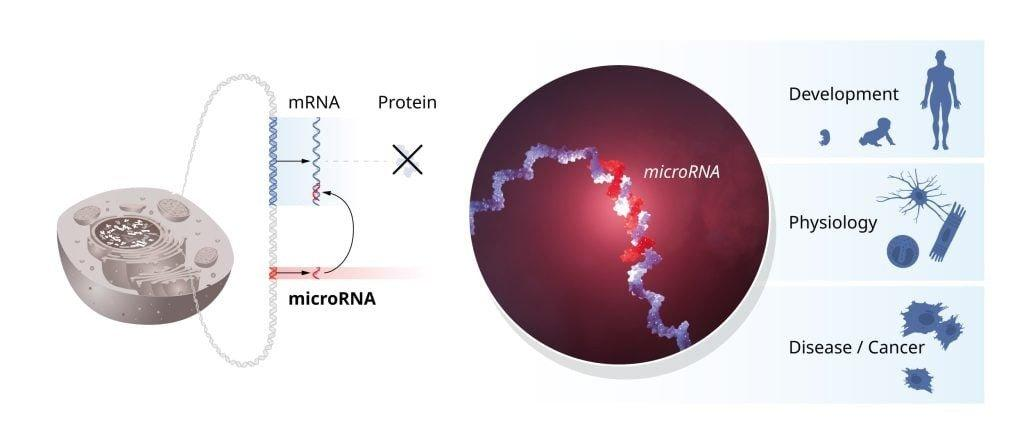
很显然,没有miRNA的参与,细胞与组织无法正常发育。一旦miRNA的调控出现异常,便可能引发癌症等严重疾病。编码miRNA的基因发生突变,已在人类中导致先天性听力损失、眼部及骨骼疾病等多种病症。
此外,miRNA生产过程中的一种关键蛋白质发生突变,还会引发DICER1综合征,这是一种罕见但严重的疾病,与多种器官和组织的癌症密切相关。
随着研究的不断深入和技术的不断发展,我们有望对miRNA的调控机制和调控方式有更全面的认识,并探索出更多的针对性调控策略,为生命科学研究和医学治疗开辟新的篇章。
两位诺奖得主简介

安布罗斯是一位备受尊敬的美国发育生物学家,他于1953年出生于美国新罕布什尔州的汉诺威,1979年获得麻省理工学院(MIT)博士学位,1979年至1985年,安布罗斯在麻省理工学院进行博士后研究,期间积累了丰富的科研经验和专业知识。
1985年,他成为哈佛大学的主要研究员,开始独立领导科研项目,并在该领域取得了显著的成果。并在1992年至2007年期间担任达特茅斯医学院的教授。如今,他是马萨诸塞大学医学院自然科学领域的西尔弗曼教授。值得一体的是,一位华人学者Roselind Lee当年在安布罗斯实验室读博,参与了安布罗斯早年对miRNA几乎所有的重要发现,后来这位优秀的学生,与安布罗斯喜结连理,成为名正言顺的“科研赢家”。

鲁弗肯则是一位在RNA调控领域做出杰出贡献的科学家,他的研究成果不仅推动了生命科学的发展,还为人类理解生物体的基因表达、发育和疾病进程提供了新的视角和方法。
他于1952年出生在美国加利福尼亚州的伯克利,1982年获得哈佛大学博士学位,并在麻省理工学院从事博士后研究。1985年,他成为马萨诸塞州总医院和波士顿哈佛医学院的主要研究员,现任遗传学教授。
可以说,两位学者在miRNA领域的原创性发现,不仅为我们打开一扇理解基因调控的大门,还开启了miRNA领域这个全新的研究领域,全球有无数分子生物学家从事这方面的研究,每年有成千上万篇论文发表出来,为我们揭示生命的奥秘。
审核:梁英 空军军医大学第二附属医院药剂科副研究员
出品:中国科协科普部
监制:中国科学技术出版社有限公司、北京中科星河文化传媒有限公司

来源: 返朴
内容资源由项目单位提供


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 返朴
返朴 
