注射用帕瑞昔布钠,适应症为用于手术后疼痛的短期治疗。
成份帕瑞昔布钠
化学名称:N-[[4-(5-甲基-3-苯基-4-异恶唑基)苯基]磺酰基]丙酰胺钠盐
化学结构式:
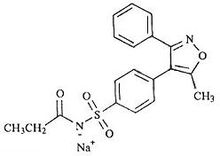
分子式:C19H17N2O4SNa
分子量:392.41
辅料:磷酸氢二钠七水合物,磷酸和/或氢氧化钠(用于调节pH值)。
性状本品为白色或类白色冻干块状物。
适应症用于手术后疼痛的短期治疗。
在决定使用选择性COX-2抑制剂前,应评估患者的整体风险。
规格(1)20mg;(2)40mg(以帕瑞昔布计)
用法用量推荐剂量为40 mg,静脉注射(IV)或肌肉注射(IM)给药,随后视需要间隔6-12小时给予20 mg或40 mg,每天总剂量不超过80 mg。可直接进行快速静脉推注,或通过已有静脉通路给药。肌肉注射应选择深部肌肉缓慢推注。
使用本品超过三天的临床经验有限。
与阿片类镇痛药联合用药:阿片类镇痛药可以与帕瑞昔布同时应用,本品使用剂量参见上文。在所有的临床评估中,帕瑞昔布是固定间隔时间给药,而阿片类药物则是按需给药。
由于选择性COX-2 抑制剂的心血管事件发生风险随着剂量及暴露时间增加而增加,因此,应尽可能使用最短疗程及最低每日有效剂量。
由于帕瑞昔布与其它药物在溶液中混合出现沉淀,因此不论在溶解或是注射过程中,帕瑞昔布严禁与其它药物混合。如帕瑞昔布与其它药物使用同一条静脉通路,帕瑞昔布溶液注射前后须采用相容溶液充分冲洗静脉通路。
静脉通路溶液的相容性
采用适用溶液配制后,帕瑞昔布溶液只能以静脉注射、肌肉注射、或加入下列液体的静脉通路给药:
氯化钠溶液 9 mg/ml(0.9%)
葡萄糖注射液 50 g/L(5%)
氯化钠 4.5 mg/ml(0.45﹪)和葡萄糖50g/L(5%)注射液
乳酸林格氏液
由于可以导致帕瑞昔布在溶液中沉淀,故不推荐向含 50 g/L(5%) 葡萄糖的乳酸林格氏液或其它未列出溶液的静脉通路中加入帕瑞昔布。
老年患者:通常,对于老年患者(≥65岁)不必进行剂量调整。但是,对于体重低于50 kg的老年患者,帕瑞昔布的初始剂量应减至常规推荐剂量的一半且每日最高剂量应减至40 mg。
肝功能损伤:通常,轻度肝功能损伤的患者(Child-Pugh评分5-6)不必进行剂量调整。中度肝功能损伤的患者(Child-Pugh评分7-9)应慎用帕瑞昔布,剂量应减至常规推荐剂量的一半且每日最高剂量降至40 mg。目前尚无严重肝功能损伤患者(Child-Pugh评分≥10)的临床用药经验,因此禁止在此类患者中使用帕瑞昔布。
肾功能损伤:依据帕瑞昔布的药代动力学,不必对轻度至中度(肌酐清除率为30-80 ml/min)、或重度(肌酐清除率[30 ml/min)肾功能损伤的患者进行剂量调整。但是,肾功能损伤的患者以及具有液体滞留倾向的患者用药时应密切观察。
儿童与青少年:没有在儿童或青少年中的使用经验,因此不推荐在此类人群中使用。
使用与处置(包括丢弃)指导说明
注射用帕瑞昔布钠使用前必须重新配制。由于不含防腐剂。因此要求采用无菌技术进行配制。
配制溶剂:
可用于配制注射用帕瑞昔布钠的溶剂包括:
氯化钠溶液 9 mg/ml(0.9%)
葡萄糖注射液 50 g/L(5%)
氯化钠 4.5 mg/ml(0.45%) 葡萄糖 50 g/L(5%)注射液
配制过程:
采用无菌技术配制帕瑞昔布冻干粉(即帕瑞昔布钠)。去除黄色(20 mg)/紫色(40 mg)启扣盖,暴露帕瑞昔布玻璃瓶橡胶瓶塞的中央部分。用无菌注射器及针头吸取适用溶剂(20 mg帕瑞昔布钠用1 ml 溶剂配制,40 mg帕瑞昔布钠用2 ml溶剂配制),然后将针头插进橡胶瓶塞中央向瓶内注入溶剂。轻轻旋转瓶体使粉末完全溶解并在使用前仔细检查配制成的溶液。将瓶内全部药液抽出供单次给药。
配制后,帕瑞昔布钠溶液应在使用前进行目测,确定溶液是否有不溶性微粒或发生变色。若观察到溶液发生变色,出现絮状物或不溶性微粒,则不得使用。
已经证实在25℃条件下,配制后药液的物理、化学稳定性可保持24小时。从微生物学角度,无菌配制的溶液应立即使用,使用者必须在使用前控制其贮藏时间与条件。一般来说,在25℃条件下保存不应超过12小时,除非溶液的配制是在严格控制的、并经过验证的无菌环境中进行,配制后,帕瑞昔布溶液应在24小时内使用,否则应废弃。
配制后的帕瑞昔布钠溶液为等渗溶液。
配制后的药液仅供单次使用。任何配制后未使用的溶液、溶剂、或废弃物品都应当按照当地要求予以处理。
药物不相容性
除[使用与处置(包括丢弃)的指导]所列药物外,帕瑞昔布不得与其它任何药物混合。
帕瑞昔布不应与阿片类药物混和于同一注射器内给药。
使用乳酸林格氏液或含50 g/L(5%)葡萄糖的乳酸林格氏液配制,帕瑞昔布会在溶液中发生沉淀,故不推荐使用。
不推荐使用灭菌注射用水,因为得到的溶液不等渗。
不得将帕瑞昔布溶液注入其它药物的静脉通路。帕瑞昔布溶液注射前后应用相容溶液充分冲洗静脉通路。
由于可以导致帕瑞昔布在溶液中沉淀,故不推荐向含50 g/L(5%)葡萄糖的乳酸林格氏液或其它[使用与处置(包括丢弃)的指导]中未列出溶液的静脉通路中加入帕瑞昔布。
不良反应根据国外文献报道,在不同发生率类别中,不良事件按其严重程度降序排列。
在28 项安慰剂对照临床研究中,在5402 名接受帕瑞昔布治疗的患者中,曾报告出现以下不良反应。
[非常常见(》1/10),常见(≥1/100,


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助

