阿尔兹海默症,一种广为人知的神经退行性疾病,表现为记忆下降,逐渐丧失日常生活能力,并伴有精神症状和行为障碍,常因感染等并发症死亡。随着人口老龄化的加重,阿尔兹海默症对社会而言是巨大的医疗和护理负担;对家庭而言是一边要承受24小时看护照料的艰辛,一边要面对至亲丧失记忆的悲痛;对个人而言则是游走于清醒和失忆之间,无力、无奈、愧疚、甚至自尊缺失的巨大折磨。
对于这样一种疾病,我们对他的发病机理知之甚少,且仍然没有行之有效的治疗手段,但冷冰冰的数字却告诉我们,随着年龄的增加,阿尔兹海默症的发病率呈指数级增长,85岁以上的老人中的患病率高达30% [1]。因此,开发治疗或改善阿尔兹海默症的药物是当前亟待解决的医学难题之一。
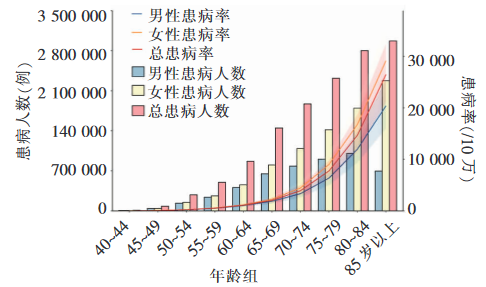
图1. 2019年我国的阿尔兹海默症及其他痴呆分年龄组患病情况
然而当前对于阿尔兹海默症的药物开发已进入艰难的瓶颈期。美国药品研究与制造商协会的数据显示,1998-2017年进入临床试验的150例药物种,仅4例获批上市。更多科学家和药企已将研发重点放在包括干细胞疗法和肠菌疗法在内的新型治疗手段。
阿尔兹海默症的成因非常复杂,包括遗传因素和生活方式等,其本质是脑部细胞的损伤或神经元连接的退化,具体表现为蛋白错误折叠和聚集,神经炎症,细胞信号转导异常,细胞运动受损等。而肠道菌群及其代谢产物能够在不同程度上影响上述过程。
肠道菌群能够合成或加工神经递质。比如乳酸杆菌可以加工合成乙酰胆碱,利用阿尔兹海默症动物模型已经证明,补充乳酸杆菌可以减轻淀粉样β蛋白神经毒性,提高空间认知能力 [2, 3]。另外,乳酸杆菌和双歧杆菌可以表达γ-氨基丁酸,这种神经递质在阿尔兹海默症病人的脑脊液中明显更低 [2, 3]。通过补充特定的肠道菌群来上调γ-氨基丁酸的水平从而改善阿尔兹海默症的研究正在动物实验中展开。
**肠道菌群可以调节脑部神经炎症和小胶质细胞功能。大脑中的常驻巨噬细胞,也叫小胶质细胞,是大脑中的清道夫,也是抵御外源异物的第一道防线。清除大脑中坏死的神经元、斑块以及感染物。但当我们年龄增长的时候,小胶质细胞功能退化,清除大脑废物的能力下降,伴随而来的就是认知能力的下降。某些肠道中吸收的代谢产物,比如异戊胺(isoamylamine)[4],****N6-**羧甲基赖氨酸等,能够随着年龄积累,只在老年阶段达到高峰并引发神经退行性疾病。**N6-**羧甲基赖氨酸在老年人群的血液和脑部的水平都远高于年轻人,因此也是与老年人退行性疾病高度相关的代谢物。N6-羧甲基赖氨酸主要堆积于小胶质细胞中,引起小胶质细胞基因表达差异,活性氧暴涨,而线粒体活力和ATP水平下降。活性氧过高会使细胞长期处于氧化压力,而线粒体失活则直接导致细胞缺乏能量,共同的结果就是细胞无法维持正常的代谢和功能,只有走向坏死[5]。另一种肠道菌群来源的代谢产物TMAO也是诱导神经炎症和加速认知退化的元凶之一。补充乳酸杆菌等益生菌,改变肠道菌群组分,竞争性的抑制TMAO的合成也在小鼠模型中被证明是有效改善认知退化的手段[6]。
有的读者可能还记得上次文章中我们提到的血脑屏障(blood-brain-barrier, BBB),为什么血脑屏障不能阻挡N6-羧甲基赖氨酸或者TMAO等有害物质呢?血脑屏障难道挡了个寂寞?

图2. 血脑屏障示意图
血脑屏障最初被发现是通过两个科学家所做的染色实验。PaulEhrlich在外周血中加入染料后发现唯独脑组织并没有被染色。而Goldmann在脑脊液中加入染料后发现只有脑组织被染色,染料并不能进入血液以及其他任何器官。因此血脑屏障是一种双向阻隔。
血液流经我们身体各处,以毛细血管的形式与组织细胞相接触,并且释放氧气,带走二氧化碳,释放营养物质,带走代谢废物。脑部或脊柱处也存在毛细血管,但这些毛细血管被层层细胞包裹,里面的物质想要释放出来进入脑组织还真不容易。毛细血管壁是一层内皮细胞,接着是一层周细胞,再接着是基底层,然后才是脑细胞即星形胶质细胞。除了层层包裹,脑毛细血管还比身体其他位置的毛细血管审查机制更严格,允许放行的大小分子更有限。这两个方面共同构成了血脑屏障的概念。正是因为血脑屏障的出现,才使得中枢神经系统不会轻易的被外源毒素、药物等伤害,又能保证必须的养分供应,保持大脑功能正常。
然而遗憾的是,当人老了血脑屏障通透性也会增加,有的科学家认为这才是老年人认知退化的关键。不仅如此,部分促炎性因子甚至可以降低脑毛细血管内皮细胞的紧密连接,破坏血脑屏障的完整性,好让自己轻而易举地进入脑部环境,诱发神经炎症[7]。有科学家发现给小鼠口服乳酸杆菌和双歧杆菌能够降低血脑屏障地通透性,小鼠海马体中的炎症因子降低,并且小鼠认知能力有所提升[8]。
说了这么多,到底有没有临床试验证明某些益生菌能够治疗阿尔兹海默症呢?
这个确实有。来自伊朗的一个科研团队招募了60名阿尔兹海默症患者,其中30人每天服用200mL含有5种益生菌的牛奶,作为对照的阿尔兹海默症患者仅食用牛奶。经过12个星期的治疗,发现服用益生菌的病人精神状态检测****的评分更高,但是体内的炎症因子水平与对照组差异不大 [9]。另外还有三个类似的临床试验给病人补充了包含双歧杆菌、乳酸杆菌在内的若干菌株,并发现益生菌可以改变肠道菌群构成、外周血中的代谢产物和细胞因子水平、活性氧的含量以及改善病人的精神状态检测的评分 [10]。
除了直接服用益生菌,其他调节肠道菌群的化合物也能够起到改善阿尔兹海默症的功效。比如由耿美玉教授团队和上海绿谷制药研发并获批上市的新型药物甘露特纳胶囊,其主要成分低聚甘露酸钠就是通过重塑肠道菌群、改变肠菌代谢物,达到降低脑部炎性细胞浸润和改善认知的作用,临床试验表明服用4周就能够看到效果。不过由于低聚甘露酸钠能够穿过血脑屏障,也不排除它能够直接调节脑部微环境等功能 [11]。
总的来说,肠道菌群对神经退行性疾病的影响不可忽视,然而如何利用肠道菌群这个刚刚被我们认知的器官,让它为我们所用,降低对脑部神经元有害的代谢产物,降低促炎性因子水平,帮助补充神经递质,增强血脑屏障功能,才能真正实现治疗阿尔兹海默症等疾病的目的。与此同时,发掘肠道菌群在治疗神经退行性疾病过程中的其他机制也同样重要。
[1] 任汝静, 殷鹏, 王志会等,代表中国阿尔茨海默病报告编写组. 中国阿尔茨海默病报告2021[J].诊断学理论与实践,2021, 20(04): 317-337.
[2] Eicher TP, Mohajeri MH.Overlapping Mechanisms of Action of Brain-Active Bacteria and BacterialMetabolites in the Pathogenesis of Common Brain Diseases. Nutrients.2022;14(13):2661. Published 2022 Jun 27.
[3] Ji HF, Shen L.Probiotics as potential therapeutic options for Alzheimer's disease. ApplMicrobiol Biotechnol. 2021;105(20):7721-7730.
[4 Teng Y, Mu J, Xu F, et al. Gutbacterial isoamylamine promotes age-related cognitive dysfunction by promotingmicroglial cell death. Cell Host Microbe. 2022;30(7):944-960.e8.
[5] Mossad O, Batut B, Yilmaz B, et al. Gut microbiotadrives age-related oxidative stress and mitochondrial damage in microglia viathe metabolite N6-carboxymethyllysine. Nat Neurosci. 2022;25(3):295-305.
[6] Wang QJ, Shen YE, Wang X, et al.Concomitant memantine and Lactobacillus plantarum treatment attenuatescognitive impairments in APP/PS1 mice. Aging (Albany NY).2020;12(1):628-649.
[7] Ni P,Dong H, Wang Y, et al. IL-17A contributes to perioperative neurocognitivedisorders through blood-brain barrier disruption in aged mice. JNeuroinflammation. 2018;15(1):332. Published 2018 Nov 30.
[8] YangXD, Wang LK, Wu HY, Jiao L. Effects of prebiotic galacto-oligosaccharide onpostoperative cognitive dysfunction and neuroinflammation through targeting ofthe gut-brain axis. BMC Anesthesiol. 2018;18(1):177. Published 2018 Nov30.
[9] Akbari E, Asemi Z, Daneshvar Kakhaki R, et al. Effect ofProbiotic Supplementation on Cognitive Function and Metabolic Status inAlzheimer's Disease: A Randomized, Double-Blind and Controlled Trial. FrontAging Neurosci. 2016;8:256. Published 2016 Nov 10.
[10] Naomi R,Embong H, Othman F, Ghazi HF, Maruthey N, Bahari H. Probiotics for Alzheimer'sDisease: A Systematic Review. Nutrients. 2021;14(1):20. Published 2021 Dec 22.
[11] Wang X, Sun G, Feng T, et al. Sodium oligomannatetherapeutically remodels gut microbiota and suppresses gut bacterial aminoacids-shaped neuroinflammation to inhibit Alzheimer's disease progression. CellRes. 2019;29(10):787-803.
(封面图片来源于网络)
文章由科普中国****创作培育计划出品,转载请注明来源



 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 最前沿的肠道菌群知识
最前沿的肠道菌群知识 
