酯在碱性溶液中的水解,产生碱性较强的烷氧基负离子和酸性较弱的羧酸,二者发生反应使平衡移向产物,故酯的碱性水解是不可逆的。多数酯在碱催化下按双分子碱催化酰氧断裂(Bac2)机理水解。
背景知识羧酸衍生物的物化性质酯常为液体,低级酯具有香味,酯的比重小,在水中溶解度低,是优良的有机溶剂。羧酸衍生物的化学性质可以分为两大类:一是衍生物的相互转化;另外是衍生物自身的特性反应。
羧酸衍生物的水解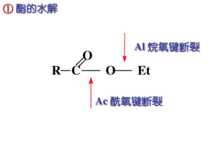
 根据酸碱的催化,烷氧基和酰氧基的断裂,可以分为8种类型,其中Bac1和Aal2尚未被发现。1
根据酸碱的催化,烷氧基和酰氧基的断裂,可以分为8种类型,其中Bac1和Aal2尚未被发现。1
酯在碱性溶液中的水解,产生碱性较强的烷氧基负离子和酸性较弱的羧酸,二者发生反应使平衡移向产物,故酯的碱性水解是不可逆的。羟基进攻酯的羰基碳,形成带负电荷的四面体结构的中间体,是反应速率最慢的一步。紧接着烷氧基离去,形成羧酸和烷铖基负离子,两者迅速发生酸碱中和反应(不可逆反应),生成酰氧基负离子(盐〉和醇。
多数酯在碱催化下按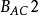 机理水解:
机理水解:
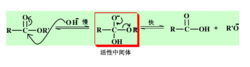
酯在碱溶液中的水解反应的速率主要取决于四面体的中间体的稳定性,凡能分散负电荷的取代基,即在酯羰基附近连有的吸电子基越多,可使中间体稳定,反应越易进行。2
影响因素1 碱水解的速率和氢氧根离子成正比。
2 羰基活性越大,α-C空阻越小,酯基空阻越小,反应速率越快。
3 形成的四面体中间体能量越低,反应速度越快。能分散负电荷的取代基对反应有利。
4 酯的碱性水解是不可逆的,碱的用量要超过催化剂量。1
相关知识酸催化酯水解的原理:
反应的第一步是酯中羰基质子化,从而增加羰基碳的正电性,有利于亲核试剂的进攻。第二步是质子化的羰基与水加成形成带正电荷的四面体结构的中间体。第三步是质子转移和消除醇分子,生成羧酸。该反应速率取决于形成四面体结构中间体的稳定性。与碱溶液水解反应一样,R和基闭体积增大,反应速率降低;与碱液水解不同的是中间体带正电荷,所以R基团供电子能力增强,使中间体稳定而水解反应速率加快。2
本词条内容贡献者为:
李廉 - 副教授 - 中国矿业大学


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助

