模型含义
以还原反应为例说明缩核模型。还原反应是典型的气一固相反应,且由外向内逐步推进。被还原的矿石内部存在一个由未反应物组成的,不断缩小的核心,直至反应结束。还原的固态产物层附着在固态反应物上,且形状和体积与原矿相差不多,变化可忽略不计。矿石较致密,还原后则较疏松。气体在产物中的扩散与在原矿中相比要容易得多。人们把以上的特点理想化,构造出一个反应模型,称为缩小的未反应核模型,简称缩核模型。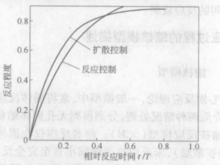
根据缩核模型理论,其反应速度由两个方面决定:一是原料与产物接触面的化学反应速度(反应控制),二是气相在产物层的扩散速度(扩散控制)。图是两种控制方式在相对时刻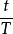 (T是一个颗粒完全反应完毕的时间)时对反应进程影响程度的曲线图,从中可看出,两种控制方式,其反应进程与相对反应时间变化趋势不完全相同,反应控制相对变化较快一些。2
(T是一个颗粒完全反应完毕的时间)时对反应进程影响程度的曲线图,从中可看出,两种控制方式,其反应进程与相对反应时间变化趋势不完全相同,反应控制相对变化较快一些。2
缩核模式的传统理论认为,晶粒转变是通过伪晶转变实现的,通常有两种晶粒转变机理:
伪晶转变机理。在整个反应过程中,反应面由颗粒表面深入核心产物保留与原始颗粒相似的形貌,典型的情况下,在产物上有一些孔洞。
化学气相迁移(CVT)机理。原始颗粒随着形成一种中间气体迁移相而分解,这种迁移相在产物晶核上沉积,这样形成的产物形貌完全与以前不同,产物的粒度分布由气相沉积的条件决定。
示例计算如图所示,我们以下列反应对缩核模型加以说明。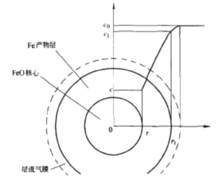
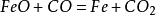
为了表达方便,取矿石形状为标准球体。这样,化学反应面的推进和扩散都可简化为一维问题,面积的表示也简单得多。实际反应物与理想形状存在或大或小的差别,但可在此基础上进行修正。3
球状反应物的初始组成全部是FeO,半径为r1。随着还原反应的进行逐步形成一个Fe产物层,未反应的FeO核心半径缩小至r。在固态反应物的周围存在着一个由层流边界层组成的气膜。这时,总的反应过程可分解为以下几个步骤:
CO通过气膜向固态产物(Fe)表面的扩散。这个过程称为外扩散。气膜外的CO浓度CO与气相中心相等,固态产物表面处(气膜内)的CO浓度为c1。
CO通过产物层向反应界面(Fe与FeO界面)的扩散。这个过程称为内扩散。反应界面半径为r,界面处CO浓度为c。
在界面上进行反应FeO+CO=Fe+CO2。这个过程称为表面化学反应。
反应生成的CO2通过产物层向外扩散至气-固界面。
CO2通过气膜向气流中心扩散。
上面是缩小的未反应核模型的内容。根据这个模型可建立起铁矿石(特别是球团矿)还原反应的动力学微分方程式。
发展简史1991年Jones首先将缩核模型应用于SCFE过程,此后,后藤元信(Goto M)等致力于在SCFE中应用缩核模型的研究,在1996年曾发表两篇论文,一篇是专门有关缩核模型的研究。他们指出,从固体物料中萃取或浸取溶质是个涉及在固体基质中的传质过程。当溶质含量与其在溶剂相中的溶解度相比要大得多时,则该过程与不可逆脱附(irreversible desorption)相似。将缩核模型用在SCFE过程中,对包含轴向弥散的模型作了数值解,并对不含轴向弥散的拟稳态(quasi-steady-state,Qss)解作了研究,讨论了此种情况下模型的准确度;另一篇论文是用SC-CO2,萃取冷冻干燥的姜,得到姜油的实验研究,再用缩核模型对所得的实验结果进行分析,认为该模型对大颗粒姜的萃取实验结果模拟是成功的。1
来源: 百度百科


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助

