大脑,这个人类体内的“三磅宇宙”,是记忆与认知的主宰。它错综复杂、蜿蜒密布的结构如一座神秘的森林,几百年来,吸引全球的脑科学专家孜孜不倦地探索。
解码大脑的赛道上,少不了中国科学家的脚步。近期,由我国科技部重点培育的“全脑介观神经联接图谱”大科学计划,在《细胞》《神经元》等国际期刊发布了10项重要成果。浙江大学医学院附属第一医院章京团队联合浙江大学段树民院士团队参与了这项全球瞩目的任务,历时两年,成功绘制出全球首张“正常人及阿尔茨海默病患者的海马单细胞分辨率空间转录图谱”。
浙江脑科学专家的这一突破性进展,为数以千万计的阿尔茨海默病患者带来曙光:它为精准诊疗靶点的开发提供了新的可能,标志着我们在病理诊疗的道路上迈出了关键一步。
这张图谱将如何助力我们理解、诊断和治疗阿尔茨海默病?带着这些问题,记者走访研究团队,解码这张海马区的“高清地图”。

实验过程中的章京(就座者)研究团队。 受访者供图
在大脑海马区装一台GPS
海马体是阿尔茨海默病最早累及的脑区之一,其中海马的受损是出现记忆障碍的核心原因,这种现象,也就是我们俗称的“老年痴呆”。
数据显示,2025年中国阿尔茨海默病及相关痴呆患病人数近1700万例,占全球病例数的29.8%。这一无法逆转的疾病,至今仍缺乏有效的早期诊断和治疗手段。
面对阿尔茨海默病发病率持续上升的严峻现实,寻找破解之道刻不容缓。作为全球首张海马单细胞分辨率空间转录图谱,这张“大脑地图”,精准定位了阿尔茨海默病的病灶。
“相当于为海马脑区的所有种类细胞都配发了‘身份证’,装上了GPS。”浙江大学医学院附属第一医院余杭院区副院长及病理科主任、浙江大学教授章京打了一个生动的比方。这张图谱不仅清晰区分了神经元、胶质细胞等大类,还捕捉到过去未被定义的稀有细胞亚群,在海马不同亚区的水平揭示了疾病特异的细胞基因的改变。
同时,研究发现细胞类型—脑区—胞外囊泡的三维网络交互,筛选了具有差异的脑源性胞外囊泡。“既有神经元表达的蛋白信号,又有空间信号,可用信息较之以往大为丰富。”
看得更清,才能治得更准。这张“地图”的诞生,为我们深入理解阿尔茨海默病,寻找早期诊断的“信号”,开发早期精准诊疗的靶点,提供了一把前所未有的钥匙。
神经系统疾病与其他疾病最大的不同,在于脑区的特异性。不同脑区,甚至同一脑区的不同亚区,神经细胞的差异都极为显著。而在病理诊断中,差之毫厘,失之千里。
比如,阿尔茨海默病发病时,最早死亡的是胆碱能神经元;而帕金森病发病时,比较早死亡的是多巴胺神经元。此外,人的海马神经元存在多种亚型,不同亚型引发的病症各不相同。海马体不同亚区的神经元死亡,后果也截然不同。
因此,在单细胞水平实现精准定位,便成为解析病理、锁定病因的关键。“以前只能定位到‘社区’,以‘小区’为单位进行病理研究,而单细胞水平,相当于定位到了小区中的‘每一个人’。”章京说。
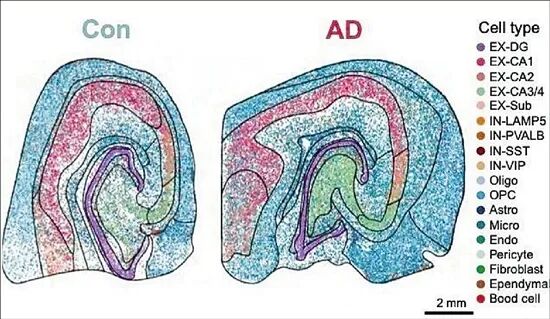
浙江脑科学家团队绘制的正常大脑的海马图谱(左)和阿尔茨海默病患者的海马图谱(右)。 图源:《神经元》期刊官网
单细胞水平的研究,成为解密大脑工作机制的关键。
“全脑介观神经联接图谱”大科学计划于2018年倡议发起。这项计划也将“介观”这一概念带到人们眼前。
“过去的研究多聚焦于宏观或微观层面。前者把大脑当作黑箱,只关注输入与输出,却不清楚中间发生了什么。微观虽在单个神经细胞或突触层面取得很大进展,但仍难以解释大脑的整体运作机制。”中国科学院院士、浙江大学教授段树民解释,大脑真正的奥秘,藏在宏观与微观之间的“介观”尺度。
介观,也就是脑科学里的“神经环路”水平,俗称“神经网络”。“大脑功能是大量神经元在环路水平上协同运行的结果。”段树民说,海马单细胞分辨率空间转录图谱,正是在这一水平绘制的高精度“地图”。在它的“导航”下,我们可以更好地解析脑区细胞及其周边环境,破解大脑运作的密码。
自19世纪以来,绘制人脑图谱就成为历代神经科学家孜孜以求的目标。至此,这个无数科研人员接力探索的复杂结构,正向我们敞开一个全新的符码。
一场多重考验的科研马拉松
这张介观脑图谱的可贵之处,在于定格了海马体区域的静态图像。它的绘制过程,堪比一场对脑力、耐力以及技术都有着极致要求的科研马拉松。
国家健康和疾病人脑组织资源库位于浙江大学医学院教学楼一楼。走进这间不算宽敞的实验室,17台超低温冰箱正持续运转,守护着一批珍贵的脑组织样本,它们是“大脑地图”得以成功绘制的重要素材来源。
“正是有了这8位阿尔茨海默病患者与8位认知正常者无私捐献的脑组织,才使这项跨越生死的精密研究成为可能。”国家健康和疾病人脑组织资源库常务副主任、浙江大学教授包爱民会向每一位参观者耐心解释,脑组织样本来之不易,保存条件与工序更是极为严格,每一步都决定着后续研究工作的成败。
“脑组织取样严格控制在死亡后10小时之内,其中半脑立即经由液氮速冻,进而转入负80度超低温冰箱冷冻存储,以最大限度保留生物大分子的完整性,满足包括本次研究在内的单细胞高分辨率空间转录图谱实验要求。”包爱民说。这些样本通过了正规的人脑组织材料研究申请和审批程序,在脑库精心选择、严格匹配之后,被发送给科研工作者进行研究。
获取高质量的样本仅仅是万里长征的第一步,随后的切片与测序过程,最为费时,更是对耐心和技术的考验。
海马体是大脑深处的复合结构,像海马一样蜷缩着。要把它切成80到100多张极薄的诊断切片,同时还要完美保留其中的空间位置信息。取材、切片、染色、分析……每一步都如履薄冰,任何微小的操作失误都可能导致前功尽弃。整个过程无异于在豆腐上完成最精妙的雕刻。
在经历了上百次切片分析后,研究团队才获得了可供测序分析的高质量样本。“单是这一过程,就占据了整个研究三到四成的时间。”章京回忆道。
绘制人脑“地图”,涉及的工程量超乎想象。介观层面脑图谱的分辨率通常为数百纳米,仅一个猕猴大脑的数据量就可达500TB(太字节)的超大量级。如果将分辨率进一步提高至几十纳米,那么猕猴大脑图谱数据量将达到数十PB(千万亿字节),足以超过一个普通数据中心的数据存储量。
而人脑的神经元数量是猕猴脑的十几倍。“如果想对人脑进行三维重构,其算力之巨大难以估量。”段树民补充道,放眼整个“全脑介观神经联接图谱”大科学计划,是一项极为庞大的工程。人脑包含近千亿个神经元,而每个神经元又与成千上万的其他神经元相连,要将这些浩如烟海的分子表达蛋白和空间关系同时描绘出来,难度可想而知。
面对如此庞大的数据,研究团队利用深圳华大生命科学研究院自主研发的时空组学技术Stereo-seq(空间增强分辨率组学测序),并借助人工智能模型算力,最终成功在两年内完成了海马整张图谱的绘制。
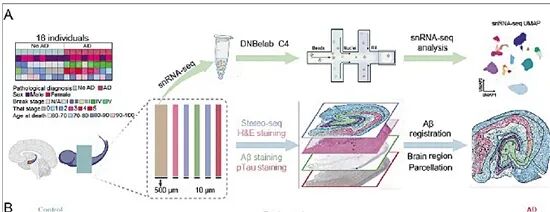
浙江脑科学家团队绘制的海马分区及亚区的转录差异(局部图)。图源《神经元》期刊官网
剩下的99%值得期待
如今,各国在脑科学研究领域的竞争日趋白热化。在9月举办的2025介观脑图谱国际研讨会上,《国际灵长类介观脑图谱联盟白皮书》正式发布,为“全脑介观神经联接图谱”大科学计划勾勒出清晰规划:到2050年,要完成人脑介观图谱的“大作”。
距离这一目标实现还有多远?
人脑包含860亿个神经元,1000多亿个胶质细胞,蜿蜒密布的血管穿插其中,组成一个庞大的网络。“目前我们大概完成了全图的1%。”章京坦言。但他随即强调:“但这是至关重要的1%,因为在此过程中,我们实现了技术体系的创新。实践表明,我国自主研发的光学成像技术已在灵长类介观脑图谱绘制中展现出优异的高效性与可靠性。”
掌握了“从0到1”的方法论与技术体系,眼下,章京与团队正计划将研究从海马体拓展至前额叶皮层、丘脑等更多关键脑区。与此同时,他们的探索正从横向水平向纵深推进。
“过去我们更关注细胞‘个体’之间的差异,就像比较‘一家人和邻居家的不同’。”他比喻道,“而现在,我们要深入观察‘同一个家庭内部成员是如何协作的’——也就是同一亚区内部,不同细胞器、信号通路之间如何协同与联动。这能让我们看清细胞在病理压力下,其内部究竟发生了哪些特异性反应,从而更精准定位疾病。”
在学界的一片火热中,科学家们并不满足于仅绘制出大脑的静态结构图,而将目光投向更落地的疾病诊断与治疗层面。
这一思路也贯穿于章京和段树民团队的研究过程。在绘制海马单细胞分辨率空间转录图谱的过程中,研究团队利用创新的纳米流式检测技术,对血液中的生物标志物进行筛选。最终,他们在几百种血液标志物中,找到诸如CCK等具有诊断价值的新型外周血神经来源细胞外囊泡相关标志物——这为阿尔茨海默病早期诊断及鉴别诊断提供了新型生物标志物,将有可能改变我们对抗这种“记忆窃贼”的方式。
“阿尔茨海默病早期诊断难,如今希望能够通过抽血这样的检测和诊断,为未来开发更加精准的干预策略奠定重要基础。”段树民表示。
不过,从实验室的突破走向临床的普及,真正打通从基础研究到临床应用的全链条,仍面临不少挑战。
在包爱民看来,脑组织样本来源的稀缺性,是当前的主要难点之一。“目前全球人脑资源库所收集到的脑组织样本总量仍然有限,且由于存在着潜在的由地域与种族差异而导致的例如遗传学、表观遗传学差异,可能会限制研究成果的普适性与转化潜力。”她表示,足够数量且具有人群代表性的脑组织样本,是构建可靠疾病模型、开展有效药物筛选及准确评估疗效的核心基础,因此,仍需要持续推动公众对脑捐献的认知与接受度。
此外,多位专家表示,要完成数据量如此庞大、所需算力巨大的研究,并在此基础上推进药物研发等临床转化,仍然需要持续且大规模的资源和资金支持。
所幸,浙江作为数字经济和人工智能产业的高地,近年来在智能计算、脑科学与脑机融合等领域持续推进创新应用。“有了算力、算法的系统加持,未来三到五年,我们将有望在脑疾病的精准预警和干预策略上实现突破,这会大大加速整个神经科学的发展进程。”章京笃定地说。
站在神经科学的新起点,介观脑图谱正如同一套日益精确的“大脑导航”,指引我们深入这片未知的疆域。未来,脑疾病可以像天气预报一样实现早期预警;医生能依据每个人的脑细胞图谱制定个性化神经保护方案……这些曾属于科幻的图景,正在科学家们持之以恒的探索中,一步步照进现实。
虽然,脑科学家们只完成了“大脑地图”的1%,但另外的99%,依然值得我们期待。
(本文作者 杨千莹 周林怡 陈宁)
延伸阅读
1%,亦是希望
如章京所言,我们完成了“全脑介观神经联接图谱”的1%。笔者看来,在脑科学领域,这看似微小的1%蕴含无限希望。
大脑,被称作人类身体上最后一个“黑匣子”。它浩如烟海的神经联接,高度的多样性,以及差异性,不断激发着全球顶尖科研团队的好奇心。随着各国创新体系的迭代更新,大脑研究的新进展层出不穷:从脑机接口技术的迭代升级,到阿尔茨海默病发病机制的新发现,再到各国脑科学计划的陆续发布都令人欣喜不已。
要知道,每一项宏大的计划,都离不开对最初1%的执着。笔者曾多次在全国两会、省两会期间采访“老委员”段树民院士,多年来,他的不少提案都围绕建设人脑组织库、启动中国的脑科学研究计划等。会场内外,段院士多番呼吁尽快建立“中国人脑库”基地的情景历历在目。可以说,没有这股韧劲,就没有今天弥足珍贵的1%。
积跬步,以至千里。我们珍惜这1%,不仅因为它为阿尔茨海默病早期诊断及鉴别诊断提供了新型生物标志物,更因为它是“从0到1”的突破,显示了我国脑科学研究实力的整体跃升。这1%告诉我们,今天,在全国,乃至全球科学家的合力之下,“全脑介观神经联接图谱”另外99%的工作正在齐头并进,它让我们相信,人类终能破解大脑之谜,为攻克脑疾病提供重要支撑。
(作者 陈宁)
专家观点
人脑组织库:给未来以希望
过去几十年,生物医药科技进展显著,很多疾病,例如传染病、癌症等都已有了治愈的希望,但人脑疾病的治疗却鲜有突破性进展。人脑和动物脑的差别太大,采用动物模型去研究人脑疾病往往只能模仿某些症状,而无法模拟人脑发病机理。科学家们已经认识到,对于人脑研究的最好样本就是人脑组织本身。
然而,由于人脑的重要性,很难通过手术途径获得正常脑组织样本,更难以获得完整的大脑去进行研究。巧妇难为无米之炊,一筹莫展的科学家们最终想出的好办法就是建立“脑银行”,又称人脑库。也就是通过志愿捐献途径,在捐献者去世后,把大脑完整取出并用特定方法保存,研究脑和脑疾病的科学家可以向人脑库申请使用存放的脑组织样本(就像从银行贷款一样),源源不断地产生科学研究成果,造福子孙后代。
中国人口众多,在建立人脑库、致力于防治脑疾病的研究方面也有着强烈的社会需求和社会责任。在中国科学院院士段树民的发起和领导下,浙江大学医学院于2013年建立了中国人脑库。2014年和2016年,中国分别召开了首届和第二届“中国人脑组织库国际研讨会”。由浙大医学院、协和等在内的十个医学院所共同发起了“中国人脑组织库协作联盟”,并且制订和发表了第一版《中国人脑组织库标准化操作方案》。
脑库严格遵守伦理学指导方针,例如遵守捐赠者及家属的知情同意、脑组织存取过程的开放透明以及脑库的非营利政策等。任何一位希望通过捐献自己的大脑来支持脑科学研究的人都可以成为捐献者。为了保护个人隐私,脑组织及其数据只在匿名化处理后才会提供给科学家研究。捐献者们都是在生前通过签署知情同意书,高尚地准许脑库在他们去世后获取其大脑和相关病史材料,应用于科研。
“脑银行”承载着人类未来的希望,对防治包括阿尔茨海默病和精神疾病在内的各种脑疾病都有着不可替代的功用。科学家们从实验材料中获取信息越多,就能越快揭示这些疾病的产生机理,从而开发有效的治疗方法。最终,全体人类都会得益于捐献者所赠与的这份礼物,它使得科学有了进步的可能,先人的生命与善意将永远延续下去。
(作者 包爱民 系浙江大学医学部教授、国家健康和疾病人脑组织资源库常务副主任)
来源: 浙江日报、潮新闻


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 浙江省科学技术协会
浙江省科学技术协会 