在微生物世界的边界上,科学正重新定义“移植”的含义。
过去我们以为粪菌移植(FMT)只是把健康人的细菌群落移入病人的肠道,如同重新播种一片荒地。
但发表在 Advanced Science 的论文《The Next Generation Fecal Microbiota Transplantation: To Transplant Bacteria or Virome》指出,真正的重建远不止细菌这一层。
在细菌之外,病毒组——尤其是噬菌体——也许才是维系肠道生态稳定的隐形力量。
传统 FMT 的制备方法往往聚焦于细菌,而忽视了病毒组与代谢因子的存在。
研究团队以系统图的方式展示了几种粪菌制备路径:从粗过滤的传统 FMT,到改良的洗涤菌移植(washed microbiota transplantation),再到更为纯化的细菌孢子制剂,以及去除细菌后仅保留病毒组的粪便病毒移植(fecal virome transplantation, FVT)。
这些方法的演进,折射出人类对“健康生态”理解的深化——从单纯的菌群重建,走向更精细的生态设计。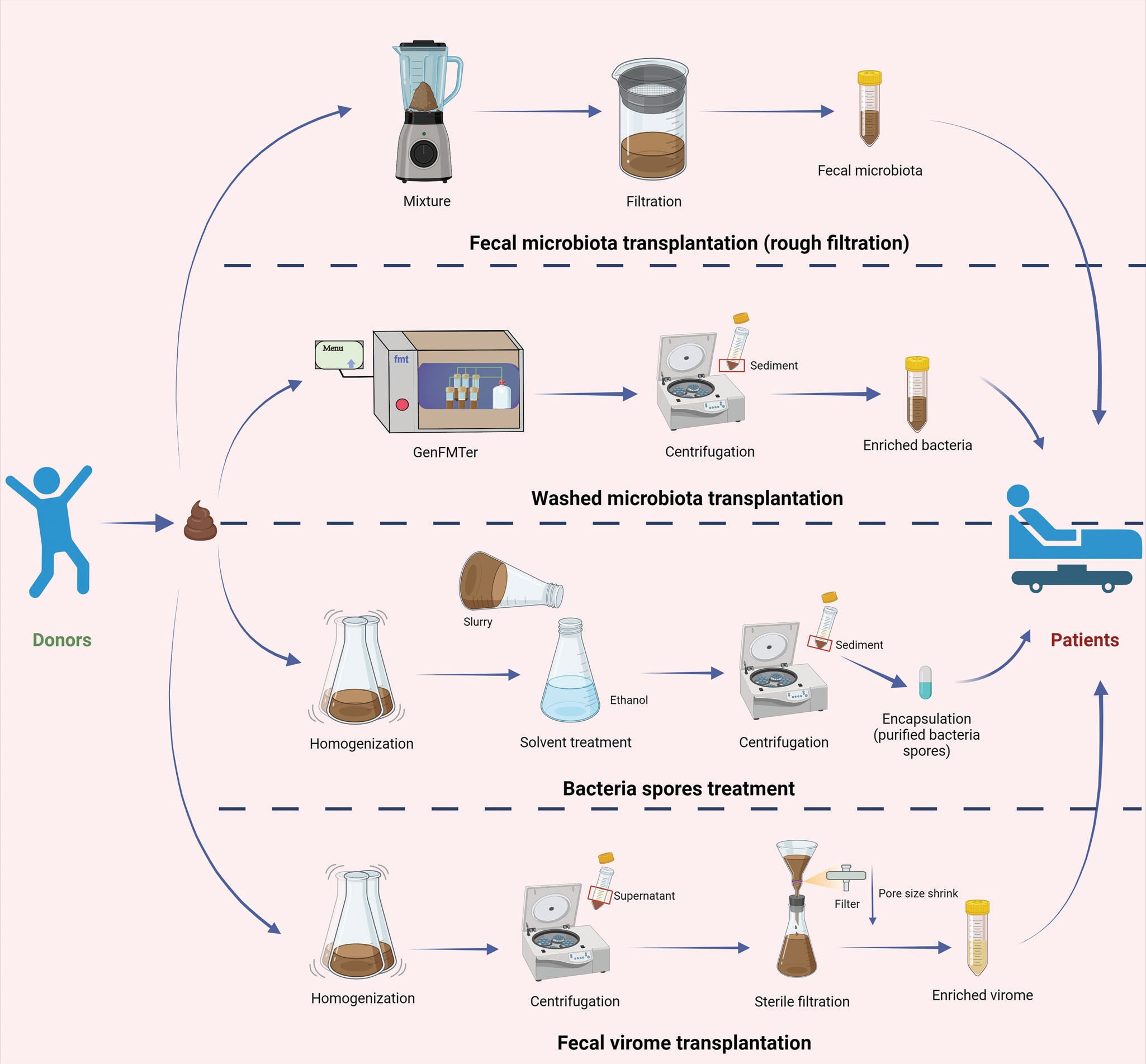
图1|粪菌移植的制备理念与方法
图中展示了四种粪菌移植制备路径:传统粗滤 FMT、洗涤菌移植、细菌孢子制剂与病毒组移植。它们分别代表了从“原生态移植”到“定义性移植”的技术演化。
随着研究的深入,科学家发现噬菌体可能是肠道健康的关键调节者。
它们寄生于细菌,却能通过捕食和基因转移调控群落结构,像无形的指挥者维系着平衡。
在动物实验和临床案例中,单独移植病毒组(FVT)也能部分恢复菌群稳态,缓解炎症或代谢紊乱。
这意味着,FMT 的疗效并非仅由细菌驱动,而是源于更复杂的生态网络。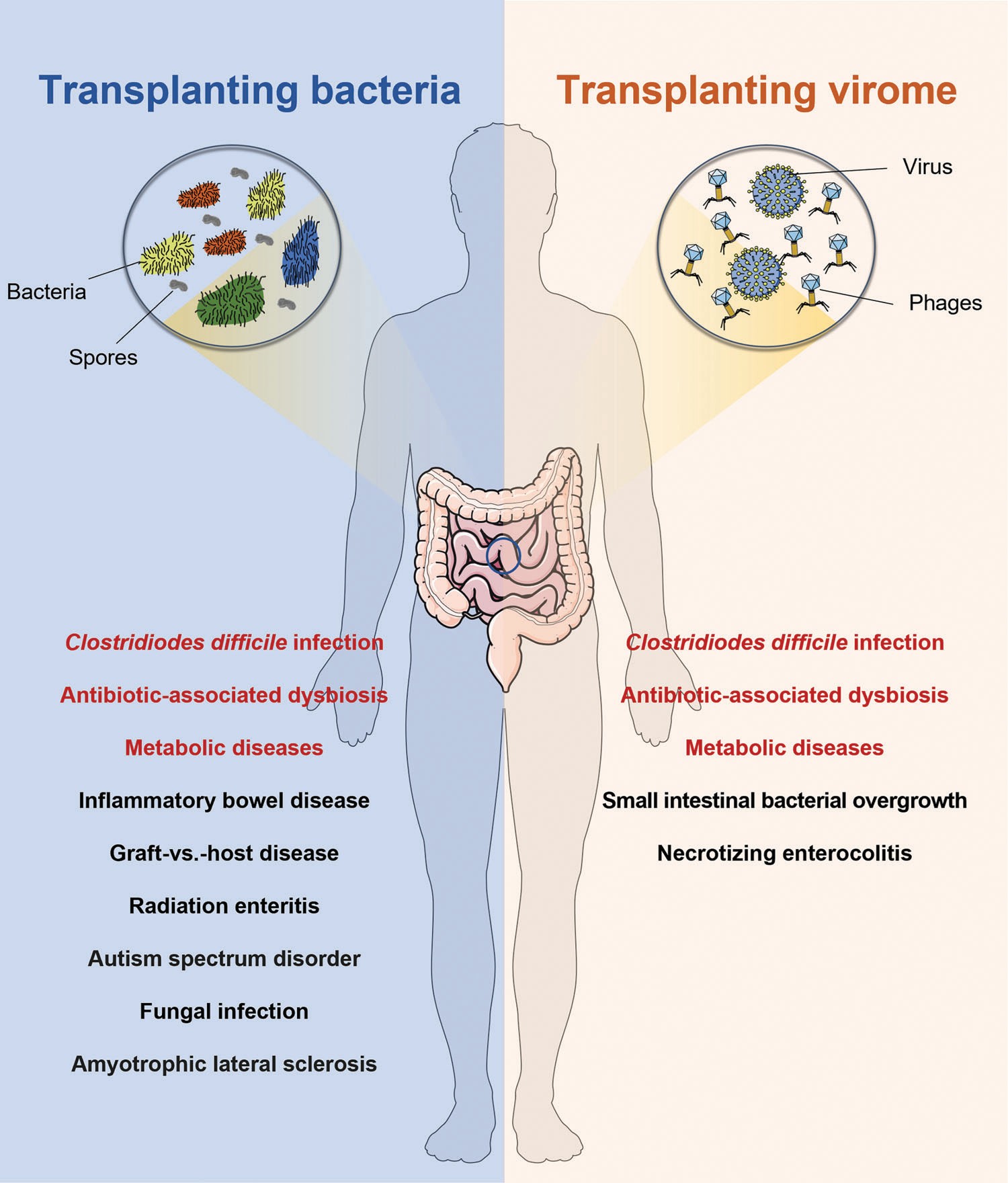
图2|细菌或病毒组移植的应用领域。
图表总结了当前已有临床或动物证据支持的应用方向:细菌移植在感染与代谢疾病中已具实践基础,而病毒组移植正在神经、免疫相关疾病中崭露头角。两者重叠的红色区域,象征着未来可能的融合疗法。
论文指出,下一代 FMT 将不再是“换粪”,而是“重建生态”。
这场转变既是技术的更新,也是理念的升华。
研究者提出,理想的移植应兼顾细菌、病毒与代谢分子的多维平衡,使移植材料更具可控性与可追溯性。
在未来,FMT 或将以人工合成的“生态药物”形态出现,既含定义菌株,也包含定向筛选的噬菌体群落,用于精准调控肠道稳态。
然而,作者也提醒我们:在迈向这一目标的途中,仍有未解之谜——
噬菌体在宿主中的长期稳定性、不同个体间的兼容性,以及生态移植的伦理与监管问题,都需要科学界共同面对。
正如论文结语所言:“我们正处在粪菌移植的新纪元,从细菌到病毒,从单一到系统,医学正在学会与生态共谋。”
当我们再谈 FMT,也许应称它为一次“微观生态的再造”。
参考文献
Zhang, F., Luo, W., Shi, Y., Fan, Z., & Ji, G. (2023). The next generation fecal microbiota transplantation: to transplant bacteria or virome. Advanced Science, 10(8), 2205293. DOI: 10.1002/advs.202301097
来源: Advanced Science


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 合康谱精准医学科普基地
合康谱精准医学科普基地 
