在心血管医学的长久历史中,我们熟知的“危险因子”无非高脂、高压、高糖。然而,过去十年,一位新玩家悄然登场——肠道菌群。2020 年发表在 Circulation Research 的综述,由克利夫兰诊所的 Stanley Hazen 团队撰写,首次系统揭示了肠道微生物如何通过代谢产物影响心血管系统,从代谢、炎症到血栓形成,构建出一幅“肠道—心脏轴”的完整图景。
研究发现,肠道菌群能将膳食中的胆碱、肉碱及磷脂转化为三甲胺(TMA),经肝脏氧化生成三甲胺氧化物(TMAO)。TMAO 可促进胆固醇在血管壁沉积、增加血小板反应性,并激活炎症通路,从而显著提高动脉粥样硬化和心梗风险。血浆 TMAO 浓度每升高 10 μmol/L,心血管事件风险可上升约 20%。
更令人震撼的是,研究还揭示了另一条平行通路——苯乙酰谷氨酸(PAGln)。它由肠菌代谢芳香族氨基酸产生,可与肾上腺素能受体结合,增强心脏兴奋性和血压反应,从而触发急性心血管事件。换言之,PAGln 是“神经型”的心脏信号,而 TMAO 是“代谢型”的风险驱动,两者共同塑造了一个看不见的“化学阴影”。
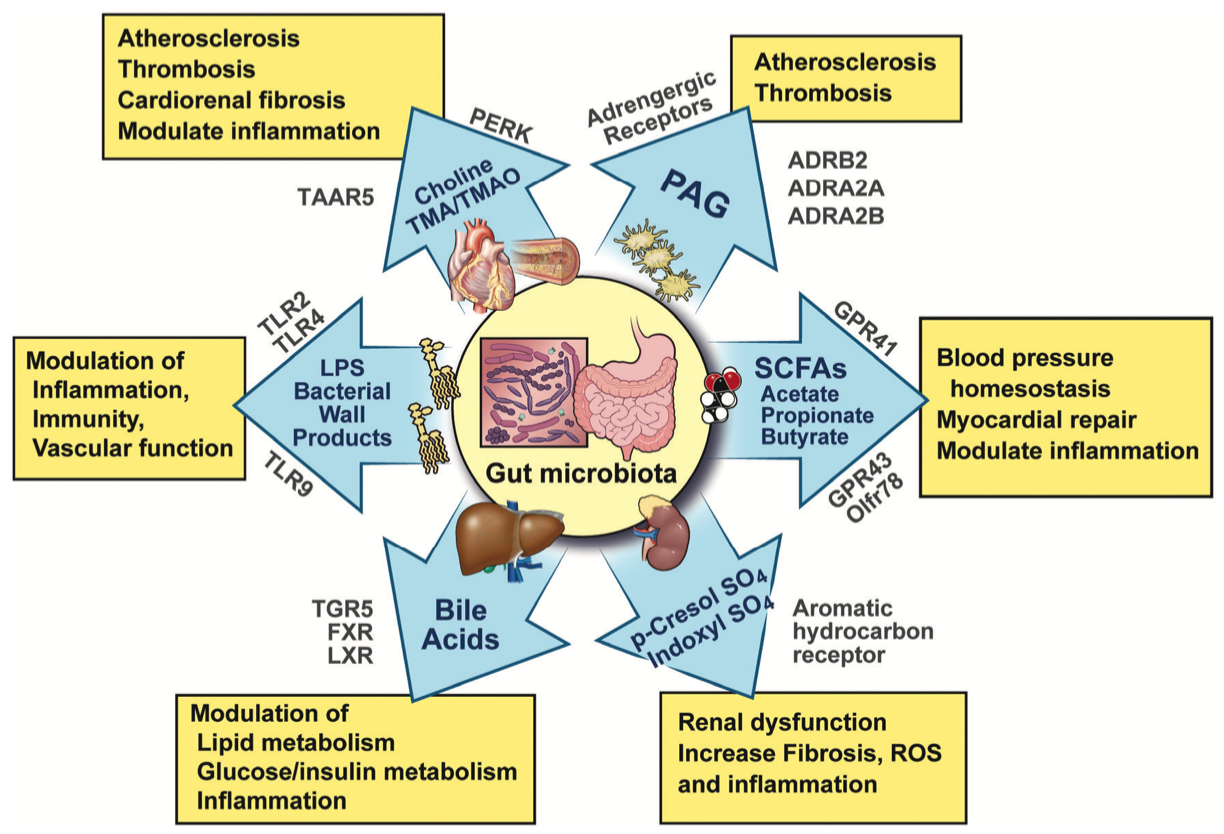
图1|肠道菌群如何通过代谢产物影响心血管系统
与此同时,论文指出,并非所有肠源代谢物都是敌人。短链脂肪酸(SCFAs)如乙酸、丙酸、丁酸,是膳食纤维经益生菌发酵的产物。它们能通过激活 GPR41、GPR43 和 Olfr78 受体调节血压与血管舒张,抑制炎症反应。相比之下,脂多糖(LPS)则由肠屏障受损后泄漏入血,通过 TLR4 受体引发系统性炎症,加速内皮功能障碍与动脉硬化。
表1|四类关键代谢物与心血管作用路径速览
| 代谢物 | 来源 | 作用靶点 | 心血管效应 |
|---|---|---|---|
| TMAO | 胆碱、肉碱 → 肠菌 CutC/D + 肝 FMO3 | 胆固醇转运、血小板活化、炎症 | 促进动脉粥样硬化与血栓 |
| PAGln | 芳香族氨基酸代谢 | 肾上腺素能受体(α₂A、β₂、β₃) | 增强心肌兴奋性与收缩压 |
| SCFAs | 膳食纤维发酵 | GPR41、GPR43、Olfr78 | 降压、抗炎、调节代谢稳态 |
| LPS | 肠道通透性增加 | TLR4 / NF-κB 通路 | 诱发慢性炎症与血管损伤 |
这些发现彻底颠覆了传统“胆固醇中心论”。它告诉我们,心脏病的风险不止取决于血脂,更取决于肠道的化学反应。Hazen 团队通过动物实验与人群数据证明:即使血脂正常,只要 TMAO 或 PAGln 升高,心梗风险仍显著上升。相反,通过调节菌群或阻断关键代谢酶,可在不改变饮食总热量的前提下降低风险。
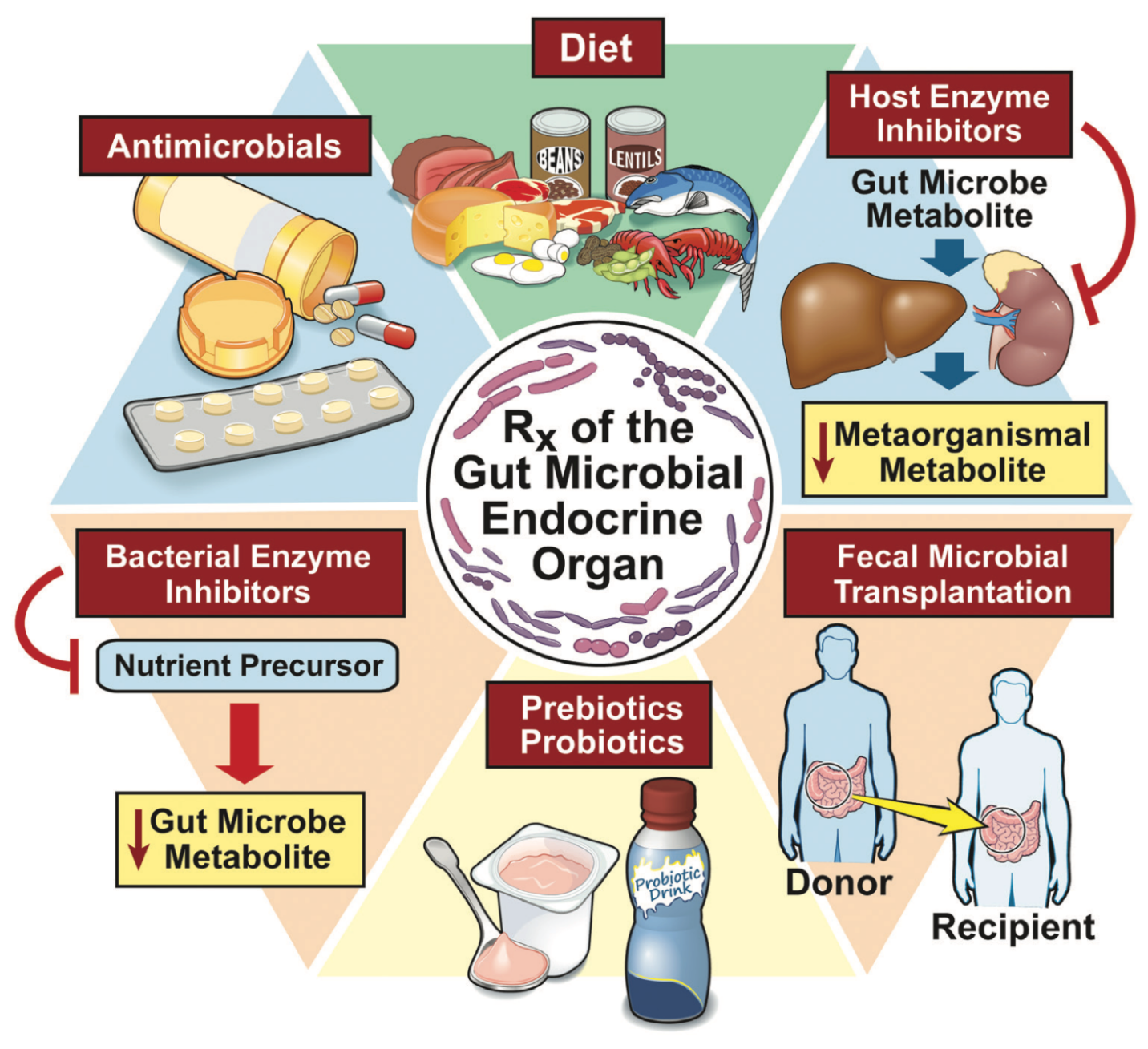
图2|如何通过调控肠道菌群改善心血管健康
🥦 饮食干预(Diet):多吃豆类、水果、蔬菜,少红肉、少油腻。
🧫 益生菌/益生元(Probiotics & Prebiotics):增加有益菌、提升肠道平衡。
💊 抑制细菌酶(Bacterial enzyme inhibitors):阻止菌群产生有害代谢物。
🧪 抗菌药物(Antimicrobials):选择性清除有害菌。
🧍♂️→🧍♀️ 粪菌移植(FMT):移植健康人的肠道菌群,重建生态。
🧬 宿主酶抑制剂(Host enzyme inhibitors):阻断人体将TMA转为TMAO的过程。
因此,未来防治心血管疾病的策略正在从“降脂”扩展为“控菌”。论文提出多种前沿方向:
饮食调控:减少红肉与蛋黄,增加膳食纤维与植物多酚,可抑制 TMA/TMAO 生成;
微生物酶抑制剂:如 DMB(3,3-二甲基-1-丁醇)能非致死性地抑制 CutC 酶;
益生菌与后生元疗法:恢复 SCFA 代谢通路,强化血管保护;
代谢监测与个体化营养:利用血浆 TMAO 与 PAGln 水平评估风险,实现“化学生态精准医学”。
这场革命的意义,不仅在于发现新靶点,更在于重塑医学观念:心血管病不是单一器官问题,而是系统代谢与微生物生态失衡的结果。 也许未来的心脏科医生,不止开他汀,也会为你开一份“肠道处方”。
参考文献:
Wang Z., Roberts A.B., Buffa J.A., et al. (2020). Gut Microbiota and Cardiovascular Disease. Circulation Research, 126(12), 1623–1645. https://doi.org/10.1161/CIRCRESAHA.120.316242
本文所用图片均为文献内Figure
来源: 合康谱精准医学科普基地


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 合康谱精准医学科普基地
合康谱精准医学科普基地 
