华中科技大学同济医学院附属协和医院/华中科技大学大学生快乐科普社团 王晓慧
在寒冷的冬日,我们常会搓手哈气取暖,可对一部分人来说,寒冷不仅是体感上的不适,更是诱发疾病的 “隐形杀手”。这类特殊人群患上的是一种名为 “冷凝集素病”(Cold Agglutinin Disease,简称 CAD)的罕见血液疾病,全球发病率仅约10-15%,因认知度低,常被误诊或漏诊。今天,我们就来揭开这种 “怕冷” 疾病的神秘面纱。
一、什么是冷凝集素病?从 “异常抗体” 说起
冷凝集素病本质是一种自身免疫性溶血性贫血,核心问题出在人体免疫系统的 “判断失误” 上 ——正常情况下,免疫系统会像 “卫士” 一样识别并清除外来病原体(如细菌、病毒);但在 CAD 患者体内,免疫系统会错误地产生一种名为 “冷凝集素” 的特殊抗体。这种抗体有个独特的 “习性”:在温暖环境下(如人体核心体温 37℃)相对 “安静”,一旦接触低温(通常低于 30℃,尤其在 10-15℃时),就会变得异常活跃,主动黏附在红细胞表面。
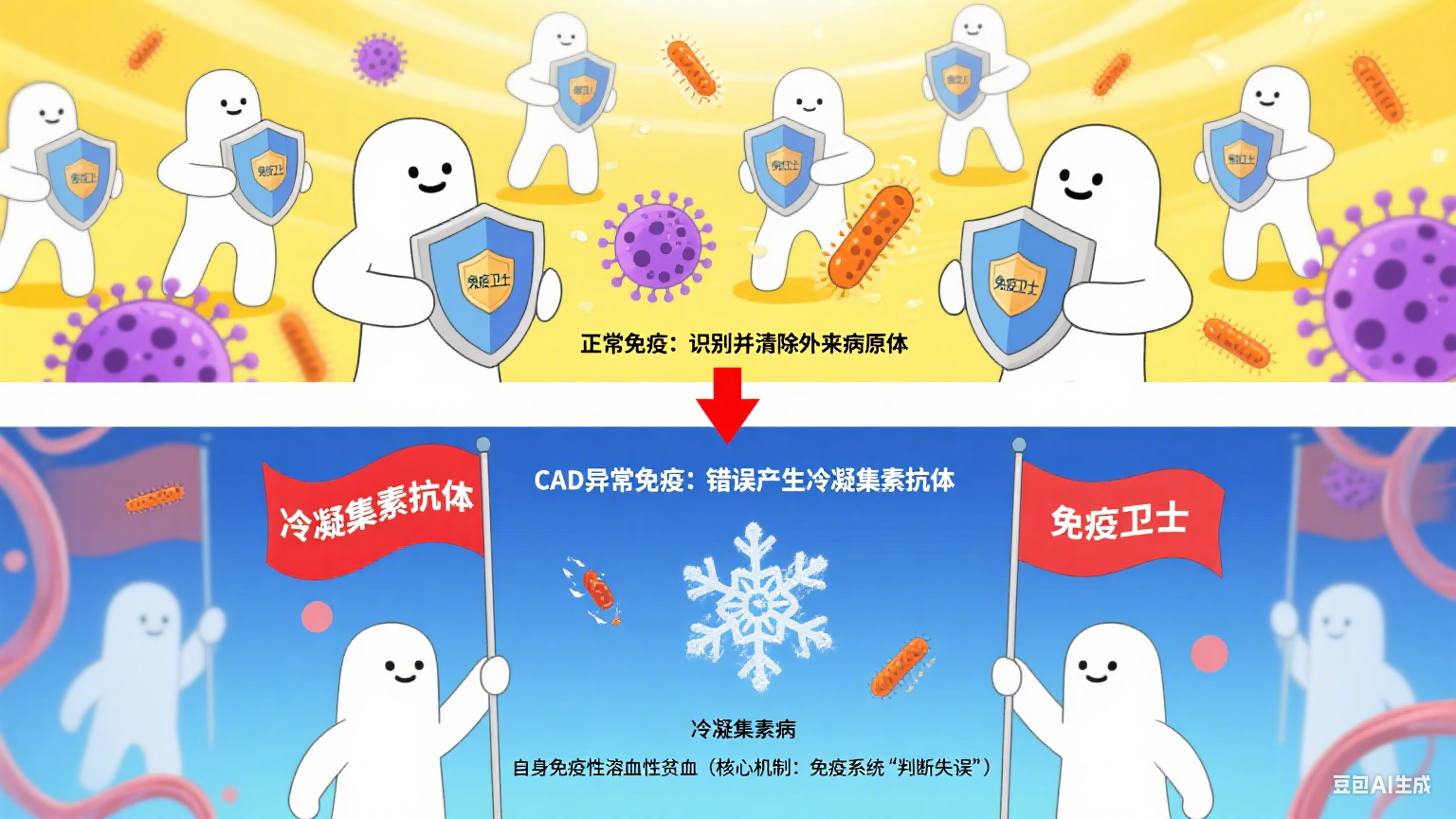
被抗体 “盯上” 的红细胞会出现两种危险情况:一是互相聚集、凝结成块,堵塞四肢或身体末端的小血管;二是被脾脏等免疫器官识别为 “异物”,进而被大量破坏( 溶血)。红细胞是携带氧气的 “运输兵”,一旦被大量破坏,就会导致贫血、缺氧,甚至引发器官损伤。
根据病因,CAD 可分为两类:
原发性 CAD:占比约 60%-70%,病因不明,多发生于 60 岁以上人群,女性略多于男性,病程通常为慢性,症状会长期存在。
继发性 CAD:由其他疾病诱发,常见诱因包括感染(如支原体肺炎、EB 病毒感染)、自身免疫病(如系统性红斑狼疮、类风湿关节炎)、血液系统肿瘤(如淋巴瘤、慢性淋巴细胞白血病)等,儿童和成人都可能患病,症状会随原发病的控制而缓解。
二、身体发出的 “寒冷预警”:这些症状别忽视
CAD 的症状与 “寒冷暴露” 高度相关,轻症患者可能仅在冬季出现轻微不适,重症患者则全年都可能发作,核心症状可归纳为三类:
1. 贫血相关症状:氧气不足的 “信号”
红细胞被破坏后,人体氧气供应不足,会出现一系列典型的贫血表现:
日常乏力、疲倦,哪怕没做重活也总觉得累;
头晕、头痛,站立或起身时症状更明显;
面色、嘴唇、指甲盖苍白,严重时呈 “青紫色”( 发绀);
心跳加快(心悸),稍微活动(如爬楼梯、走路)就气短、胸闷,甚至出现胸痛。
2. 寒冷诱发的 “特异性症状”:CAD 的 “标志性表现”
这是区别于普通贫血的关键,也是很多患者最初就诊的原因:
肢端症状(雷诺现象):手指、脚趾接触冷水或暴露在冷空气中后,会迅速出现 “苍白→发紫→潮红” 的三色变化,同时伴随麻木、刺痛、发凉,温暖后几分钟到几小时才能逐渐缓解。严重时,手指末端可能因血管堵塞出现溃疡、甚至组织坏死。

其他暴露部位症状:耳朵、鼻子、面部等暴露在外的部位,也可能出现发凉、发紫、僵硬,冬季戴口罩、围巾后症状会减轻。
3. 溶血相关并发症:红细胞破坏的 “后遗症”
红细胞大量破坏会产生一种名为 “胆红素” 的代谢产物,过量胆红素会导致:
皮肤、眼睛巩膜发黄(黄疸),尿液颜色变深,呈浓茶色或酱油色;
长期慢性溶血可能导致脾脏肿大,部分患者能摸到左上腹部有轻微隆起或肿块,按压时可能有隐痛。
警惕 “急症信号”:出现这些情况需立即就医
少数患者可能因寒冷刺激或感染诱发 “急性溶血危象”,出现以下危及生命的症状,需立即前往医院急诊:
突然高热、寒战、剧烈腰痛或腹痛;
尿量急剧减少(少于 400ml / 天),甚至无尿(急性肾衰竭信号);
肢体突然剧痛、发凉、发黑,无法活动(血管完全堵塞,可能导致截肢)。
三、如何确诊?这些检查是 “关键证据”
由于 CAD 罕见,症状易与普通贫血、雷诺病、冻疮等混淆,临床误诊率较高。
1. 基础检查:先判断 “是否贫血、是否溶血”
血常规:通过检测红细胞计数、血红蛋白浓度,判断是否存在贫血(成人男性血红蛋白<120g/L、女性<110g/L 即为贫血);同时观察红细胞形态,CAD 患者可能出现 “红细胞碎片” 或 “大小不一的红细胞”。
网织红细胞计数:网织红细胞是骨髓新生成的红细胞,CAD 患者因溶血导致红细胞减少,骨髓会 “加班” 生成新红细胞,因此网织红细胞计数会升高(正常参考值 0.5%-1.5%,患者可能达到 5%-10%)。
溶血指标检测:包括血清胆红素(间接胆红素升高,因红细胞破坏产生)、乳酸脱氢酶(LDH,红细胞内的酶,破坏后释放到血液中,数值升高)、结合珠蛋白(结合血红蛋白的蛋白,溶血时被大量消耗,数值降低),这些指标能间接证明 “红细胞正在被破坏”。
2. 核心诊断试验:冷凝集素试验
这是确诊 CAD 的 “金标准”,原理是模拟低温环境观察红细胞是否聚集:
医生抽取患者血液后,将其置于 4℃低温环境中,若血液中的冷凝集素活跃,红细胞会迅速聚集、沉淀,试管底部会出现明显的 “凝块”;
同时会检测 “冷凝集素效价”,正常人群效价通常<1:32,而 CAD 患者效价多≥1:64,部分重症患者甚至可达 1:1000 以上,效价越高,症状通常越严重。
3. 鉴别检查:排除其他疾病,寻找病因
直接抗人球蛋白试验(DAT,又称 Coombs 试验):检测红细胞表面是否结合抗体,CAD 患者通常为 “补体 C3 阳性、IgG 阴性”,这一结果能区别于其他类型的自身免疫性溶血性贫血(如温抗体型溶血性贫血多为 IgG 阳性)。
原发病筛查:若怀疑继发性 CAD,需进一步做感染筛查(如支原体抗体检测、EB 病毒检测)、自身抗体检测(如抗核抗体、类风湿因子)、肿瘤相关检查(如淋巴结超声、骨髓穿刺),明确是否由其他疾病诱发。

四、如何治疗与管理?“避寒” 是基础,治疗分轻重
冷凝集素病的治疗没有 “万能方案”,需根据病情轻重、是否有原发病等因素个体化制定,核心原则是 “减少寒冷暴露、控制溶血、处理原发病”。
1. 基础管理:做好 “保暖”,远离诱因
这是所有 CAD 患者的 “第一道防线”,也是最经济有效的预防措施:
冬季或寒冷天气外出时,务必做好全身保暖:戴手套、围巾、帽子、耳罩,穿保暖袜子、加绒裤子、防风外套,避免皮肤直接接触冷空气;
日常避免接触冷水:洗手、洗脸、洗菜用温水(建议水温≥37℃),不喝冰水、不吃冰饮,冬季避免用冷水洗衣服或拖地;
特殊场景防护:若需在低温环境工作(如冷库、冷链物流),需提前申请调整岗位;冬季洗澡时,先调节好浴室温度(建议 25℃以上),避免受凉。
2. 药物治疗:针对溶血,控制抗体
轻症患者:若仅在寒冷时出现轻微症状,无明显贫血(血红蛋白≥100g/L),可暂不用药,仅通过保暖和定期复查(每 3-6 个月查血常规、胆红素)监测病情。
中重症患者:若出现明显贫血、频繁溶血,需使用药物控制,常用方案包括:
利妥昔单抗:一种靶向 B 细胞的单克隆抗体,能减少冷凝集素的产生,是目前治疗原发性 CAD 的一线药物,通常需静脉输注,疗程为 4-6 周,有效率约 60%-70%。
其他免疫抑制剂:若利妥昔单抗效果不佳,可联用或换用硼替佐米、伊布替尼、苯达莫司汀等药物,尤其适合合并淋巴瘤的继发性 CAD 患者。
糖皮质激素(如泼尼松):短期使用可缓解急性溶血症状,但长期使用副作用大(如骨质疏松、血糖升高、免疫力下降),一般不单独作为长期治疗方案。
3. 紧急治疗:输血与原发病处理
输血治疗:仅在严重贫血(血红蛋白<60g/L)或出现明显缺氧症状(如呼吸困难、胸痛)时紧急使用,且输血时有特殊要求 —— 需将血液加热至 37℃左右(避免低温诱发溶血加重),同时选择 “冷凝集素效价低” 的供血者血液,防止输血后溶血加剧。
继发性 CAD 治疗:重点针对原发病,如感染诱发者需用抗生素,肿瘤诱发者需进行化疗或靶向治疗,自身免疫病诱发者需用免疫抑制剂,原发病控制后,冷凝集素病的症状也会随之缓解。
五、预后与生活:罕见病也能 “好好生活”
很多人听到 “罕见病” 会感到恐慌,但冷凝集素病的预后并非 “绝望”:
原发性 CAD 患者通过规范保暖和药物治疗,多数能控制症状,维持正常的生活质量,寿命接近普通人;
继发性 CAD 患者的预后取决于原发病,若原发病(如感染)能治愈,CAD 也可能完全缓解;若原发病为恶性肿瘤(如淋巴瘤),则需积极治疗原发病,CAD 症状会随肿瘤控制而改善。
对患者而言,除了医疗干预,心态调整也很重要:不必因 “罕见” 而焦虑,可通过加入罕见病患者社群(如中国罕见病联盟),与其他患者交流经验;同时定期随访血液科医生,根据病情变化调整治疗方案,避免因忽视保暖或漏服药物导致病情加重。
最后想说:认识它,才能更好地应对它
冷凝集素病虽罕见,但并非 “无迹可寻”—— 只要记住 “寒冷诱发症状、贫血 + 肢端发紫” 这两个关键特征,出现异常时及时就医,就能尽早明确诊断。对普通人而言,了解这种疾病也能帮助身边的患者:若大家发现有人冬天手指频繁发紫、怕冷且容易疲劳,不妨提醒 TA “或许需要做个血液检查”,你的一次关注,可能就是患者获得正确治疗的开始。
罕见病不 “孤单”,科学认知与规范管理,就能让 “怕冷” 的血液重新温暖起来。

参考文献
[1] 中华医学会血液学分会红细胞疾病(贫血)学组.中国成人自身免疫性溶血性贫血诊疗指南(2023年版).中华血液学杂志,2023,44(1):12-18.
[2] 刘京倩, 张凤奎. 冷凝集素疾病的诊疗进展.中华血液学杂志,2022,43(6):524-528.
[3] Berentsen S, Barcellini W. Autoimmune Hemolytic Anemias. N Engl J Med. 2021 Oct 7;385(15):1407-1419. doi: 10.1056/NEJMra2033982. PMID: 34614331.
[4] BERENTSEN S. How I trea t cold agglutinin disease . Blood,2021,137(10):1295-1303.
[5]Röth A, Barcellini W, D'Sa S, Miyakawa Y, Broome CM, Michel M, Kuter DJ, Jilma B, Tvedt THA, Weitz IC, Yoo R, Jayawardene D, Vagge DS, Kralova K, Shafer F, Wardȩcki M, Lee M, Berentsen S. Sustained inhibition of complement C1s with sutimlimab over 2 years in patients with cold agglutinin disease. Am J Hematol. 2023 Aug;98(8):1246-1253. doi: 10.1002/ajh.26965. Epub 2023 May 29. PMID: 37246953.
[6]Rossi G, Gramegna D, Paoloni F, Fattizzo B, Binda F, D'Adda M, Farina M, Lucchini E, Mauro FR, Salvi F, Marchetti M, Fazi P, Zaja F, Barcellini W. Short course of bortezomib in anemic patients with relapsed cold agglutinin disease: a phase 2 prospective GIMEMA study. Blood. 2018 Aug 2;132(5):547-550. doi: 10.1182/blood-2018-03-835413. Epub 2018 Jun 13. PMID: 29898955.
来源: 大学生快乐科普驿站


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 大学生快乐科普驿站
大学生快乐科普驿站 