系统性红斑狼疮(systemic lupus erythematosus, SLE)是一种多因素、病因复杂的自身免疫性疾病,形象地说,就如同人体免疫系统 “叛变”,调转矛头攻击自身组织与器官 。其症状表现多样,病程进展复杂,且在女性群体中高发。尤为棘手的是,SLE 早期症状隐匿,往往在患者毫无察觉时,器官损伤已悄然积累。因此,实现 SLE 的早期风险预测与精准分层,对疾病的有效管理与预防至关重要。
蛋白质组学聚焦于研究人体成千上万种蛋白质,致力于绘制蛋白质 “全景图谱”。作为连接遗传与疾病表型的 “中间桥梁”,它助力科研人员深入剖析复杂疾病(如 SLE)背后遗传或非遗传风险因素的作用机制,宛如借助显微镜洞察基因调控背后的精细奥秘。然而,目前学界对于大规模蛋白质组学特征与 SLE 发病风险间的关联,仍缺乏深入认知,即尚未明确蛋白质水平的动态变化对 SLE 发病的预示程度。但可以确定的是,深入挖掘蛋白质组学数据,有望揭示全新的疾病机制,锁定关键 “枢纽蛋白”,为研发 SLE 新型疗法提供突破口。
(图片来源于网络,版权归原作者)
针对这一研究空白,南方医科大学南方医院国家肾脏病临床医学研究中心展开了相关工作,研究成果发表于《Rheumatology》杂志。此项研究依托约 3000 种血浆蛋白质数据,成功构建出由 22 种蛋白组成的模型,该模型在预测 SLE 发病风险方面成效显著。南方医院国家肾脏病临床医学研究中心秦献辉教授为论文通讯作者,博士研究生杨思思为第一作者 。

研究团队纳入 28,220 名基线时未患 SLE 的女性参与者,并将其随机分为训练集与测试集。在训练集中,研究人员精准筛选出 22 种与新发 SLE 紧密相关的蛋白质,并以此构建血浆蛋白质预测模型。经检验,该模型在测试集(C 指数 = 0.801)与训练集(C 指数 = 0.819)中均展现出良好的 SLE 风险预测能力。与现有的基因风险模型(C 指数 = 0.638)及临床风险预测模型(C 指数 = 0.706)相比,此蛋白质模型优势显著,极大提升了预测效能。
通过对这 22 种蛋白质开展富集分析与网络分析,研究人员进一步明确,TNF、CD80 和 LGALS9 是 SLE 候选蛋白相互作用网络中的核心蛋白(见图 1)
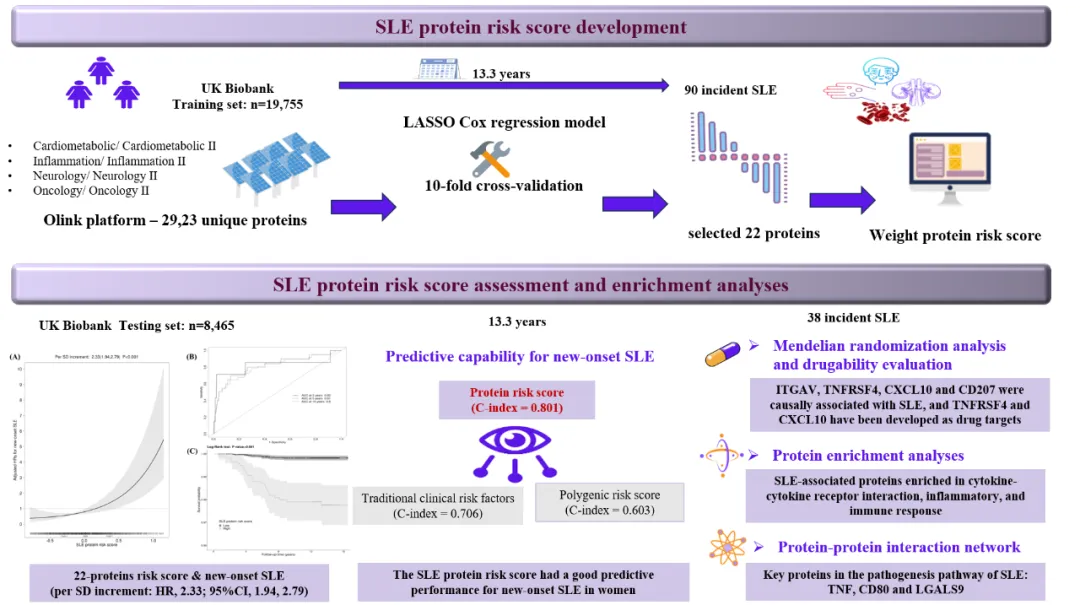
图1 研究结果示意图
研究团队还对这 22 种蛋白进行孟德尔随机化及药物靶点分析,结果显示,ITGAV、TNFRSF4、CXCL10 和 CD207 这 4 种蛋白与 SLE 存在直接因果关联。值得注意的是,TNFRSF4 和 CXCL10 已作为癌症与自身免疫性糖尿病的药物靶点,极有可能被重新开发,应用于 SLE 的临床治疗。
在临床实践中,血液样本采集简便易行,血浆蛋白检测具有高度客观性、可量化性以及操作便捷性。相较于传统依赖患者自我报告、医疗记录,或需多次繁复检查的临床危险因素收集方式,血浆蛋白检测在大规模人群筛查中优势尽显,能够快速、精准输出关键信息,规避冗长繁琐的评估流程。
综上所述,本研究证实,仅需一项简单的血浆蛋白检测,即可高效预测 SLE 发病风险。这为 SLE 风险预测开创了全新、便捷的方法,特别适用于大规模人群筛查与早期风险识别。借助该方法,不仅能够助力患者在疾病早期及时干预,还能有效降低疾病进展引发的长期损害,显著改善患者预后。
参考文献:Yang S, Zhang Y, Ye Z, et al. Plasma proteomics for risk prediction and identification of novel drug targets in systemic lupus erythematosus. Rheumatology (Oxford). Published online January 30, 2025. doi:10.1093/rheumatology/keaf055
编辑 | 杨思思 梁晓龙
审核 | 秦献辉 张园园
来源: 肾脏健康促进研究


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 肾脏健康促进研究
肾脏健康促进研究 
