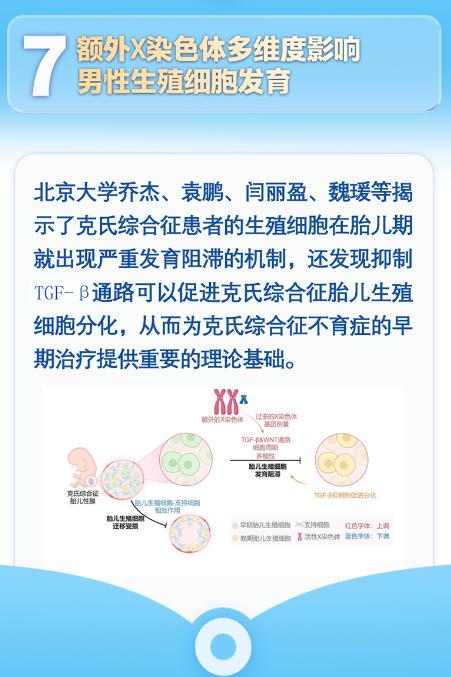
在北京大学第三医院的生殖医学中心,一位28岁的男性患者正接受染色体核型分析。镜下显示的47,XXY核型让医生们意识到,这个看似普通的不育病例背后,隐藏着X染色体与男性生殖细胞的激烈博弈。2024年,北大团队的最新研究揭示,额外X染色体的异常活跃,正是导致克氏综合征患者生殖细胞发育停滞的关键。
人类的性别由性染色体决定,正常男性为XY,女性为XX。但每500个男婴中就有1个携带额外的X染色体,成为47,XXY核型的克氏综合征患者。这些患者通常表现为睾丸发育不全、第二性征弱化和不育。传统理论认为,额外的X染色体会在胚胎发育早期通过XIST RNA介导的失活机制被"关闭",但北大团队通过单细胞测序技术发现,在XXY患者的精原细胞中,两条X染色体均保持活跃状态,导致X连锁基因的表达量比正常细胞高出50%。
这种基因剂量的失衡直接引发了生殖细胞的"发育危机"。在男性胚胎的性腺分化阶段,XY细胞会启动睾丸决定基因SRY,而XXY细胞却表现出异常的基因表达模式。研究人员发现,额外X染色体上的RPS4X基因过度表达,通过抑制SOX9蛋白活性,阻断了生殖嵴向睾丸分化的关键步骤。更致命的是,在青春期启动时,XXY精原细胞因XIST RNA的缺失无法完成减数分裂,导致生精过程停滞在精母细胞阶段。
TGF-β信号通路的异常激活成为另一个关键节点。在正常男性生殖细胞中,TGF-β通路维持着适度的活性,调控细胞增殖与凋亡的平衡。但在XXY细胞中,X染色体上的TGFBR3基因过度表达,导致该通路持续处于激活状态。这种"过度刹车"效应使精原细胞过早进入凋亡程序,导致睾丸组织中出现大量退化的生精小管。通过基因编辑技术敲低TGFBR3表达后,XXY细胞的凋亡率下降了40%,生精小管结构明显改善。
这些发现为男性不育症的治疗开辟了新路径。在动物实验中,研究团队通过慢病毒载体递送XIST RNA,成功诱导额外X染色体的沉默,使XXY小鼠的精子生成恢复到正常水平的30%。针对TGF-β通路的抑制剂临床试验也已启动,初步结果显示,使用ALK5抑制剂可使患者睾丸体积增大25%,血清抑制素B水平上升40%,这两项指标均与精子生成能力密切相关。
这项发表在《自然·医学》的研究,不仅改写了克氏综合征的病理机制,更揭示了性染色体剂量调控的普遍规律。在特纳综合征(XO)女性患者中,研究人员同样发现X染色体基因剂量异常与卵巢早衰的关联。这些发现为开发基于性染色体调控的精准医疗方案奠定了基础。
当我们凝视这些显微镜下的染色体,看到的不仅是遗传物质的排列组合,更是生命密码的精密调控。从基因剂量失衡到信号通路异常,每一步都在诉说着生殖细胞发育的复杂故事。未来,或许通过靶向XIST RNA或TGF-β通路,我们能为那些被染色体异常困扰的男性打开生育的新窗口。这些科学发现的光芒,终将照亮无数家庭的希望之路。
来源: 桂粤科普


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 桂粤科普
桂粤科普 
