在上海长征医院的病房里,一位硬皮病患者正接受最后一次随访。曾经僵硬如皮革的皮肤变得柔软,心肺功能的影像学检查显示纤维化病灶明显逆转。这不是科幻电影的情节,而是2024年中国科学家用异体CAR-T细胞创造的医学奇迹。这种源自健康供者的"通用型"免疫细胞,正以革命性的方式重塑自身免疫病的治疗格局。
免疫系统的"自我攻击"是自身免疫病的核心病机。当B细胞错误地产生针对自身组织的抗体,系统性红斑狼疮、硬皮病等疾病便悄然降临。传统疗法依赖激素和免疫抑制剂,如同给免疫系统蒙上眼罩,虽能暂时缓解症状,却无法根治疾病,且副作用显著。CAR-T细胞疗法的出现,为这些患者带来了新希望。这种通过基因编辑赋予T细胞精准识别能力的技术,在癌症治疗中已展现出惊人疗效,但自体CAR-T疗法的局限性始终制约其普及——每位患者需单独制备细胞,周期长达两周,成本高达百万,且部分患者因免疫系统受损无法完成细胞采集。
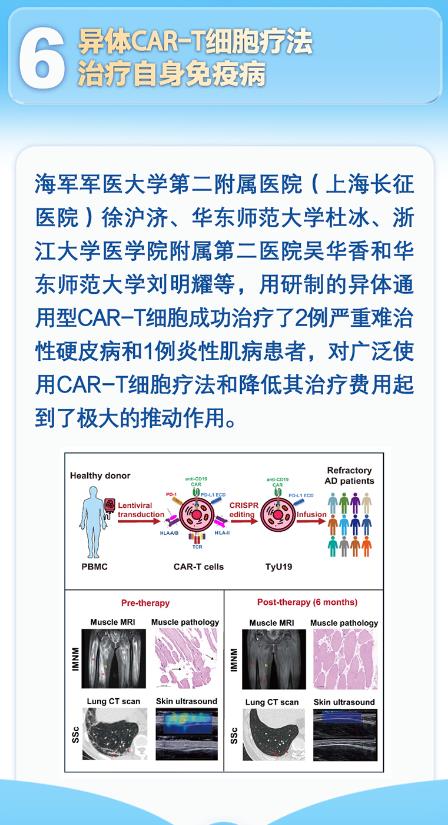
海军军医大学徐沪济团队的突破在于创造性地使用健康供者的T细胞,通过基因编辑技术解决异体排斥难题。他们开发的TyU19型CAR-T细胞,如同经过严格训练的"通用士兵",既能精准清除异常B细胞,又避免了移植物抗宿主病(GVHD)的风险。在首批临床试验中,两名硬皮病患者和一名炎性肌病患者接受治疗后,皮肤硬度、肌肉力量和器官功能均出现显著改善,部分患者甚至实现了纤维化逆转。这种疗效突破传统认知,因为纤维化通常被认为是不可逆的组织损伤。
技术创新的关键在于"基因剪刀"的巧妙运用。研究人员通过CRISPR/Cas9技术敲除T细胞受体(TCR)基因,避免异体T细胞攻击患者正常组织;同时敲除HLA基因,降低宿主免疫系统对供体细胞的识别。这种双重编辑如同为CAR-T细胞穿上"隐身衣",使其在患者体内存活时间延长至6个月以上,确保持续清除异常B细胞。更令人惊喜的是,这种通用型疗法只需一份健康供者的血液,即可制备200份CAR-T细胞,将治疗成本降低至自体疗法的十分之一。
这种"现货供应"模式正在改变临床实践。在浙江大学医学院附属儿童医院,毛建华团队用自体CAR-T疗法成功治疗20例难治性红斑狼疮患儿,所有患者症状缓解并停用激素。而通用型CAR-T的优势在儿童患者中尤为显著——部分患儿因长期使用免疫抑制剂导致T细胞功能受损,自体疗法难以实施。如今,健康供者的"优质细胞"成为新选择,治疗周期从数周缩短至数天。
尽管取得重大突破,科学家仍在不断优化技术。在安全性方面,研究人员通过调整清淋预处理方案,将细胞因子释放综合征(CRS)发生率降至15%以下,且所有患者均未出现严重神经毒性。针对不同自身免疫病的靶点研究也在展开:靶向CD20的CAR-T细胞已进入类风湿关节炎临床试验,而双特异性CAR-T技术则试图同时调控B细胞和异常T细胞,为多发性硬化症等复杂疾病提供解决方案。
站在技术革新的临界点,我们看到的不仅是医学的进步,更是生命科学的无限可能。从癌症治疗到免疫修复,CAR-T细胞的跨界应用正在重新定义疾病治愈的边界。未来,或许每位自身免疫病患者都能像使用抗生素一样,便捷地接受"通用型"细胞治疗,彻底摆脱终身用药的困扰。这些源自健康供者的"生命种子",终将在患者体内绽放出治愈的希望之花。
来源: 桂粤科普


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 桂粤科普
桂粤科普 
