精子老矣,尚能用否?
撰文 | 阿拉蕾(同济大学医学院内科学硕士)、晓蕊(上海交通大学医学院妇产科学博士)
由于社会、经济、工作压力、高学历教育等因素的影响,夫妇结婚、生育的年龄越来越晚。近年来,我国逐步放开计划生育,有意愿生育二孩、三孩的男性也越来越多。众所周知,随着女性年龄的增加,生育力逐步下降。但是,年龄对男性生育力的影响,似乎关注度较低。在我们的传统中,男性常有“先立业,后成家”的思想,也常拿出一些名人的例子来:赌王78岁生女,齐白石79岁得子……能不能生,似乎主要看女方的因素。
何鸿燊与最小的女儿何超欣丨来源网络
事实真是如此吗?
男性的生育年龄真的没有上限吗?
男性终生具备生育能力——理论上是
“理论上”!
一切要从精子的发生说起。精子来源于睾丸,严格意义上,来源于睾丸的精曲小管。精子的发生始于干细胞的分化,干细胞(stem cell)中的“干”,意义为“起源”,即“起源细胞”,具有无限的自我更新和分化潜能。精子的发生过程可以简单归纳为:干细胞→精原细胞→初级精母细胞→次级精母细胞→精子细胞→精子。只有当精原细胞的总体数量显著减少时,干细胞才会进入分化阶段。男性精子的发生在性成熟后持续进行,直至个体死亡。
年龄增加,尤其是到了50岁以上,精子质量有变化吗?有关睾丸组织学以及精液质量,在这方面缺少具有代表性的数据,现有数据之间也存在差异,因此难以给出圆满的解答。
组织学方面,并未发现老年人的睾丸体积有普遍萎缩的情况;精液质量方面,由于各研究所纳入人群的特征不同,精子活动能力、精子浓度、精子数量等指标结果存在差异。有研究显示,60岁以上生育过的老年人,各指标(例如睾酮水平、精子数量等)与年轻父亲之间无明显差别;也有研究显示,在25~50岁的人群中,精子浓度随年龄增长逐渐降低[1]。总体来说,与女性绝经期相比,男性的生育功能不会突然丧失,从理论上来说,男性终生具备生育能力。
为什么说“理论上”?
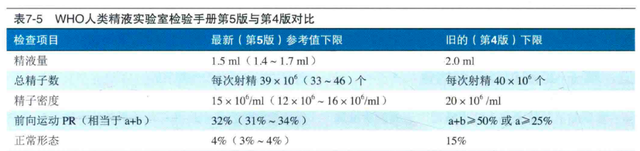
精子的发生过程受许多因素的影响,包括基础疾病(例如:慢性肾功能/肝功能不全、糖尿病等)、内分泌水平、电离辐射、药物、重金属、吸烟、饮食、饮酒等,也与特发性因素有关。前面的都好理解,什么叫“特发性因素”?就是说人群中精子质量已经发生了系统性改变。根据既往研究,当精子浓度<30~55×106/ml时,生育能力开始下降。但是,过去15年内的多项研究报道,年轻男性(18~21岁)的中位精子浓度为41~55×106/ml,这说明相当比例的男性精液质量不佳,而这种普遍的下降趋势已经持续了几十年[2]。甚至,世界卫生组织(WHO)人类精液实验室检验手册更新[3]时,把部分精液质量指标进行了下调。
WHO精液质量指标更新[3](点击看大图)
中国的数据也不容乐观。在15年(2001~2015)的观察期内,研究者共对30636名青年男性(平均年龄21.6岁)进行了精子质量评估。结果显示,精子浓度由68×106/ml下降至47×106/ml,正常形态比例由31.8%下降至10.8%,合格捐助者的比例由55.8%下降至17.8%[4]。
此外,很多与精子生成本身无关的男性疾病也会影响受孕的成功率。例如输精管疾病、阴茎勃起功能障碍(ED)、射精障碍等。说起不孕不育,人们会自然的把目光首先投向女方。事实上,虽然关于不孕原因的数据在各地区有所差异,但总体来说,单纯为女方原因的占约1/3,单纯为男方原因的占约1/3,男女双方都有问题的占约1/3。
没有任何疾病
没有任何不良生活习惯
是否就代表“老来得子”不是难事?
但是,生娃,
也希望要生一个健康的娃!
让我们先来看一组数据。
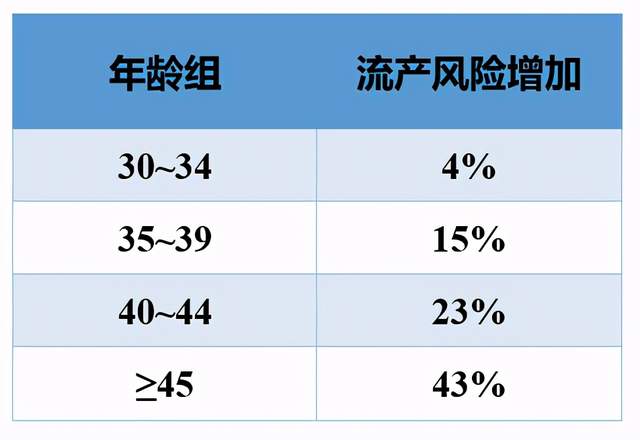
首先,是妇产科领域的权威杂志 Human Reproduction update 在2020年发表的一篇Meta分析。众所周知,高龄女性会对生育造成不利影响,而这项分析结果显示,高龄男性同样与自然流产的风险增加有关。30~34岁、35~39岁、40~44岁、≥45岁年龄组,流产风险分别增加4%、15%、23%和43%。与女性相比,可能男性年龄增加带来的影响没有那么明显,但也同样需要引起重视。[5]
第二,孩子出生,对全家来说都是高兴的事情。但是,全球著名的四大医学期刊之一《英国医学期刊》(BMJ)抛出了一组数字。科学家对美国2007~2016年出生的、共40 529 905名新生儿及其父母的资料进行了分析,排除了母亲的诸多影响因素后,父亲年龄>45岁,早产的概率提高14%,孩子患癫痫的概率提高18%,新生儿低体重的发生率提高14.5%,孩子进入重症监护室的概率提高15.1%,需要机械通气的概率提高8.6%,出现其他并发症的概率提高12.2%。[6]
第三,在现实生活中,如果孩子在生长发育过程中出现问题,人们会首先把目光投向母亲。但是要知道,父亲的精子对受精卵也有一半的贡献,不能把锅都甩给母亲。例如,自闭症是广泛性发育障碍的一种代表性疾病。有研究对132271名儿童进行回顾性分析,发现父亲年龄超过40岁,子代自闭症的发病率是父亲年龄<30岁的5.75倍[7];另有一项研究,对14 231名自闭症患儿与56 924名健康儿童进行分析后也发现,40岁以上男性所生育子代的自闭症发病风险是20岁男性的3.3倍[8]。不仅是自闭症,男性高龄生育与子代患精神分裂症、情感障碍、白血病、中枢神经系统疾病等风险增加也多有报道。
等一下
不是说,男性“终生”具备生育能力?
就算精子数量、浓度上有所降低
那也就是“量”的变化
为何还会造成上面说的这些不利影响呢?
没错,除了量变,还会有质变!
我们就重点谈谈基因的那些事儿!
基因是个体的遗传密码,而染色体是基因的载体。基因异常,会增加不育、胎停、流产、出生缺陷的风险。高龄女性不孕的原因中,非整倍体(即:染色体数目异常)是重要原因之一。什么叫“非整倍体”?精子或卵子的染色体为23条,以n表示;胚胎细胞的染色体是46条,以2n表示,是整数倍。“非整倍体”是指细胞内染色体数目增加或减少了1条或数条。例如,某号染色体少了1条,就叫单体型(2n-1);某号染色体多了1条,就叫三体型(2n+1)。(详见《生娃有危险?怕娃不健康?冻卵可取吗?破解“高龄”女性生育难题》)
和卵子相似,精子也会出现非整倍体。出现非整倍体的主要原因也是在减数分裂期,染色体未正确分离。有数据显示,非整倍体精子的发生率为5%~7%;年龄和非整倍体发生率之间的关系,尚缺少质量较高的研究,现有研究结果并不统一。
在自然流产和先天缺陷中,非整倍体可以来源于父亲、母亲,也可以来源于受精卵最初的几次分裂。随着人类基因组工程的进展,现有研究发现,除了少数几种染色体异常的类型,84%~100%常见非整倍体异常来自卵子染色体数目的异常,只有0~7.7%来自精子[9]。因此,与女性相比,男性非整倍体精子对后代的危险性较小。
既往对精子质量的常规检测,主要包括精液量、精子数量、精子密度、正常形态等。近年来,精子DNA碎片(SDF,sperm DNA fragmentation)成为评价精液质量的新指标。SDF是指各种原因下,精子核DNA或线粒体DNA发生单链或双链断裂,导致父源基因完整性受损的情况。造成SDF的具体机制尚不明确,目前主要有精子成熟障碍(注:精子对自身DNA修复的能力和环境适应能力降低)、精子凋亡异常(注:细胞通过某种方式逃过了正常的凋亡途径,而产生了异常精子)和氧化应激(注:外源性、内源性活性氧的影响)3种学说。
精子碎片化率(DFI,DNA fragmentation index)对男性生育影响的研究也不断增加,在这里举几个例子。
1、DFI与男性不育。有研究显示,正常精液中,DFI为13.0±7.3%;在不育男性精液中,DFI达到40.9±14.3%[10]。此外,DFI与常规精液检查指标(精子计数,精子形态,精子向前运动率)呈负相关[11]。就是说,DFI值越高,常规的精液检查指标也越差。
2、DFI与反复流产。国内有研究显示,有反复流产史患者的丈夫,有37.5%的精子DFI>30%,而正常生育者的丈夫中仅有25.8%有这样的情况。[12]
3、DFI与胚胎发育及子代健康。对于自然受精的胚胎,较高DFI可能导致胚胎遗传不稳定,子代出现遗传性疾病或先天性疾病的风险增加;对于辅助生殖技术培育的胚胎,还可能会降低移植成功率。
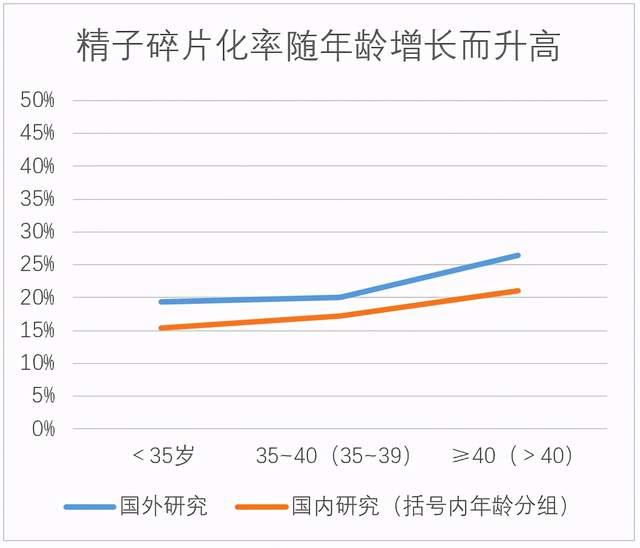
年龄与DFI之间的关系,较多研究均已证实。国外研究显示,45岁以上男性精子DFI水平为32.0%,30岁及以下男性则为15.2%,前者是后者的两倍。40岁以后,精子DFI水平快速增加,30~35、35~40、40~45岁男性的精子DFI分别为19.4%、20.1%、26.4%[13]。国内的研究结果与国外的趋势基本相符,<35岁、35~39岁,>40岁男性的DFI分别为15.4%、17.2%和21.1%。[14]
需要说明的是,这里仅针对非整倍体和DFI进行了讨论,除此以外,高龄男性的DNA突变、表观遗传学的改变,也都会对子代健康产生影响。因此,当高龄男性有生育需求时,精子的遗传学评估也有其必要性,在临床上也越来越受到重视。
总 结
的确,与女性相比,男性生育力可以维持的时间较长。戒烟、戒酒、生活规律、适当锻炼、有病治病的情况下,身体状态在一定程度上还是可以靠努力保持。然而,衰老是无法避免的,年龄增长是不可改变的事实。高龄喜得子女的例子的确存在,但同样伴随着“概率”和“风险”。随着辅助生殖技术的发展,高龄男性可以通过体外受精(IVF)或卵胞浆内精子注射(ICSI)等方式来助孕。
但是,辅助生殖技术并不能保证可以排除所有可能存在的遗传学异常,尚有许多问题等待人们去解答。还是那句话,除了在准备生育前进行孕前咨询和相关医学检测,最好的办法就是“在合适的时间,做合适的事”。
参考资料
[1] 主编 郭应禄,辛钟成,金杰. 男性生殖医学(第2版).北京大学医学出版社.2016.
[2] Helena E Virtanen, Niel Jorgensen, Jorma Toppari. Nat Rev Urol. 2017; 14(2): 120-130.
[3] 谷翊群等 译. 世界卫生组织人类精液检查与处理实验室手册(第五版). 人民卫生出版社. 2011)
[4] Chuan Huang, Baishun Li, Kongrong Xu, et al. Fertil Steril. 2017; 107(1): 83-88.
[5] Nadia A du Fosse, Marie-Louise P van der Hoorn, Jan M M van Lith, et al. Hum Reprod Update. 2020; 26(5): 650-669.
[6] Yash S Khandwala, Valerie L Baker, Gary M Shaw, et al. BMJ. 2018; 363: k4372.
[7] Reichenberg A, Gross R, Weiser M, et al. Arch Gen Psychiatry. 2006; 63(9): 1026-1032.
[8] Buizer-Voskamp JE, Laan W, Staal WG, et al. Schizophr Res. 2011; 129(2-3): 128-32.
[9] 史庆华,许波,杨庆岭,等. 中国科学技术大学学报. 2008;38(8):883-889
[10] Sergerie M, G Laforest, L Bujan, et al. Hum Reprod. 2005; 20(12): 3446-3451
[11] Oya Sena Aydos, Yunus Yukselten, Fuat Kaplan, et al. Turk J Urol. 2015; 41(4): 191-197
[12] 刘成军,王蔼明,商微,等. 中华男科学杂志. 2011;17(7):619-621.
[13] 2Sergey I Moskovtsev, Jennifer Willis, J Brendan M Mullen. Fertil Steril. 2006; 85(2): 496-9.
[14] 乜照燕,吴海峰,张娜,等. 中国计划生育学杂志. 2012;20(1):30-36.
来源: 返朴


 科普中国公众号
科普中国公众号
 科普中国微博
科普中国微博

 帮助
帮助
 返朴
返朴