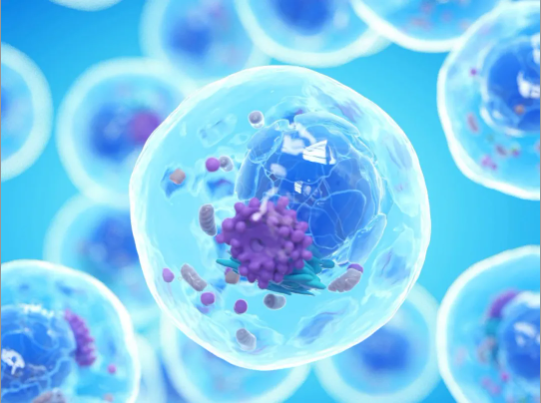
在当代科技迅猛发展的背景下,干细胞作为一种前沿技术备受瞩目。然而,要确保其在治疗和研究中的安全和有效性,高质量的干细胞至关重要。而“高质量”并非仅仅取决于单一指标,而是由多重因素共同影响。
细胞的来源是影响其质量的首要因素之一。不同的细胞来源可能会影响其遗传特性、稳定性以及功能表达。因此,在选择干细胞时,必须考虑其来源的质量和适用性,以确保所选细胞具有最佳的治疗潜力。
01****选择正规医疗机构
首先,要选择正规的医疗机构。细胞治疗是一项复杂的医疗技术,需要专业的医疗团队和先进的医疗设备。因此,选择正规的医疗机构是保证细胞质量的第一步。

02****了解细胞的来源
获得高质量的干细胞所需的细胞来源的重要性不言而喻。细胞供者本身的年龄和身体状况都会对细胞质量产生影响。
年龄因素是易于理解的,因为随着人类的老化,细胞的活力会逐渐减弱。英国利兹大学的科研团队在2019年通过体外培养的实验证实:年轻人的骨髓间充质干细胞增殖能力明显优于老年人。
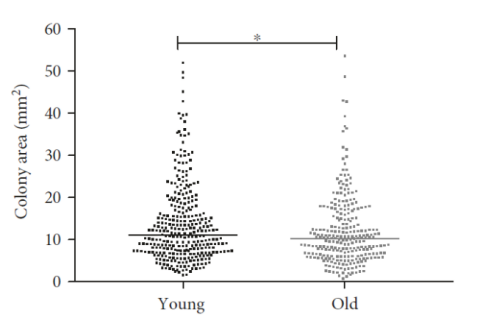
Young(19-37)与old(61-76)岁年龄组细胞生长活力对比
年轻组的生长面积及总量明显高于老年组
考虑到年龄因素,有关围产组织的脐带、胎盘以及羊膜间充质干细胞(通常被称为零岁细胞)应被视为首选来源。其次是年轻人的骨髓和脂肪间充质干细胞。然而,老年人的自体干细胞治疗并不被推荐,因其活力可能随着年龄的增长而减弱。

年轻人与老年人体内细胞对比
在进行供体的多能干细胞治疗前,必须审慎考虑供体本身的身体状况。
根据《生物样本库多能干细胞管理技术规范》的规定,必须采用经过验证的方法对干细胞进行真菌、细菌、传染病原体(包括HIV、HBV、HCV、HTLV、HCMV、EBV、TP等)和支原体的检测。然而,这些检测只构成了基本要求。
除了病毒感染外,许多疾病也会对自体间充质干细胞的功能和疗效产生影响,例如遗传性疾病、自身免疫性疾病以及某些慢性疾病等。
以糖尿病为例,根据2017年发表在《Stem Cells Translational Medicine》(影响因子:6.9)的研究,长期患有2型糖尿病会降低干细胞的增殖能力、免疫抑制潜力和存活率。特别是在患有糖尿病超过10年且较为肥胖的情况下,采用自体干细胞进行治疗可能不是明智的选择。(根据262个案例的证实,输注间充质干细胞可能是糖尿病的长期解决方案)

长期患2型糖尿病及肥胖会影响自体骨髓间充质干细胞的疗效
03****关注细胞存活率
当干细胞或免疫细胞进入体内,只有活着的细胞能真正起到修复或治疗的作用,失活细胞不仅有碍疗效,有时还会“帮倒忙”,引发机体毒性反应。
所以细胞存活率不但关乎细胞质量,更涉及人体自身的安全。也正因如此,T/CSCB-0002和T/CSCB-0005都要求未冻存细胞存活率****≥90%
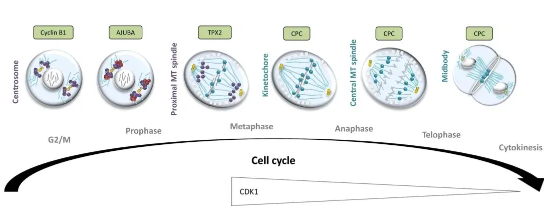
04****细胞的活性--代次
细胞代次是指干细胞在体外培养中的传代次数。最初从脐带、胎盘、羊膜等提取的干细胞是原始P0代,每传一代则称为P1代干细胞,以此类推。在这个过程中,有一个关键特性:干细胞的生物学效力和增殖特性会随着传代次数的增加逐渐下降。

图a代表P3代,图b代表P8代
按照这个论据,如果我们追求高活性,只需使用最初从组织中分离的P0代干细胞,对吗?然而,情况并非如此简单。
首先,细胞代次并不宜低于3代
根据这个论据,追求高活性时仅使用从组织中分离的P0代干细胞并不是最佳选择。虽然P0代干细胞在活性方面表现出色,但存在两个主要问题:
首先,P0-P3代干细胞的数量可能不足以满足治疗需求。在过去的临床试验中,干细胞通常达到千万级以上,而P0-P3代干细胞刚开始培养,数量相对较低,可能无法达到治疗标准。
其次,P0-P3代干细胞的安全性可能存在问题。由于培养时间短,可能没有足够的时间进行彻底净化,导致残留有害物质,如细菌、病毒或微生物。因此,尽管这些代次的干细胞活性高,但从安全性角度来看存在潜在风险。
另外,从各代干细胞的生长曲线检测结果来看,P4-P7代干细胞的活性也在高水平范围内,并且与前三代没有明显断层差距。因此,综合考虑各方面的优势和缺点,P0-P3代干细胞并不是最佳选择,不必过分追求前三代干细胞。
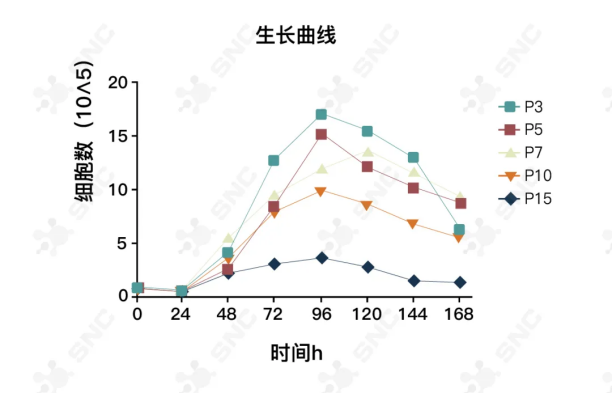
体外培养P3/5/7/10/15代细胞的生长曲线
其次,细胞代次不宜高于7代
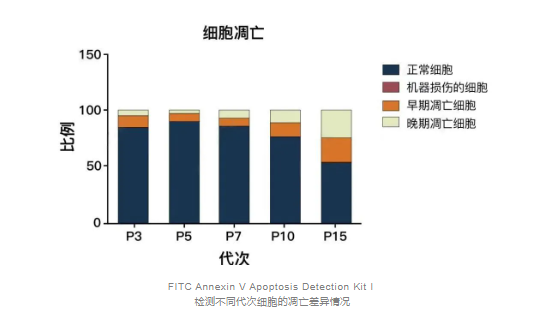
在P7代之后的干细胞中,经历了充分的培养和扩增,细胞数量增加,但质量却急剧下降。研究表明,随着代次的增加,干细胞的增殖能力和遗传稳定性急剧减弱,凋亡现象愈加严重。到了P15代晚期,凋亡细胞数量已经达到了50%,因此这样的干细胞显然不适合用作移植的选择。
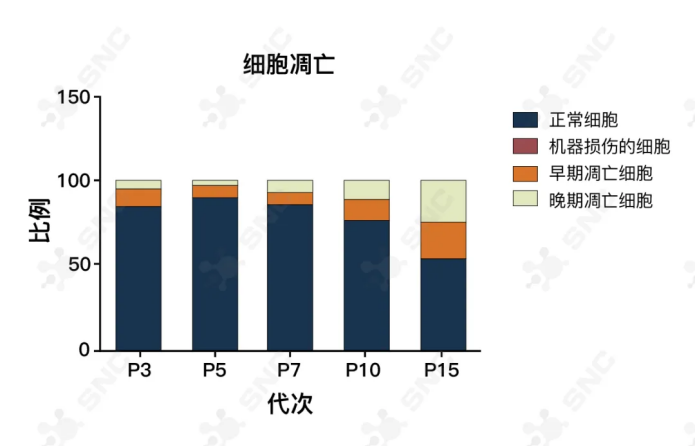
FITC Annexin V Apoptosis Detection Kit I
检测不同代次细胞的凋亡差异情况
**几代细胞最优质?**结论:
就间充质干细胞**(MSCs)而言,临床应用的最佳代数应该在4~7****代。**
有研究分别对胎盘间充质干细胞P5、P10和P15代细胞的增殖能力进行了检测,结果显示P5代间充质干细胞的增殖能力明显高于P10和P15代,实验结果表明,胎盘间充质干细胞在体外培养时,随着细胞代次的增加,细胞会逐渐出现的老化。 由于胎盘干间充质细胞在P5代后增殖能力会逐渐的下降,所以作为**临床应用时最好选择****P5(含)**代以下的为宜。
原因:
首先,细胞代次并不宜低于3代。
处于这个代次的干细胞确实活性很高,可惜的是,它还没能经过足够的体外培养、扩增,这样可能导致:
**一、细胞总数量不够。**我们能看到在过往的干细胞临床试验里,干细胞使用量几乎都是千万级以上的,而P0-P3代次的干细胞才刚刚开始培养,干细胞含量客观来说很低,很有可能达不到使用标准。哪怕它各项活性都很好,也巧妇难为无米之炊。
二、**细胞安全性不够。**培养时间短,也意味着来不及进行彻底净化,其中可能残留提取过程中感染的细菌、病毒、微生物等有害物质。尽管这些代次的干细胞有很高的活性,但于安全角度,却十分堪忧。
从各代干细胞生长曲线检测结果来看,P4-P7****代的数据其实也都在高活性范围之内,并未与前3代细胞形成断层差距,所以总结所有优势与缺点,P0-P3****代细胞并不是优选。
其次,建议用于临床应用的脐带间充质干细胞,体外培养最好不超过第5****代。
P7代之后的干细胞,算是经过了足够的培养扩增,这细胞数量是上去了,但质量也是断崖式下跌。有研究表明,P7代次之后,干细胞增殖能力及遗传稳定性急剧下降,细胞凋亡的数量也很可怕,到了P15代晚期,凋亡细胞数量直奔50%。
研究表明( 利用无血清培养基培养的 )脂肪间充质干细胞在传代至5代的过程中,生物学特性及遗传特性基本稳定,没有明显变化。初步揭示了脂肪间充质干细胞体外传代至第5代(含)以内可以安全使用。
所以在兼顾数量、安全及干细胞活性三方因素后,P4-P7****代次的细胞会是最佳选择。
小结
总结来说:一份细胞的质量优劣由多重因素共同决定,包括细胞活率、细胞来源、细胞活性等。如果只关注其中某一指标,可能会影响疗效,甚至引发安全问题。
然而,随着干细胞技术的不断成熟,国家也在不断完善干细胞质量管控体系。整个行业正朝着规范化、更加长远地利于临床转化的方向发展。相信在未来,高质量的干细胞不再需要我们拥有“火眼金睛”,更多人们可以切身体会到干细胞的“神奇”。
免责声明:内容来源于网络,版权归原作者所有。本文为科普性知识,仅作信息交流之目的,不具备任何临床治疗建议或方向,不做商业用途,如涉及作品内容、版权和其它问题,请联系我们删除
END